Hémochromatose
Hémochromatose
Hémochromatose
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
LES HYPERFERRITINEMIES<br />
EN MEDECINE INTERNE<br />
Dr V Loustaud-Ratti<br />
Service Pr Vidal Limoges
INTRODUCTION<br />
F LA FERRITINE : paramètre biologique de référence pour<br />
évaluer le stock en fer de l’organisme<br />
UNE FERRITINE BASSE: Facile!<br />
Mais une FERRITINE ELEVEE ?<br />
F plus de 50 % des HF ne sont pas associées à une surcharge en fer<br />
Questions:<br />
Quelle est la signification d ’une hyperferritinémie ?<br />
La ferritine est-elle un outil de dépistage en dehors des carences martiales?<br />
F coût du dosage : nomenclature B 70 (18.80 EUROS)
PROTEINES ET METABOLISME DU FER<br />
Protéine de transport : transferrine et son récepteur<br />
Saturation transferrine >0.45 = surcharge<br />
<br />
<br />
<br />
<br />
Protéine de stockage : ferritine<br />
IRP : Iron Regulatory Proteins<br />
régulation de la synthèse de la ferritine et de la transferrine<br />
surcharge : augmentation ferritine diminution transferrine<br />
carence : diminution de la ferritine augmentation de la transferrine<br />
Ferroportine : protéine de l ’excrétion du fer hors des cellules+++ pôle<br />
basal des entérocytes et autres cellules<br />
Hepcidine : hormone de synthèse hépatique, chef d’orchestre de<br />
l’absorbption et de la localisation cellulaire du fer en fonction des besoins
PROTEINES ET METABOLISME DU FER<br />
Hepcidine : hormone de synthèse hépatique, chef d’orchestre de l’absorbption et<br />
de la localisation cellulaire du fer en fonction des besoins<br />
Découverte de l’hepcidine par les Rennais en 2001 dans le modèle murin<br />
J Bio Chem 2001<br />
Institut Cochin : Nature Genetics 2003 (Gaël Nicolas)<br />
Souris génétiquement modifiées<br />
Hyperexpression du gène de l’hepcidine au niveau hépatique<br />
anémie (id anémie inflammatoire ou séquestration macroph du fer et<br />
hyperproduction d’hepcidine<br />
Perspective : inhiber la production d’hepcidine à la source ou élaboration<br />
d’antagonistes de l’hepcidine<br />
Absence d’expression du gène de l’hepcidine au niveau hépatique<br />
Tableau de surcharge ferrique majeure et décès. Si hepcidine inj survie<br />
Pourparlers avec société de biotechnologie européenne pour traduire<br />
l’hepcidine en molécule pharmaceutique utilisable chez l’homme
Transferrine<br />
Récepteur<br />
Transferrine<br />
Saturé<br />
cellule<br />
ferritine<br />
Pôle basal<br />
ferroportine<br />
Gène IRE<br />
Hepcidine
GENETIQUE ET SURCHARGE EN FER<br />
<br />
1996 : découverte du gène HFE mais mécanisme de l ’hyperabsorption du fer<br />
non élucidé<br />
Mutation C282Y chromosome 6<br />
• HFE2 : hémochromatose juvénile, chromosome 1, identification ?<br />
2000 : Récepteur 2 à la transferrine (TFR2) : Homozygotie Y250X chromosome 3<br />
Familles italiennes et portugaises.<br />
<br />
2001 : Mutation du gène de la ferroportine 1 (SLC11A3) surcharge ferrique avec<br />
hyperferritinémie, saturation normale ou peu augmentée, surcharge réticuloendothéliale,<br />
saignées moins bien tolérées.Transmission familiale dominante<br />
<br />
2002 : <strong>Hémochromatose</strong> juvénile par mutation du gène de l’hepcidine
GENETIQUE ET SURCHARGE EN FER<br />
<br />
1996 : découverte du<br />
HFE<br />
gène<br />
1<br />
HFE mais mécanisme de l ’hyperabsorption du fer<br />
non élucidé<br />
Mutation C282Y chromosome 6<br />
HFE 2<br />
• HFE2 : hémochromatose juvénile, chromosome 1, identification ?<br />
HFE 3<br />
2000 : Récepteur 2 à la transferrine (TFR2) : Homozygotie Y250X chromosome 3<br />
Familles italiennes et portugaises.<br />
<br />
<br />
2001 : Mutation du gène de la ferroportine<br />
HFE<br />
1 (SLC11A3)<br />
4?<br />
surcharge ferrique avec<br />
hyperferritinémie, saturation normale ou peu augmentée, surcharge réticuloendothéliale,<br />
saignées moins bien tolérées.Transmission familiale dominante<br />
HFE 6<br />
2002 : <strong>Hémochromatose</strong> juvénile par mutation du gène de l’hepcidine
HEMOCHROMATOSE GENETIQUE HFE1<br />
HFE 1 chromosome 6 (Nat Genet 1996, 13, 399- 408)<br />
H63D<br />
H65C<br />
Fer lié à la transferrine<br />
HEPCIDINE ?<br />
Béta 2 microglob<br />
S<br />
S<br />
Re de la transferrine<br />
Membrane plasmatique<br />
Pas de mutation C282 Y : lien normal avec la béta 2 microglobuline.<br />
HFE joue son rôle régulateur
HEMOCHROMATOSE GENETIQUE<br />
HFE 1 chromosome 6 (Nat Genet 1996, 13, 399- 408)<br />
H63D<br />
H65C<br />
Fer lié à la transferrine<br />
HEPCIDINE?<br />
Béta 2 microglob<br />
S<br />
S<br />
Re de la transferrine<br />
Membrane plasmatique<br />
C282 Y empêche le lien avec la béta 2 microglobuline : le fer rentre en masse. HFE ne joue<br />
plus son rôle régulateur.
HEMOCHROMATOSE GENETIQUE<br />
En France, la mutation C282Y à l ’état homozygote est<br />
quasiment exclusive.<br />
Elle correspond à 96 % des phénotypes hémochromatose<br />
(Italie : 79 %).
EXPRESSION PHENOTYPIQUE<br />
Elle évolue en trois phases :<br />
* de 20 à 30 ans : asthénie, ostéoarthropathie, cytolyse<br />
* de 40 à 50 ans : diabète, cirrhose, cardiomyopathie,<br />
hypogonadisme,<br />
* > à 50 ans : cancer du foie.
LE DEPISTAGE GENETIQUE FAMILIAL<br />
Information et consentement écrit. Remise par le médecin<br />
On ne demande que la mutation C282Y<br />
Pas de prise en charge<br />
Il se fait chez les parents, dans la fratrie, chez les enfants.<br />
La loi interdit la pratique du génotypage chez le sujet mineur.<br />
ÖOn peut proposer le génotypage chez le conjoint.<br />
ÖSinon, le génotypage peut se faire à partir de l ’âge de<br />
15 - 17 ans.
L ’EXPRESSION PHENOTYPIQUE<br />
La pénétrance est variable et souvent incomplète.<br />
ÖElle varie en fonction du sexe :<br />
* Hommes 25 - 40 ans : expression si saturation supérieure à 50<br />
% constante mais variable<br />
* Femmes 35 - 50 ans : expression si saturation supérieure à 45<br />
% dans seulement 50 % des cas.<br />
ÖFacteurs acquis ou génétiques<br />
¥facteurs exogènes augmentant la surcharge ferrique<br />
¥polymorphisme génétique (interactions avec les protéines jouant un rôle dans le<br />
métabolisme du fer).
QUELLE EST LA SIGNIFICATION<br />
D ’UNE HETEROZYGOTIE C282Y ?<br />
- L ’index hépatique en fer est le même dans la population C282Y et<br />
la population non mutée. La saturation de la transferrine n ’est pas<br />
différente dans les deux groupes.<br />
- Seule la mutation C282Y - H63D à l ’état de double hétérozygotie<br />
s ’associe à une petite surcharge en fer (Feder Nat Genet 1996)<br />
Et à une petite augmentation de la saturation de la transferrine.
QU ’EN EST-IL DE LA MUTATION H63D ?<br />
L’hétérozygotie H63D correspond à un simple<br />
polymorphisme génétique sans conséquence clinique.<br />
L ’homozygotie H63D s ’associe à une augmentation de la<br />
saturation de la transferrine mais pas d ’augmentation de<br />
la ferritine (Moirand Gastroenterology 1999).
FACTEURS FAVORISANT L ’EXPRESSION<br />
DES HETEROZYGOTIES C282Y - H63D,<br />
DE LA DOUBLE HETEROZYGOTIE H63D ET C282Y<br />
ET DE L ’HOMOZYGOTIE H63D<br />
* Insulinorésistance<br />
* Alcool<br />
* Cirrhose<br />
* Porphyrie cutanée tardive
GENETIQUE ET SURCHARGE EN FER<br />
HEMOCHROMATOSE GENETIQUE :<br />
HFE2 : hémochromatose juvénile, chromosome 1, transmission auto récessive<br />
Mutations : gène de l’hémojuvéline (OMIM 602390) située en 1q21<br />
Ou gène de l’Human antimicrobial peptide (HAMP, OMIM606464)<br />
Clinique : adultes jeunes 15 - 25 ans<br />
<br />
Hospitalisation urgence : insuffisance cardiaque ou cirrhose<br />
décompensée + hypogonadisme<br />
Pas de mutation C282Y<br />
Recours thérapeutique :<br />
- Vitamine C mobilise le fer à partir du cœur,<br />
- Traitement par DESFERAL et saignées : efficacité +++ évite la double<br />
transplantation (Am J Human Genet 1999, 64 - 1388-93)
GENETIQUE ET SURCHARGE EN FER<br />
HEMOCHROMATOSE GENETIQUE :<br />
Hepcidine : 2001 équipe rennaise : son absence est responsable dans<br />
le modèle murin de surcharge en fer<br />
Description d ’une hémochromatose juvénile par mutation du gène de<br />
l ’hepcidine : situé en 19q13<br />
atteinte cardiaque gravissime et insuffisance endocrinienne majeure<br />
première ou deuxième décennie<br />
différente de l ’HJ classiquement liée au chromosome 1 dont le gène<br />
n ’est pas identifié.<br />
Pigeon C J Biol Chem 2001; 16 : 7811-9<br />
Nicolas G Proc Natl Acad Sci USA 2001; 98 : 8730-5<br />
Roetto A Blood 2002; 100 : 733- 4
GENETIQUE ET METABOLISME DU FER<br />
<br />
Syndrome hyperferritinémie cataracte<br />
Ë<br />
autosomal dominant<br />
Ë<br />
cataracte nucléaire congénitale symptômes ou non<br />
Ë<br />
Ë<br />
4 mutations décrites sur le gène IRE (iron responsive element) de la<br />
sous-unité L : augmentation de la L ferritine (non régulée par le fer)<br />
par hyperproduction cellulaire (cataracte?)<br />
Ö sujet jeune hyperferritinémie sans surcharge = examen ophtalmologique
PRINCIPALES ETIOLOGIES RECONNUES<br />
DANS LA LITTERATURE<br />
HYPERFERRITINEMIES PAR SURCHARGE<br />
& Surcharges primitives<br />
<strong>Hémochromatose</strong> génétique<br />
& Surcharges secondaires par fréquence<br />
Ø hépatosidérose dysmétabolique<br />
Øalcool<br />
Øanémies chroniques<br />
Øporphyrie cutanée tardive<br />
Øtransfusions érythrocytaires multiples<br />
Øinsuffisance rénale chronique dialysée (avant érythropoïétine)<br />
ØSIDA (stade avancé)
PRINCIPALES ETIOLOGIES RECONNUES<br />
DANS LA LITTERATURE<br />
HYPERFERRITINEMIES PAR SURCHARGE<br />
& Surcharges rares<br />
acéruléoplasminémie congénitale (coeff sat normal)
PRINCIPALES ETIOLOGIES RECONNUES<br />
DANS LA LITTERATURE<br />
HYPERFERRITINEMIES SANS SURCHARGE<br />
& Syndromes inflammatoires<br />
Maladies inflammatoires chroniques dont les pathologies<br />
de système<br />
Infections<br />
& Lyses cellulaires<br />
cytolyse hépatique aigüe ou chronique (ferritine non glycosylée)<br />
tumeurs solides ou hémopathies malignes (glycosylation faible<br />
ou nulle)<br />
& Les syndromes hémophagocytaires<br />
& Maladie de Still
PRINCIPALES ETIOLOGIES RECONNUES<br />
DANS LA LITTERATURE<br />
HYPERFERRITINEMIES SANS SURCHARGE<br />
Pathologies à part<br />
Dysthyroïdies<br />
Syndrome hyperferritinémie cataracte héréditaire<br />
Maladie de Gaucher
Quelques commentaires: Ferritine et<br />
inflammation<br />
La ferritine est une protéine de l ’inflammation.<br />
a) Hyperferritinémie majeure non corrélée aux autres protéines de<br />
l ’inflammation = rechercher une autre cause que l ’inflammation<br />
b) Une ferritine normale ou discrètement élevée au cours d ’un<br />
syndrome inflammatoire majeur = rechercher la carence martiale<br />
(anémie non spécifique); intérêt de la ferritine érythrocytaire
Quelques commentaires: Ferritine et STILL<br />
[ maladie inflammatoire<br />
hépatites aigües<br />
hémophagocytose<br />
mais aussi<br />
[ Van Reeth : diminution de la fraction glycosylée 3.7%<br />
(vs 65 % chez les témoins, 30.2% autres M de Système)<br />
(J Rheumatol, 1994)<br />
Outil diagnostique dans les atteintes articulaires fébriles?
Quelques commentaires: Ferritine et cancer<br />
"Mécanismes possibles :<br />
- cellules néoplasiques : isoferritine acide glycosylation faible<br />
ou nulle<br />
- réponse inflammatoire : glycosylation normale<br />
- transfusions répétées : ferritine basique glycosylée<br />
- insuffisance hépatique<br />
"Taux élevés : marqueur de métastase et évolutif<br />
hépatoK, ovaire, neuroblastomes, tm germinales,<br />
mélanomes<br />
poumons, sein<br />
LMC, LMNH<br />
"Taux modérés ou bas : TD et urogénitaux
Syndrome hyperferritinémie cataracte<br />
Ëautosomal dominant<br />
Ëcataracte nucléaire congénitale symptômes ou<br />
non<br />
Ë4 mutations décrites sur le gène IRE (iron<br />
responsive element) de la sous-unité L :<br />
augmentation de la L ferritine (non régulée par le<br />
fer)<br />
par hyperproduction cellulaire (cataracte?)<br />
Ösujet jeune hyperferritinémie sans surcharge =<br />
examen ophtalmologique
METHODOLOGIE<br />
ETUDE RETROSPECTIVE<br />
PATIENTS CONSECUTIFS<br />
RECRUTES SUR 3 ANS<br />
EN HOSPITALISATION<br />
REPONDANT AU CRITERE D ’HYPERFERRITINEMIE ><br />
240 ng/ml<br />
> 300 ng/ml
269 DOSSIERS EXPLOITABLES<br />
F moyenne d’âge : 64 ans (extrêmes de 20 et 95<br />
ans)<br />
F sex-ratio H/F : 1,6<br />
F motifs d’hospitalisation :<br />
- variés<br />
- HF dans 9 cas
OBJECTIFS<br />
F déterminer les ≠ étiologies d’une ferritine<br />
élevée dans un recrutement de Médecine<br />
Interne<br />
F étudier la signification biologique d’une<br />
ferritine élevée<br />
F déterminer une CAT pratique devant une HF
METHODES STATISTIQUES<br />
ÖLes comparaisons de moyennes : test t de Student ou analyse<br />
de variance (ANOVA) en fonction de la taille de l ’échantillon)<br />
ÖLes corrélations : test r de Pearson ou rho de Spearman en<br />
fonction de la taille de l ’échantillon<br />
ÖLe degré de signification a été retenu pour un risque<br />
alpha = 0.05
RESULTATS GLOBAUX
syndrome inflammatoire : 61 % des cas<br />
anémie : 63 % des cas
HYPERFERRITINEMIES : REPARTITION DES ETIOLOGIES<br />
12 %<br />
12 %<br />
3 % 2 %2 %<br />
29 %<br />
Hépatopathies<br />
Pathologies malignes<br />
Infections<br />
Maladies systémiques<br />
Divers<br />
Lyses cellulaires<br />
<strong>Hémochromatose</strong>s primitives<br />
Hémophagocytoses<br />
19 % 21 %<br />
18 % des patients ont 2 ou plus pathologies associées
pathologies associées : 11 %
**PATHOLOGIES ASSOCIEES 19,6 %
pathologies associées : * 18 %
RESULTATS EN FONCTION DES<br />
ETIOLOGIES
LES HEPATOPATHIES<br />
n = 100
syndrome inflammatoire : 30 % des cas<br />
cirrhose : 5 % des cas
Les hépatosidéroses dysmétaboliques (n = 32) :<br />
caractères cliniques et paracliniques<br />
F sexe masculin (Sex ratio 7)<br />
F âge moyen (55.8 +/-12.6)<br />
F pléthorique<br />
F pas de pathologie associée le plus souvent<br />
F pas d’expression clinique de la maladie<br />
F un élément du syndrome X dans plus de 95 % des cas :<br />
- BMI >25 : 78 %<br />
- HTA : 34%<br />
- dyslipidémie : 68 %<br />
- perturbation du métabolisme glucidique : 41 %<br />
F HF modérée et CS normal dans 76 % des cas
Les hépatites chroniques C (n = 22) :<br />
caractères cliniques et paracliniques<br />
F sexe masculin (sex ratio 2.1)<br />
F âge moyen (53.7 +/- 14.5)<br />
F hépatite chronique active : score de Knodell moyen 8,9 +/-<br />
3,3<br />
F réalisation du dosage à la recherche d’un facteur de<br />
résistance au traitement<br />
F HF faible (59% 1000), 50 % sat > 0.45)
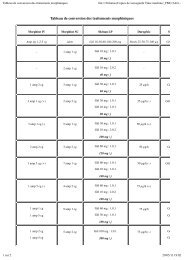
563 614 483 1120 4829 593<br />
moyenne des taux de ferritine en ng/ml<br />
le CS et le fer sérique sont significativement plus élevés vs autres<br />
étiologies<br />
corrélation faible entre ferritine et CS<br />
les HCC et les hémochromatoses ont un CS plus élevé vs HSD
LES PATHOLOGIES MALIGNES<br />
n = 68
F Tumeurs solides : 26 cas<br />
poumon (5), foie (4), prostate (4), sein (3), rein<br />
(3) ...<br />
F Hémopathies : 44 cas<br />
myélodysplasies (14), lymphomes (12), sd<br />
myéloprolifératifs (8), myélomes (6)...<br />
F métastases : 13 %<br />
F syndrome inflammatoire : 72%<br />
F pathologies associées : 34 %
ê<br />
FDans les pathologies malignes, les taux de ferritine (1246 ng/ml +/-<br />
1903) sont significativement plus élevés vs autres étiologies (p < 0,0002)
LES INFECTIONS n = 60
F infection bactérienne dans 97 % des cas<br />
F broncho-pneumopathies (12) infections des voies urinaires (8)<br />
digestives (6), ostéoarthrites (6), endocardites (5)...<br />
F syndrome inflammatoire : 97 % des cas<br />
F fer sérique normal ou diminué : 77 % des cas<br />
F le CS est significativement plus bas vs autres étiologies (p < 0,001)
ê<br />
moyenne des taux de ferritine : 793 ng/ml +/- 1259
LES MALADIES DE SYSTEME<br />
n = 38
n<br />
Maladie de Horton 7<br />
Polyarthrite rhumatoïde 6<br />
Syndrome de Gougerot 5<br />
Périartérite noueuse 4<br />
Dermatopolymyosite 3<br />
Vascularite X 3<br />
Lupus 2<br />
Maladie de Still de l'adulte 2<br />
Sarcoidose 1<br />
Maladie de Crohn 1<br />
Maladie de Whipple 1<br />
Granulomatose systémique 1<br />
Amylose 1<br />
Syndrome de Sharp 1<br />
l syndrome inflammatoire : 58 %<br />
l pathologies associées : 29 %
moyenne des taux de ferritine : 524 ng/ml +/- 266<br />
ê
PATHOLOGIES DIVERSES<br />
n = 38
n<br />
Maladies thrombo-emboliques 10<br />
Syndromes inflammatoires non documentés 7<br />
Hyperferritinémies isolées 4<br />
Arthrites microcristallines 3<br />
Dysglobulinémies monoclonales 2<br />
Insuffisance rénale chronique 2<br />
Péricardite 1<br />
Méningoencéphalite 1<br />
Cholécystite chronique 1<br />
BOOP 1<br />
Hyperthyroïdie 1<br />
Hyperparathyroïdie 1<br />
Ataxie cérébelleuse dégénérative 1<br />
PTAI 1<br />
Dénutrition sévère 1<br />
Acido-cétose 1<br />
l Syndrome<br />
inflammatoire : 71 %<br />
l MTE isolée dans<br />
4 cas / 10
LYSES CELLULAIRES<br />
n = 10
Hémolyses*<br />
IDM<br />
pancréatite aiguë<br />
8 cas<br />
1 cas<br />
1 cas<br />
l Syndrome inflammatoire<br />
: 55,5 %<br />
l<br />
pathologies associées<br />
: 40 %<br />
* auto-immunes 4<br />
anémies constitutive 2<br />
médicamenteuses 1<br />
indéterminée 1
moyenne des taux de ferritine : 623 ng/ml +/- 359<br />
ê
DISCUSSION
Comparaison avec l’étude de Lee Mark<br />
(The Am J of Med, 1995)<br />
Etude rétrospective des hyperferritinémies >1000<br />
% id de pathologies associées (17%)<br />
Tumeurs malignes et foie sont les 2 causes pp de<br />
ferritine élevée<br />
Les hémochromatoses secondaires ont les valeurs les<br />
plus élevées; Lee n ’a pas d ’hémophagocytose<br />
Le VIH est la 3è cause infectieuse chez Lee<br />
Pas de corrélation ferritine, CS et CRP
DISCUSSION (suite)<br />
Óles pathologies associées à une surcharge en fer<br />
" intérêt diagnostique de l’analyse moléculaire du<br />
gène HFE<br />
" l’individualisation récente du syndrome HSD<br />
modifie les critères diagnostiques de surcharge en fer<br />
lien avec la stéatose et la stéatofibrose non alcoolique<br />
(NASH)<br />
surcharge en fer = pour le foie fibrose<br />
et risque vasculaire théorique, carcinogénèse
DISCUSSION (suite)<br />
Ð les pathologies non associées à une surcharge en fer :<br />
$ HF et cancers<br />
Mais dans cette série tous les cancers étaient<br />
symptomatiques<br />
Bilan paranéoplasique peu raisonnable ?<br />
Doit-il être discuté si ferritine >1000? Exhaustif ou limité au<br />
dépistage non invasif?<br />
Notre attitude...
DIAGNOSTIC D ’UNE<br />
HYPERFERRITINEMIE<br />
CAT
HYPERFERRITINEMIE CAT<br />
CS normal ou abaissé < 0.45 CS >0.45<br />
- CRP surcharge en fer<br />
- transaminases secondaire<br />
- paramètres du SD X oui non<br />
alcool,séro VHC VIH<br />
- Ferritines majeures transfusions X gène HFE<br />
- ferroportine 1 haptoglobine<br />
- HF / Cataracte sidéroblastes<br />
- Acéruléoplasminémie<br />
- Bilan paranéoplasique ? + HG<br />
ferritine >1000<br />
ou ALAT aN<br />
ou gros foie<br />
HG non liée<br />
à HFE?<br />
SAIGNEES<br />
PBH
CONCLUSIONS SUR CETTE<br />
ETUDE<br />
les 2 principales limites sont :<br />
" le caractère rétrospectif, patients<br />
hospitalisés<br />
" le % élevé des pathologies associées<br />
intérêt des isoferritines :<br />
isoferritines acides<br />
sous-unités glycosylées<br />
ferritine intra-érythrocytaire
CONCLUSIONS GENERALES<br />
paramètre biologique non spécifique<br />
faible valeur discriminative de l’élévation des taux<br />
interférences majorantes nombreuses<br />
association ferritine et CS élevé surcharge en fer
Le dosage de la ferritine sérique n ’est pas un<br />
examen de première intention<br />
Il doit être orienté par un contexte clinique ….