TABLEAU A-6Études non randomisées auprès d’enfants (suite)AUTEURS,ANNÉE, TYPED’ÉTUDEPOPULATION ÀL’ÉTUDE, DURÉE,TYPE D’INSULINERÉSULTATSCONCLUSIONPompes versus multi-injections (NPH) (études de séries de cas)Hathout etal., 2003Série de casrétrospectiveN = 39 patients âgésde 10 à 20 ansDurée = 12 moisPompe :lisproMulti-injections avantla pompe :NPH et lisproTaux d’HbA1c (avant-après pompe) (valeurmoyenne et intervalle de confiance) :3 mois avant la pompe : 8,38 % (7,94-8,81)3 mois après la pompe : 7,55 % (7,25-7,86)Différence entre les groupes : p < 0,0001À 9 et à 12 mois, la différence avant-après pompen’est pas significativeGlycémie moyenne (valeur moyenne et intervallede confiance) en mg/dL : NS12 mois avant la pompe : 184,4 (159,03-209,77)12 mois après la pompe : 193,40 (178,40-208,40)L’effet bénéfique initial de lapompe sur le taux d’HbA1c n’estpas soutenu dans le temps.Hypoglycémies graves : NDAcidocétoses :Fréquence diminuée chez 2 patients après utilisationde la pompeLiberatore etal., 2004Série de casrétrospectiveN = 73 patients âgésde 2 à 17 ans (jeunesmotivés à essayer lapompe)Durée = de 6 à30 moisTaux d’HbA1c (avant-après pompe à 12 mois) :8,3 ± 1,0 vs 7,5 ± 1,1 % (p < 0,00001)Glycémie moyenne : NDHypoglycémies graves :20 crises/100 patients/anLa pompe a amélioré le tauxd’HbA1c sans augmenter les hypoglycémiesni les acidocétoses.Pompe : lisproAcidocétoses :4,3 crises/100 patients/an23 % des enfants ont eu un problème techniqueavec la pompe nécessitant son retour au fabricantLitton et al.,2002Série de casN = 9 patients âgésde moins de 4 ansayant une maîtriseglycémiqueinadéquateDurée = 12,7 mois (de7 à 19 mois)Pompe : NDTaux d’HbA1c (avant-après) :9,5 ± 0,4 vs 7,9 ± 0,3 % (p < 0,001)Glycémie moyenne : NDHypoglycémies graves :0,52 ± 0,1 vs 0,09 ± 0,02 crise/mois (p < 0,05)Acidocétoses : NS0,06 ± 0,03 visite à l’urgence par mois, tant avantqu’après la pompeLe traitement par pompe peutdiminuer le taux d’HbA1c et lafréquence des hypoglycémieschez des enfants d’âge préscolaireayant une maîtrise glycémiqueinadéquate. Des familles hautementmotivées et superviséespeuvent donner un traitementefficace et sécuritaire à des enfantssélectionnés.Multi-injections avantla pompe : NPH etrégulière ou lispro56
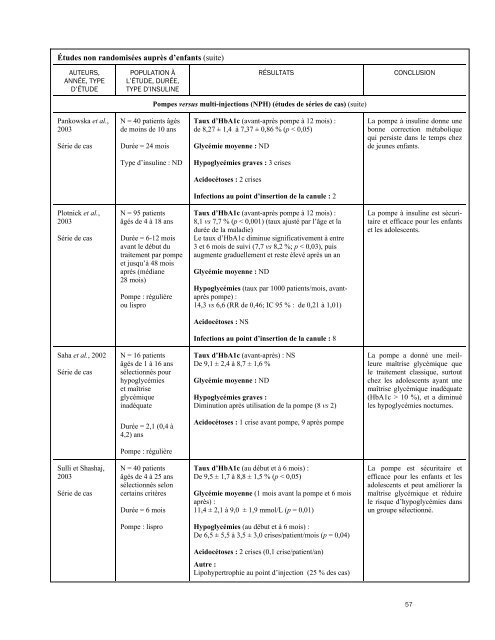
Études non randomisées auprès d’enfants (suite)AUTEURS,ANNÉE, TYPED’ÉTUDEPOPULATION ÀL’ÉTUDE, DURÉE,TYPE D’INSULINERÉSULTATSCONCLUSIONPompes versus multi-injections (NPH) (études de séries de cas) (suite)Pankowska et al.,2003Série de casN = 40 patients âgésde moins de 10 ansDurée = 24 moisTaux d’HbA1c (avant-après pompe à 12 mois) :de 8,27 ± 1,4 à 7,37 ± 0,86 % (p < 0,05)Glycémie moyenne : NDLa pompe à insuline donne unebonne correction métaboliquequi persiste dans le temps chezde jeunes enfants.Type d’insuline : NDHypoglycémies graves : 3 crisesAcidocétoses : 2 crisesInfections au point d’insertion de la canule : 2Plotnick et al.,2003Série de casN = 95 patientsâgés de 4 à 18 ansDurée = 6-12 moisavant le début dutraitement par pompeet jusqu’à 48 moisaprès (médiane28 mois)Pompe : régulièreou lisproTaux d’HbA1c (avant-après pompe à 12 mois) :8,1 vs 7,7 % (p < 0,001) (taux ajusté par l’âge et ladurée de la maladie)Le taux d’HbA1c diminue significativement à entre3 et 6 mois de suivi (7,7 vs 8,2 %; p < 0,03), puisaugmente graduellement et reste élevé après un anGlycémie moyenne : NDHypoglycémies (taux par 1000 patients/mois, avantaprèspompe) :14,3 vs 6,6 (RR de 0,46; IC 95 % : de 0,21 à 1,01)La pompe à insuline est sécuritaireet efficace pour les enfantset les adolescents.Acidocétoses : NSInfections au point d’insertion de la canule : 8Saha et al., 2002Série de casN = 16 patientsâgés de 1 à 16 anssélectionnés pourhypoglycémieset maîtriseglycémiqueinadéquateTaux d’HbA1c (avant-après) : NSDe 9,1 ± 2,4 à 8,7 ± 1,6 %Glycémie moyenne : NDHypoglycémies graves :Diminution après utilisation de la pompe (8 vs 2)La pompe a donné une meilleuremaîtrise glycémique quele traitement classique, surtoutchez les adolescents ayant unemaîtrise glycémique inadéquate(HbA1c > 10 %), et a diminuéles hypoglycémies nocturnes.Durée = 2,1 (0,4 à4,2) ansAcidocétoses : 1 crise avant pompe, 9 après pompePompe : régulièreSulli et Shashaj,2003Série de casN = 40 patientsâgés de 4 à 25 anssélectionnés seloncertains critèresDurée = 6 moisTaux d’HbA1c (au début et à 6 mois) :De 9,5 ± 1,7 à 8,8 ± 1,5 % (p < 0,05)Glycémie moyenne (1 mois avant la pompe et 6 moisaprès) :11,4 ± 2,1 à 9,0 ± 1,9 mmol/L (p = 0,01)La pompe est sécuritaire etefficace pour les enfants et lesadolescents et peut améliorer lamaîtrise glycémique et réduirele risque d’hypoglycémies dansun groupe sélectionné.Pompe : lisproHypoglycémies (au début et à 6 mois) :De 6,5 ± 5,5 à 3,5 ± 3,0 crises/patient/mois (p = 0,04)Acidocétoses : 2 crises (0,1 crise/patient/an)Autre :Lipohypertrophie au point d’injection (25 % des cas)57
- Page 5:
LA MISSIONL'Agence d'évaluation de
- Page 8 and 9:
REMERCIEMENTSCe rapport a été pr
- Page 10 and 11:
proposé à ceux qui sont le plus s
- Page 12 and 13:
RECOMMANDATIONSL’AETMIS recommand
- Page 14 and 15:
6.1.1 Avantages ...................
- Page 16 and 17:
LISTE DES ABRÉVIATIONSAATRMACDADDQ
- Page 18 and 19:
Insuline glargine : nouvelle insuli
- Page 20 and 21:
2 LE DIABÈTE DE TYPE 1Selon les do
- Page 22 and 23:
[EDIC Research Group, 2003]. Les gr
- Page 24 and 25: terme [Buse, 2003; Davidson, 2003].
- Page 26 and 27: 3 LA POMPE À INSULINE3.1 DESCRIPTI
- Page 28 and 29: emboursement de la technologie, au
- Page 30 and 31: 5.2 INNOCUITÉL’innocuité sera e
- Page 32 and 33: Research Group [1995a] sur les effe
- Page 34 and 35: Multi-injections avec l’insuline
- Page 36 and 37: Synthèse (adultes)Les études comp
- Page 38 and 39: correction glycémique identique le
- Page 40 and 41: EnfantsQuatre des cinq essais rando
- Page 42 and 43: 6 LA PERSPECTIVE DES PATIENTSPour c
- Page 44 and 45: formation des patients et au démar
- Page 46 and 47: 7 LA PERSPECTIVE DES PROFESSIONNELS
- Page 48 and 49: que le besoin en enseignement et en
- Page 50 and 51: 8 ASPECTS ÉCONOMIQUES8.1 REVUE DE
- Page 52 and 53: pompes à insuline ne sont rembours
- Page 54 and 55: de ces composantes. Selon ces résu
- Page 56 and 57: TABLEAU 10Déboursés requis tous l
- Page 58 and 59: 9 ANALYSELa revue de la littératur
- Page 60 and 61: pas plus efficaces que les multi-in
- Page 62 and 63: contexte de restrictions budgétair
- Page 64 and 65: 11 RECOMMANDATIONSL’AETMIS recomm
- Page 66 and 67: TABLEAU A-2Essais contrôlés rando
- Page 68 and 69: Études non randomisées auprès d
- Page 70 and 71: TABLEAU A-4Publications rejetées (
- Page 72 and 73: TABLEAU A-5Essais randomisés aupr
- Page 76 and 77: TABLEAU A-6Études non randomisées
- Page 78 and 79: TABLEAU A-7Publications rejetées (
- Page 80 and 81: ANNEXE B : STRATÉGIE DE RECHERCHES
- Page 82 and 83: TABLEAU C-2Exemples de critères de
- Page 84 and 85: ANNEXE D : PERSPECTIVE DES PATIENTS
- Page 86 and 87: 9) Quelle est la deuxième raison p
- Page 88 and 89: 23) Quelle formation à l’utilisa
- Page 90 and 91: TABLEAU D-1Données sociodémograph
- Page 92 and 93: DATE :_______________ MILIEU :_____
- Page 94 and 95: TABLEAU F-1ANNEXE F : ÉTUDES ÉCON
- Page 96 and 97: ANNEXE G : COÛTS DIFFÉRENTIELS DU
- Page 98 and 99: TABLEAU G-3Estimation des coûts mo
- Page 100 and 101: Bringer J, Costalat G, Jaffiol C, R
- Page 102 and 103: DeVries JH, Snoek FJ, Kostense PJ,
- Page 104 and 105: Hirshberg B, Rother KI, Digon BJ, L
- Page 106 and 107: Pankowska E, Lipka M, Wysocka M, Sz
- Page 108: Tamborlane WV, Fredrickson LP, Aher