Slidy lekce 5: Srážecí reakce
Slidy lekce 5: Srážecí reakce
Slidy lekce 5: Srážecí reakce
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
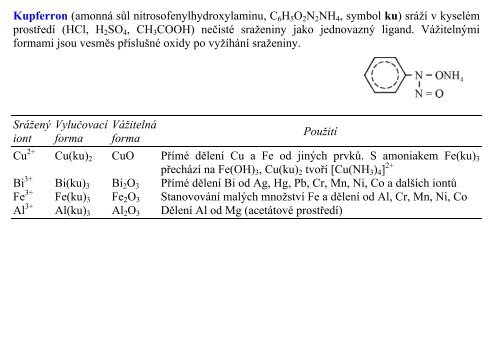
Kupferron (amonná sůl nitrosofenylhydroxylaminu, C6H5O2N2NH4, symbol ku) sráží v kyselém<br />
prostředí (HCl, H2SO4, CH3COOH) nečisté sraženiny jako jednovazný ligand. Vážitelnými<br />
formami jsou vesměs příslušné oxidy po vyžíhání sraženiny.<br />
Srážený<br />
iont<br />
Vylučovací<br />
forma<br />
Vážitelná<br />
forma<br />
Použití<br />
Cu 2+ Cu(ku)2 CuO Přímé dělení Cu a Fe od jiných prvků. S amoniakem Fe(ku)3<br />
přechází na Fe(OH)3, Cu(ku)2 tvoří [Cu(NH3)4] 2+<br />
Bi 3+ Bi(ku)3 Bi2O3 Přímé dělení Bi od Ag, Hg, Pb, Cr, Mn, Ni, Co a dalších iontů<br />
Fe 3+ Fe(ku)3 Fe2O3 Stanovování malých množství Fe a dělení od Al, Cr, Mn, Ni, Co<br />
Al 3+ Al(ku)3 Al2O3 Dělení Al od Mg (acetátové prostředí)