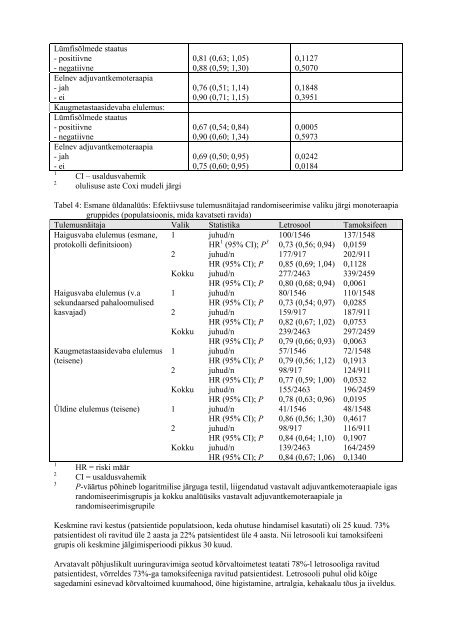
Lümfisõlmede staatus - positiivne - negatiivne Eelnev adjuvantkemoteraapia - jah - ei Kaugmetastaasidevaba elulemus: Lümfisõlmede staatus - positiivne - negatiivne Eelnev adjuvantkemoteraapia - jah - ei 1 CI – usaldusvahemik 2 olulisuse aste Coxi mudeli järgi 0,81 (0,63; 1,05) 0,88 (0,59; 1,30) 0,76 (0,51; 1,14) 0,90 (0,71; 1,15) 0,67 (0,54; 0,84) 0,90 (0,60; 1,34) 0,69 (0,50; 0,95) 0,75 (0,60; 0,95) 0,1127 0,5070 0,1848 0,3951 0,0005 0,5973 0,0242 0,0184 Tabel 4: Esmane üldanalüüs: Efektiivsuse tulemusnäitajad randomis<strong>ee</strong>rimise valiku järgi monoteraapia gruppides (populatsioonis, mida kavatseti ravida) Tulemusnäitaja Valik Statistika Letrosool Tamoksif<strong>ee</strong>n Haigusvaba elulemus (esmane, protokolli definitsioon) Haigusvaba elulemus (v.a sekundaarsed pahaloomulised kasvajad) Kaugmetastaasidevaba elulemus (teisene) Üldine elulemus (teisene) 1 1 2 3 1 2 Kokku 1 2 Kokku 1 2 Kokku 2 Kokku juhud/n HR 1 (95% CI); P 3 juhud/n HR (95% CI); P juhud/n HR (95% CI); P juhud/n HR (95% CI); P juhud/n HR (95% CI); P juhud/n HR (95% CI); P juhud/n HR (95% CI); P juhud/n HR (95% CI); P juhud/n HR (95% CI); P juhud/n HR (95% CI); P juhud/n HR (95% CI); P juhud/n HR (95% CI); P 100/1546 0,73 (0,56; 0,94) 177/917 0,85 (0,69; 1,04) 277/2463 0,80 (0,68; 0,94) 80/1546 0,73 (0,54; 0,97) 159/917 0,82 (0,67; 1,02) 239/2463 0,79 (0,66; 0,93) 57/1546 0,79 (0,56; 1,12) 98/917 0,77 (0,59; 1,00) 155/2463 0,78 (0,63; 0,96) 41/1546 0,86 (0,56; 1,30) 98/917 0,84 (0,64; 1,10) 139/2463 0,84 (0,67; 1,06) 137/1548 0,0159 202/911 0,1128 339/2459 0,0061 110/1548 0,0285 187/911 0,0753 297/2459 0,0063 72/1548 0,1913 124/911 0,0532 196/2459 0,0195 48/1548 0,4617 116/911 0,1907 164/2459 0,1340 HR = riski määr CI = usaldusvahemik P-väärtus põhineb logaritmilise järguga testil, liigendatud vastavalt adjuvantkemoteraapiale igas randomis<strong>ee</strong>rimisgrupis ja kokku analüüsiks vastavalt adjuvantkemoteraapiale ja randomis<strong>ee</strong>rimisgrupile Keskmine ravi kestus (patsientide populatsioon, keda ohutuse hindamisel kasutati) oli 25 kuud. 73% patsientidest oli ravitud üle 2 aasta ja 22% patsientidest üle 4 aasta. Nii letrosooli kui tamoksif<strong>ee</strong>ni grupis oli keskmine jälgimisperioodi pikkus 30 kuud. Arvatavalt põhjuslikult uuringuravimiga seotud kõrvaltoimetest teatati 78%-l letrosooliga ravitud patsientidest, võrreldes 73%-ga tamoksif<strong>ee</strong>niga ravitud patsientidest. Letrosooli puhul olid kõige sagedamini esinevad kõrvaltoimed kuumahood, öine higistamine, artralgia, kehakaalu tõus ja iiveldus.
Nendest ainult artralgiat esines letrosooli rühmas märkimisväärselt sagedamini kui tamoksif<strong>ee</strong>ni rühmas (20% vs 13% tamoksif<strong>ee</strong>niga). Letrosoolravi oli seotud ka suurema osteoporoosi tekkeriskiga (2,2% vs 1,2% tamoksif<strong>ee</strong>niga). Üldiselt oli teatatud kardiovaskulaarsete/tserebrovaskulaarsete nähtude, sõltumata põhjusest, arv mistahes ajahetkel pärast randomis<strong>ee</strong>rimist mõlemas grupis sarnane (10,8% letrosooli grupis ja 12,2% tamoksif<strong>ee</strong>ni grupis). Nende hulgas teatati trombemboolilistest juhtudest letrosooli grupis märkimisväärselt harvem (1,5%) kui tamoksif<strong>ee</strong>ni grupis (3,2%) (P< 0,001), samal ajal kui südamepuudulikkusest teatati letrosooli grupis märkimisväärselt sagedamini (0,9%) kui tamoksif<strong>ee</strong>ni grupis (0,4%) (P=0,006). Normi piires olnud s<strong>ee</strong>rumi üldkolesterooli algtasemega patsientidel täheldati letrosooli grupis 5,4%-l patsientidest üldkolesterooli sisalduse suurenemist enam kui 1,5 korda üle normi ülemise piiri võrreldes 1,1%-ga tamoksif<strong>ee</strong>ni grupis. Pikaajaline adjuvantravi Mitmekeskuselises topeltpimedas randomis<strong>ee</strong>ritud plats<strong>ee</strong>bokontrolliga uuringus osales enam kui 5100 postmenopausis patsienti, kellel oli diagnoositud esmane kas hormoonretseptor-positiivne või teadmata hormoonretseptor-sõltuvusega rinnanäärme kasvaja ning kes 4,5 kuni 6 aasta jooksul saadud tamoksif<strong>ee</strong>ni adjuvantravi järgselt olid progressioonivabad, määrati juhuslikult kas letrosooli- või plats<strong>ee</strong>bogruppi. Esmasel analüüsil pärast keskmiselt 28-kuulist jälgimist (25% patsientidest jälgiti vähemalt 38 kuud) ilmnes, et letrosool vähendas võrreldes plats<strong>ee</strong>boga haiguse taastekke riski 42% võrra (riski määr, 0,58; P=0,00003). Statistiliselt olulist <strong>ee</strong>list haigusvabas elulemuses täheldati letrosooligrupis sõltumata nodaalsest staatusest – nodaalnegatiivne: riski määr 0,48, P=0,002; nodaalpositiivne: riski määr 0,61, P=0,002. Sekundaarse tulemusnäitaja üldise elulemuse (ÜE) seisukohast teatati kokku 113 surmajuhtumist (51 letrosooliga, 62 plats<strong>ee</strong>boga). Üldiselt puudus erinevate ravigruppide vahel märkimisväärne erinevus üldises elulemuses (riski määr 0,82; P=0,29). Hiljem jätkus uuring mitte pimendatult ja plats<strong>ee</strong>bot saanud patsiendid võisid minna üle letrosoolile, kui nad seda soovisid. Pärast seda, kui uuring muutus avatuks, otsustas üle 60% plats<strong>ee</strong>borühma patsientidest, kellel oli õigus letrosoolile üle minna, seda ka teha (st hiljem laiendatud adjuvantrühm). Patsiendid, kes läksid plats<strong>ee</strong>bolt üle letrosoolile, ei olnud adjuvant-tamoksif<strong>ee</strong>ni saanud keskmiselt 31 kuud (vahemikus 14…79 kuud). Kaasajastatud ravisoovi analüüsid teostati keskmiselt 49-kuulisel jälgimisel. Letrosoolirühmas oli vähemalt 30% patsientidest jälgimisel 5 aastat ja 59% vähemalt 4 aastat. Haigusvaba elulemuse kaasajastatud analüüsil vähendas letrosool märkimisväärselt rinnanäärmevähi taastekke riski võrreldes plats<strong>ee</strong>boga (riski määr 0,68; 95% CI 0,55; 0,83; P=0,0001). Letrosool vähendas ka märkimisväärselt võimalust uue invasiivse kontralateraalse vähi tekkeks – võrreldes plats<strong>ee</strong>boga 41% (võimaluse määr: 0,59; 95% CI 0,36; 0,96; P=0,03). Kaugmetastaasidevabas elulemuses või üldises elulemuses ei olnud märkimisväärset erinevust. Luu mineralisatsioonitiheduse (BMD) alamuuringu, mis hõlmasid 226 patsienti kaasajastatud tulemused (keskmine jälgimisperioodi kestus oli 40 kuud) näitasid, et letrosooli saanud patsientidel vähenes 2 aasta jooksul (võrreldes algväärtustega) reieluu proksimaalse osa BMD (keskmine reieluu proksimaalse osa BMD langus 3,8% võrreldes keskmiselt 2,0% langusega plats<strong>ee</strong>bogrupis (P=0,012, kohandatud bisfosfonaatide kasutamisega, P=0,018). Letrosooli saavaid patsiente seostati selgroolülide suurema BMD langusega, kuigi märkimisväärset erinevust ei esinenud. BMD alamuuringus oli kohuslik täiendavalt kasutada kaltsiumi ja D-vitamiini preparaate. Kaasajastatud tulemused Lipid alamuuringust (hõlmas 347 patsienti; keskmine jälgimisperiood oli 50 kuud) ei näidanud letrosooli- ja plats<strong>ee</strong>bogrupi vahel märkimisväärseid erinevusi üldkolesteroolis või mistahes lipiidifraktsioonides. Põhiuuringu kaasajastatud analüüsi andmetel teatas 11,1% letrosooligrupi patsientidest ravi ajal kardiovaskulaarsetest kõrvaltoimetest võrreldes 8,6%-ga plats<strong>ee</strong>bogrupis, kuni ümberlülitumiseni. Nende kõrvaltoimete hulka kuulusid müokardiinfarkt (letrosooliga 1,3%, plats<strong>ee</strong>boga 0,9%);