Chương trình bồi dưỡng HS giỏi Quốc gia (Tỉnh KonTum)
https://app.box.com/s/8pikf51nbzkajtvsccfa5e2vj0sqidxv
https://app.box.com/s/8pikf51nbzkajtvsccfa5e2vj0sqidxv
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
https://twitter.com/daykemquynhon<br />
plus.google.com/+DạyKèmQuyNhơn<br />
www.facebook.com/daykem.quynhon<br />
https://daykemquynhon.blogspot.com<br />
http://daykemquynhon.ucoz.com<br />
Nơi <strong>bồi</strong> <strong>dưỡng</strong> kiến thức Toán - Lý - Hóa cho học sinh cấp 2+3 /<br />
Diễn Đàn Toán - Lý - Hóa Quy Nhơn 1000B Trần Hưng Đạo Tp.Quy Nhơn <strong>Tỉnh</strong> Bình Định<br />
U= ln với C o nồng độ trong bán tế bào 1<br />
⇒ C o = 5,00.10 -3 mol/L<br />
⇒ln = lnC o -<br />
C nồng độ trong bán tế bào 2<br />
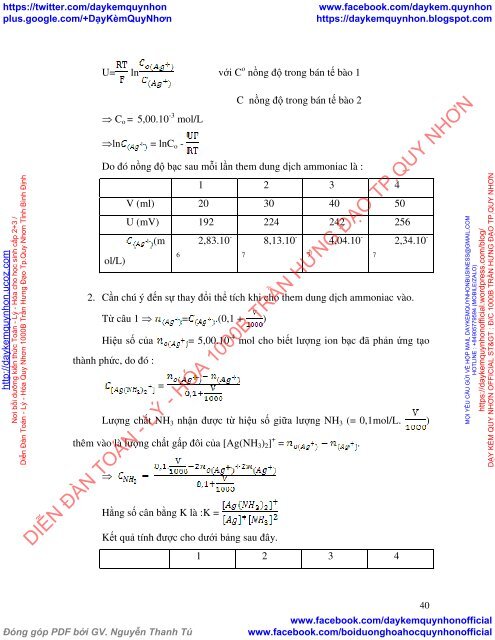
Do đó nồng độ bạc sau mỗi lần them dung dịch ammoniac là :<br />
ol/L)<br />
1 2 3 4<br />
V (ml) 20 30 40 50<br />
U (mV) 192 224 242 256<br />
(m<br />
6<br />
2,83.10 -<br />
7<br />
8,13.10 -<br />
7<br />
4,04.10 -<br />
7<br />
2,34.10 -<br />
2. Cần chú ý đến sự thay đổi thể tích khi cho them dung dịch ammoniac vào.<br />
Từ câu 1 ⇒ = .(0,1 + )<br />
Hiệu số của<br />
thành phức, do đó :<br />
=<br />
= 5,00.10 -4 mol cho biết lượng ion bạc đã phản ứng tạo<br />
Lượng chất NH 3 nhận được từ hiệu số giữa lượng NH 3 (= 0,1mol/L. )<br />
thêm vào là lượng chất gấp đôi của [Ag(NH 3 ) 2 ] + = .<br />
⇒<br />
Hằng số cân bằng K là :K =<br />
Kết quả tính được cho dưới bảng sau đây.<br />
DIỄN ĐÀN TOÁN - LÝ - HÓA 1000B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
1 2 3 4<br />
MỌI YÊU CẦU GỬI VỀ HỘP MAIL DAYKEMQUYNHONBUSINESS@GMAIL.COM<br />
HOTLINE : +84905779594 (MOBILE/ZALO)<br />
https://daykemquynhonofficial.wordpress.com/blog/<br />
DẠY KÈM QUY NHƠN OFFICIAL ST> : Đ/C 1000B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
Đóng góp PDF bởi GV. Nguyễn Thanh Tú<br />
40<br />
www.facebook.com/daykemquynhonofficial<br />
www.facebook.com/boiduonghoahocquynhonofficial