Instrumentelle Analytik Einleitung Seite 1 Einführung 1.1 ...
Instrumentelle Analytik Einleitung Seite 1 Einführung 1.1 ...
Instrumentelle Analytik Einleitung Seite 1 Einführung 1.1 ...
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
<strong>Instrumentelle</strong> <strong>Analytik</strong> <strong>Einleitung</strong> <strong>Seite</strong><br />
1 <strong>Einführung</strong><br />
<strong>1.1</strong> Analytisches System<br />
Instrument.<br />
<strong>Analytik</strong><br />
N020_<strong>Einleitung</strong>_a_BAneu.doc - 1/11<br />
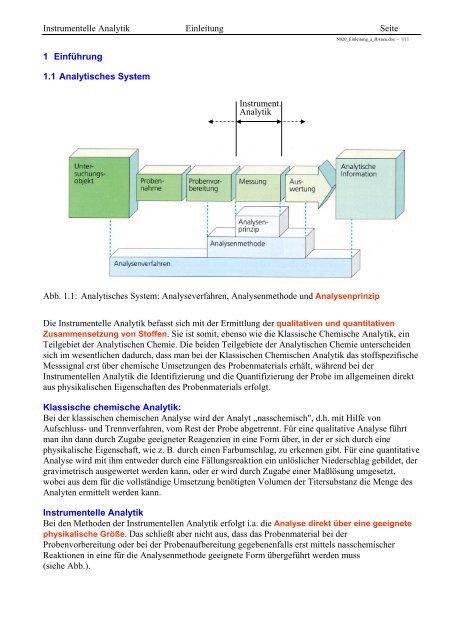
Abb. <strong>1.1</strong>: Analytisches System: Analyseverfahren, Analysenmethode und Analysenprinzip<br />
Die <strong>Instrumentelle</strong> <strong>Analytik</strong> befasst sich mit der Ermittlung der qualitativen und quantitativen<br />
Zusammensetzung von Stoffen. Sie ist somit, ebenso wie die Klassische Chemische <strong>Analytik</strong>, ein<br />
Teilgebiet der Analytischen Chemie. Die beiden Teilgebiete der Analytischen Chemie unterscheiden<br />
sich im wesentlichen dadurch, dass man bei der Klassischen Chemischen <strong>Analytik</strong> das stoffspezifische<br />
Messsignal erst über chemische Umsetzungen des Probenmaterials erhält, während bei der<br />
<strong>Instrumentelle</strong>n <strong>Analytik</strong> die Identifizierung und die Quantifizierung der Probe im allgemeinen direkt<br />
aus physikalischen Eigenschaften des Probenmaterials erfolgt.<br />
Klassische chemische <strong>Analytik</strong>:<br />
Bei der klassischen chemischen Analyse wird der Analyt „nasschemisch", d.h. mit Hilfe von<br />
Aufschluss- und Trennverfahren, vom Rest der Probe abgetrennt. Für eine qualitative Analyse führt<br />
man ihn dann durch Zugabe geeigneter Reagenzien in eine Form über, in der er sich durch eine<br />
physikalische Eigenschaft, wie z. B. durch einen Farbumschlag, zu erkennen gibt. Für eine quantitative<br />
Analyse wird mit ihm entweder durch eine Fällungsreaktion ein unlöslicher Niederschlag gebildet, der<br />
gravimetrisch ausgewertet werden kann, oder er wird durch Zugabe einer Maßlösung umgesetzt,<br />
wobei aus dem für die vollständige Umsetzung benötigten Volumen der Titersubstanz die Menge des<br />
Analyten ermittelt werden kann.<br />
<strong>Instrumentelle</strong> <strong>Analytik</strong><br />
Bei den Methoden der <strong>Instrumentelle</strong>n <strong>Analytik</strong> erfolgt i.a. die Analyse direkt über eine geeignete<br />
physikalische Größe. Das schließt aber nicht aus, dass das Probenmaterial bei der<br />
Probenvorbereitung oder bei der Probenaufbereitung gegebenenfalls erst mittels nasschemischer<br />
Reaktionen in eine für die Analysenmethode geeignete Form übergeführt werden muss<br />
(siehe Abb.).
<strong>Instrumentelle</strong> <strong>Analytik</strong> <strong>Einleitung</strong> <strong>Seite</strong><br />
Abb. 1.2: Gliederung der Analytischen Chemie<br />
Die <strong>Instrumentelle</strong> <strong>Analytik</strong> umfasst alle Verfahren der Analytischen<br />
Chemie, bei denen die qualitative oder die quantitative Bestimmung<br />
der Zusammensetzung einer Probe wesentlich über die Ermittlung<br />
physikalischer Eigenschaften des Probenmaterials erfolgt.<br />
N020_<strong>Einleitung</strong>_a_BAneu.doc - 2/11<br />
<strong>Instrumentelle</strong> <strong>Analytik</strong> ist die Anwendung physikalisch-chemischer Techniken.<br />
Erfolgreiches analytisches Arbeiten erfordert<br />
• für die Handhabung der Analysengeräte fundierte Kenntnisse aus vielen Gebieten der Physik,<br />
wie z. B. aus der Optik, der Atom- und Molekülphysik, der Festkörperphysik,<br />
der Verfahrenstechnik oder der Elektronik und Messtechnik.<br />
• für die Handhabung der Proben und für die Interpretation der Messergebnisse ein gutes<br />
Wissen über Stoffe und Stoffumwandlungen.<br />
<strong>1.1</strong>.1 Überblick der Analysenmethoden in der <strong>Instrumentelle</strong>n <strong>Analytik</strong><br />
Im Prinzip kann jede physikalische Eigenschaft, die für einen Stoff, für ein Element oder für eine<br />
Verbindung charakteristisch ist, als Grundlage für eine Analysenmethode herangezogen werden. Für<br />
die Praxis haben sich folgende Methoden als besonders geeignet erwiesen:<br />
charakteristische Absorption oder Emission elektromagnetischer Strahlung<br />
• Atomabsorptions-Spektrometrie (AAS)<br />
• Atomemissions-Spektrometrie (AES oder OES)<br />
• Röntgenfluoreszenz-Spektrometrie (RFA)<br />
• Infrarot-Spektrometrie<br />
• UV/VIS-Spektrometrie<br />
• Photolumineszenz-Spektrometrie
<strong>Instrumentelle</strong> <strong>Analytik</strong> <strong>Einleitung</strong> <strong>Seite</strong><br />
elastische Streuung elektromagnetischer Strahlung an Molekülen<br />
• Röntgendiffraktometrie<br />
inelastische Streuung elektromagnetischer Strahlung an Molekülen<br />
• Raman-Spektrometrie<br />
gerichtete oder diffuse Reflexion elektromagnetischer Strahlung an Proben<br />
oder an Probenoberflächen<br />
• Reflexionsspektrometrie im infraroten Spektralbereich<br />
• Reflexionsspektrometrie im sichtbaren und ultravioletten Spektralbereich<br />
Wechselwirkungen zwischen Ionen und elektrischen und/oder magnetischen Feldern<br />
• Massenspektrometrie (MS)<br />
• Sekundärionen-Massenspektrometrie (SIMS)<br />
N020_<strong>Einleitung</strong>_a_BAneu.doc - 3/11<br />
charakteristische Vorgänge an oder zwischen Elektroden mit den Messgrößen Potential, Stromstärke,<br />
Ladung, Leitfähigkeit, Dielektrizitätszahl, Kapazität oder Impedanz<br />
• Potentiometrie<br />
• Voltammetrie, Polarographie<br />
• Konduktometrie<br />
• Coulometrie<br />
• Dekametrie<br />
• Flammenionisations-Detektion (FID)<br />
Bindungsenergien von Elektronen<br />
• Augerelektronen-Spektrometrie (AES)<br />
• Elektronenspektrometrie zur chemischen Analyse (ESCA) oder Röntgen-Photoelektronen-<br />
Spektrometrie (XPS)<br />
• UV-Photoelektronen-Spektrometrie (UPS)<br />
Adsorption an einem stationären oder mobilen Trägermaterial<br />
• Papier-Chromatographie<br />
• Dünnschicht-Chromatographie<br />
• Flüssigkeits-Chromatographie<br />
• Gas-Chromatographie<br />
Änderung von thermischen Zustandsgrößen in Abhängigkeit von der Wärmeaufnahme bzw.<br />
Wärmeabgabe<br />
• Thermogravimetrie (TG)<br />
• Differential-Thermoanalyse (DTA)
<strong>Instrumentelle</strong> <strong>Analytik</strong> <strong>Einleitung</strong> <strong>Seite</strong><br />
Brechungsindex<br />
• Refraktometrie<br />
N020_<strong>Einleitung</strong>_a_BAneu.doc - 4/11<br />
Drehung der Schwingungsebene polarisierter elektromagnetischer Strahlung in optisch aktiven<br />
Materialien (optische Rotationsdispersion ORD bzw. Zirkulardichroismus CD)<br />
• Polarimetrie<br />
Emission natürlicher oder künstlich angeregter radioaktiver Strahlung<br />
• Radiometrie<br />
• Neutronenaktivierungs-Analyse<br />
Paramagnetismus der Elektronenhülle bzw. des Atomkerns<br />
• Kernresonanz-Spektrometrie (NMR-Spectrometry)<br />
• Elektronenspinresonanz-Spektrometrie (ESR- bzw. EPR-Spectrometry)<br />
Immer häufiger gelingt es, die speziellen Vorzüge einzelner Analysenmethoden durch Kopplung der<br />
Methoden in einem einzigen Gerät zu vereinigen. So nutzt man z. B. die hohe<br />
Nachweisempfindlichkeit der UV/VIS-Spektrometrie oder der Photolumineszenz-Spektrometrie zur<br />
Detektion der durch chromatographische Systeme aufgetrennten Komponenten eines Stoffgemisches.<br />
Für die Identifizierung der Komponenten eignet sich vorzüglich ein IR-Spektrometer (GC-IR-<br />
Kopplung). Als ein noch empfindlicherer Detektor für die Chromatographie erweist sich das<br />
Massenspektrometer (GC- bzw. LC-MS-Kopplung). Bei massenspektrometrischen Elementanalysen<br />
hat sich für die Atomisierung der Probe und für die Ionisierung der Probenatome der Plasmabrenner<br />
des Plasma-Emissions-Spektrometers (ICP-AES) bestens bewährt (ICP-MS-Kopplung).<br />
<strong>1.1</strong>.2 Kriterien für die Wahl der Analysenmethode<br />
Da sich die Anwendungsbereiche der Analysenmethoden beträchtlich überlappen können und da jede<br />
Analysenmethode ihre besonderen Stärken besitzt, kommt, für ein gegebenes analytisches Problem<br />
der Wahl der Analysenmethode eine besondere Bedeutung zu. Um diese optimal treffen zu können,<br />
sollte man sich die folgenden Fragen beantworten:<br />
• In welcher Form liegt die Probe vor (z. B. als Gas, als Flüssigkeit, als Lösung, als Feststoff,<br />
als Paste, als Pulver)?<br />
• Soll die Probe auf bestimmte Elemente oder auf bestimmte Verbindungen untersucht werden?<br />
• In welchem Konzentrationsbereich des Analyten soll die Probe untersucht werden?<br />
• Ist ihre ungefähre Zusammensetzung bekannt?<br />
• Kann die Probenmatrix das Analysenergebnis beeinflussen (spektrale Interferenzen,<br />
chemische Interferenzen, physikalische Interferenzen)?<br />
• Wie viel Probenmaterial steht zur Verfügung?<br />
• Was für eine Information wird gewünscht?<br />
- Eine qualitative Analyse<br />
- Eine quantitative Analyse<br />
- Die Bestimmung des Gehalts an Beimischungen (Qualitätskontrolle)
<strong>Instrumentelle</strong> <strong>Analytik</strong> <strong>Einleitung</strong> <strong>Seite</strong><br />
N020_<strong>Einleitung</strong>_a_BAneu.doc - 5/11<br />
- Die Untersuchung der Probe auf Abwesenheit bestimmter Stoffe (Reinheitskontrolle)<br />
- Eine Analyse der Oberfläche der Probe<br />
- Eine Lokalanalyse<br />
• Welche Analysengenauigkeit wird gefordert?<br />
• Darf die Probe durch den Messvorgang verändert oder zerstört werden?<br />
• Spielt die Analysendauer eine Rolle (z. B. Prozesskontrolle, Störfall)?<br />
• Sind für die Analyse besondere Arbeitsmittel, Vorrichtungen oder Anschlüsse erforderlich<br />
(z. B. Gase, Kühlwasser, flüssiger Stickstoff oder flüssiges Helium, Abzüge,<br />
Abschirmungen)?<br />
• Handelt es sich um Routineuntersuchungen, um Reihenuntersuchungen oder um<br />
Untersuchungen von Proben mit ständig wechselnden Zusammensetzungen?<br />
• Was steht an Personal zur Verfügung (Qualität und Quantität)?<br />
• Soll mit vorhandenen Geräten gearbeitet werden, oder dürfen neue Geräte angeschafft<br />
werden?<br />
• Was dürfen neue Geräte kosten?<br />
• Was darf die Analyse kosten?<br />
<strong>1.1</strong>.3 Aufbau eines Analysengerätes<br />
Probe (aufbereitet oder direkt)<br />
Abb.: Bauteile eines typisches Analysegerätes<br />
Jedes Analysengerät besteht im Prinzip aus vier Komponenten:<br />
• dem Signalerzeuger<br />
• dem Detektor<br />
• der Signalverarbeitung<br />
• der Signalausgabe<br />
Der Signalerzeuger veranlasst die Probe zur Abgabe eines charakteristischen Signals. Der Detektor<br />
empfängt das Signal und wandelt es in ein leicht weiter zu verarbeitendes, im allgemeinen in ein<br />
elektrisches Signal, um. Die Signalverarbeitung führt eine Analog/Digitalwandlung und Operationen<br />
wie z. B. Gleichrichten, Integrieren, Differenzieren, Subtrahieren oder Vergleichen mit einem<br />
Referenzsignal durch. Die Signalausgabe erfolgt auf einem Monitor oder an einen Speicher.
<strong>Instrumentelle</strong> <strong>Analytik</strong> <strong>Einleitung</strong> <strong>Seite</strong><br />
<strong>1.1</strong>.4 Probennahme, Probenaufbereitung, Probenvorbereitung<br />
Die Herstellung der Proben ist von entscheidender Bedeutung für die Qualität eines<br />
Analyseergebnisses.<br />
Unsachgemäßes Vorgehen oder<br />
mangelnde Sorgfalt bei der<br />
Probennahme, Probenaufbereitung<br />
und Probenvorbereitung<br />
ist in der Praxis die häufigste und<br />
gravierendste Fehlerquelle (Fehler<br />
bis zu 100%).<br />
Abb.:<br />
Fehlerquellen in der <strong>Analytik</strong><br />
Fehler bei der Probennahme, beim Transport, bei der Lagerung und insbe-<br />
sondere bei der Vorbereitung der Proben, können durch eine noch so<br />
aufwendige Kalibrierung und Sorgfalt bei der Durchführung der Messungen<br />
selbst mit den besten Instrumenten nicht mehr behoben werden.<br />
Beispiel: Direkt- / Verbundverfahren<br />
Verbundverfahren<br />
Probe wird in mehreren Schritten hergestellt.<br />
- Probennahme Realprobe<br />
- Homogenisierung Laborprobe<br />
- Lösen, Aufschluss gereinigte Probe<br />
- Abtrennung der Matrix1 reine Substanz<br />
(Beispiel: UV/VIS-Spektrometrie)<br />
Direktverfahren<br />
Probe wird direkt ohne Zwischenschritte<br />
analysiert<br />
(Beispiel: GF-AAS mit Feststoff, AES)<br />
Aus Zeitgründen wird in der Vorlesung auf die Probenherstellung nicht eingegangen.<br />
Sie lernen jedoch im Praktikum einzelne Aufbereitungstechniken kennen.<br />
Zertifizierte <strong>Analytik</strong>labors müssen sich an genaue Vorschriften und Richtlinien bei der<br />
Probennahme halten (Stichworte - Qualitätssicherung, Qualitätsmanagement).<br />
1 Matrix: Stoff oder Stoffsystem in die der Analyt eingebettet ist<br />
N020_<strong>Einleitung</strong>_a_BAneu.doc - 6/11
<strong>Instrumentelle</strong> <strong>Analytik</strong> <strong>Einleitung</strong> <strong>Seite</strong><br />
N020_<strong>Einleitung</strong>_a_BAneu.doc - 7/11<br />
<strong>1.1</strong>.5 Spektroskopische Messverfahren / Methoden der <strong>Instrumentelle</strong>n <strong>Analytik</strong><br />
In der untenstehenden Tabelle sind noch mal die Charakteristika der wichtigsten<br />
spektroskopischen Verfahren zusammengefasst.<br />
Diese Verfahren werden in der Vorlesung behandelt.<br />
Atomabsorptionsspektrometrie<br />
AAS<br />
Atomemissionsspektrometrie<br />
AES<br />
UV/VIS-<br />
Absorptionsspektrometrie<br />
Methode Physikalisches Prinzip Art der Probe<br />
(Präparation)<br />
Elektronenübergänge in<br />
äußeren Schalen<br />
Elektronenübergänge in<br />
äußeren Schalen<br />
Elektronenübergänge in<br />
äußeren Schalen<br />
IR-Spektrometrie Anregung von<br />
Schwingungen<br />
und Rotationen<br />
Fluorimetrie Elektronenübergänge in<br />
äußeren Schalen<br />
Röntgenfluoreszenzanalyse Elektronenübergänge in<br />
inneren Schalen<br />
Massenspektrometrie MS Massenbestimmung aus<br />
Ladung/Masse von Ionen<br />
Kernresonanzspektrometrie<br />
NMR<br />
Richtungsübergänge von<br />
Atomkernen mit permanentem<br />
magnetischen Dipolmoment in<br />
äußeren Magnetfeldern<br />
Wellenlängenbereiche: Röntgen 0,0005 ... 0,005 µm<br />
UV: 0,01 ... 0,4 µm<br />
VIS: 0,4 ... 0,8 µm<br />
IR: 0,8 ... 100 µm<br />
Atome im<br />
Grundzustand<br />
Atome im<br />
angeregten<br />
Zustand<br />
Molekülgase,<br />
Moleküle und Ionen<br />
in Lösungen,<br />
Festkörper<br />
Molekülgase,<br />
organische<br />
Moleküle<br />
Moleküle und Ionen<br />
in Lösungen,<br />
Festkörper<br />
Atome und Ionen in<br />
Flüssigkeiten und<br />
Festkörpern<br />
Atom- und<br />
Molekülionen im<br />
Gaszustand<br />
Moleküle in<br />
Lösungen und<br />
Festkörper<br />
Anwendung<br />
Elementanalyse bis in<br />
den Spurenbereich<br />
Elementanalyse bis in<br />
den Spurenbereich<br />
Qualitative und<br />
quantitative Analyse<br />
von Molekülen und<br />
Ionen<br />
Qualitative Analyse und<br />
Strukturbestimmung von<br />
organischen Stoffen,<br />
Quantitative Analyse von<br />
Molekülgasen<br />
Qualitative und<br />
quantitative Analyse<br />
von Molekülen bis in<br />
den Spurenbereich<br />
Elementanalyse von<br />
Haupt- und<br />
Nebenkomponenten<br />
Qualitative und<br />
quantitative Analyse<br />
von Elementen und<br />
Molekülen<br />
Identifizierung und<br />
Strukturbestimmung<br />
von organischen<br />
Molekülen
<strong>Instrumentelle</strong> <strong>Analytik</strong> <strong>Einleitung</strong> <strong>Seite</strong><br />
Abb.: Schema eines Atomabsorptionsspektrometers AAS<br />
Abb.: Schema eines Flammenemissionsspektrometers<br />
Abb.: Schema eines Gleichlicht-Einstrahl-Filterphotometers<br />
N020_<strong>Einleitung</strong>_a_BAneu.doc - 8/11
<strong>Instrumentelle</strong> <strong>Analytik</strong> <strong>Einleitung</strong> <strong>Seite</strong><br />
Abb.: Schema eines Zweistrahl UV/VIS Spektrometers<br />
N020_<strong>Einleitung</strong>_a_BAneu.doc - 9/11
<strong>Instrumentelle</strong> <strong>Analytik</strong> <strong>Einleitung</strong> <strong>Seite</strong><br />
Abb.: Schema eines Fourier-Transform-IR-Spektrometers<br />
Abb.: Schema eines Spektralfluorimeters<br />
N020_<strong>Einleitung</strong>_a_BAneu.doc - 10/11
<strong>Instrumentelle</strong> <strong>Analytik</strong> <strong>Einleitung</strong> <strong>Seite</strong><br />
Abb.: Schema eines Quadrupol-Massenspektrometers<br />
Abb.: Schema eines Kernresonanzspektrometers<br />
N020_<strong>Einleitung</strong>_a_BAneu.doc - 11/11