Chemie und ihre Didaktik, Universität Wuppertal - Bergische ...
Chemie und ihre Didaktik, Universität Wuppertal - Bergische ...
Chemie und ihre Didaktik, Universität Wuppertal - Bergische ...
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
<strong>Bergische</strong> <strong>Universität</strong> <strong>Wuppertal</strong><br />
Fachbereich C - <strong>Chemie</strong><br />
Prof. Dr. Michael W. Tausch<br />
Klausur in Allgemeine <strong>Chemie</strong> für das 1. Semester, Studiengang GHR-Lehramt<br />
Zugelassene Hilfsmaterialien: Buchners <strong>Chemie</strong>-Begleiter, Taschenrechner<br />
Name........................................................<br />
Matr. Nr....................................................<br />
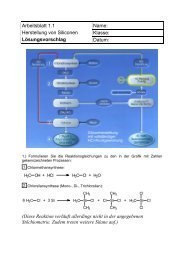
Aufgabe 1 Im folgenden Bild wir die Entstehung von saurem Regen erläutert:<br />
1.1 Bei welchem(n) der folgenden<br />
Vorgänge bilden sich welche der<br />
angegebenen Oxide? Bitte schreiben<br />
Sie jeweils die Formel(n) der Oxide auf:<br />
Bei Heizungsanlagen in Gebäuden:<br />
...............................................................<br />
....<br />
Bei Blitzen in Gewittern:<br />
...............................................................<br />
...<br />
Bei der Verbrennung von Benzin in<br />
Motoren:<br />
..........................................................<br />
........<br />
1.2 Schreiben Sie an die Formeln aus den Reaktionsgleichungen die Oxidationszahlen, die Ihnen<br />
erlauben, festzustellen, ob es sich jeweils um eine Redoxreaktion handelt oder nicht. Bezeichnen Sie<br />
dann die betreffenden Reaktionen im Bild mit dem Wort „Redox“.<br />
1.3 Schreiben Sie für jede der im Bild vorkommenden Säuren die Formel eines Salzes auf <strong>und</strong><br />
benennen Sie das Salz:<br />
1.4 Salzsäure setzt aus Calciumcarbonat CaCO3 Kohlensäure frei, die in Kohlenstoffdioxid <strong>und</strong><br />
Wasser zerfällt. Formulieren Sie die Reaktionsgleichungen <strong>und</strong> geben Sie jeweils an, ob es sich um<br />
a) eine Redoxreaktion, b) eine Protolyse oder c) keine von beiden handelt:
Aufgabe 2<br />
____________<br />
_____________<br />
HBrO3<br />
KBr<br />
NaBrO2<br />
HBrO<br />
HBrO4<br />
Brom<br />
2.1 Tragen Sie unter die Elektronenschalenmodelle in die beiden ersten Kästen die<br />
Namen der betreffenden Elemente ein <strong>und</strong> geben sie <strong>ihre</strong> Plätze (Gruppe, Periode)<br />
im Periodensystem sowie <strong>ihre</strong> Atommassen an.<br />
2.2 Geben Sie im dritten Kasten in der üblichen Schreibweise die Oxidationszahlen<br />
aller Brom-Atome in den angegebenen Verbindungen an.<br />
2.3 Bei den folgenden Aussagen handelt es sich um Trends im Periodensystem der<br />
Elemente. Kreuzen Sie die richtigen Aussagen an.<br />
� Die Elektronegativität nimmt in den Gruppen von oben nach unten ab.<br />
� Die Ionenradien nehmen in den Perioden von links nach rechts zu.<br />
� Die Ionisierungsenergien nehmen in den den Perioden von links nach rechts zu.<br />
� Die Ionisierungsenergien nehmen in den Gruppen von oben nach unten ab.<br />
� Der Metallcharakter nimmt in den Gruppen von oben nach unten ab.
Aufgabe 3<br />
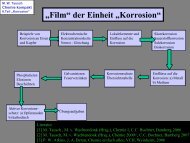
BORN-HABER-Kreisprozess zur NaCl-Synthese<br />
3.1 Berechnen Sie aus den Angaben im<br />
Diagramm die Gitterenergie (Gitterenthalpie)<br />
ΔHG von Natriumchlorid.<br />
ΔHG = ................... kJ/mol.<br />
3.2 Verläuft der Elektronentransfer von<br />
den Natrium- zu den Chloratomen, d.h.<br />
die Bildung von Ionen, exotherm oder<br />
endotherm? Bitte den falschen Begriff<br />
streichen <strong>und</strong> begründen.<br />
exotherm/endotherm, weil ..................<br />
................................................................<br />
................................................................<br />
3.3 Welcher der im BORN-HABER-Kreisprozess beteiligten Teilprozesse ist dafür<br />
verantwortlich, dass die NaCl-Synthese exotherm verläuft? Nennen Sie den<br />
Teilprozess (auf der durchgezogenen Linie) <strong>und</strong> begründen Sie, warum es gerade<br />
dieser ist.<br />
______________________________________ , weil .................................................<br />
........................................................................................................................................<br />
........................................................................................................................................<br />
3.4 Für welche der folgenden Eigenschaften eines Salzes hat der Betrag der<br />
Gitterenergie eine entscheidende Bedeutung? Bitte ankreuzen.<br />
� Schmelztemperatur � Farbe<br />
� Dichte � Wasserlöslichkeit<br />
3.5 Beschriften Sie in der nebenstehenden<br />
Modellzeichnung die Natrium-Ionen mit Na + <strong>und</strong> die<br />
Chlorid-Ionen mit Cl - .<br />
3.6 Nennen Sie anhand dieser Zeichnung die<br />
Koordinationszahlen von Na + <strong>und</strong> von Cl - im<br />
Natriumchlorid-Gitter.<br />
KZ(Na + ) = ..........<br />
KZ(Cl - ) = ...........
Aufgabe 4<br />
4.4 Was geschieht, wenn man die beiden Elektroden in die Lösungen tiefer eintaucht?<br />
Die Spannung der Zelle U: steigt / fällt / bleibt gleich (bitte zwei Begriffe streichen)<br />
Die Stromstärke der Zelle I: steigt / fällt / bleibt gleich (bitte zwei Begriffe streichen)<br />
4.5 Zeichnen Sie in die obige Skizze Pfeile ein, die den Stromfluss in der Zelle <strong>und</strong> außerhalb der<br />
Zelle verdeutlichen. Schreiben Sie auf die Pfeile die Symbole bzw. Formeln der Teilchen, die<br />
elektrische Ladung transportieren.<br />
Aufgabe 5<br />
Definieren Sie mit wenigen Worten folgende Begriffe:<br />
4.1. Beschriften Sie die Galvanische Zelle mit „+“(Pluspol),<br />
„-„ (Minuspol), „D“ (Donator-Halbzelle) <strong>und</strong> „A“(Akzeptor-<br />
Halbzelle).<br />
4.2. Formulieren Sie die Elektrodenprozesse in den beiden<br />
Halbzellen:<br />
A: ................................................................................<br />
D:.................................................................................<br />
4.3. Wie verändert sich die Spannung U, wenn:<br />
Die Zinksulfat-Lösung verdünnt wird? U steigt/fällt<br />
Die Kupfersulfat-Lösung verdünnt wird? U steigt/fällt<br />
Aktivierungsenergie:...........................................................................................................................<br />
.........................................................................................................................................................<br />
Katalysator:......................................................................................................................................<br />
..........................................................................................................................................................<br />
Reaktionsenthalpie:..........................................................................................................................<br />
...........................................................................................................................................................<br />
Anode: ..............................................................................................................................................<br />
...........................................................................................................................................................<br />
Protolyse: .........................................................................................................................................<br />
..........................................................................................................................................................
Aufgabe 6<br />
Produkte Hinreaktion Prinzip von<br />
Le Chatelier<br />
Edukte<br />
Umkehrbare Dynamisches<br />
Reaktion Gleichgewicht<br />
Rückreaktion Druck<br />
Chemisches<br />
Gleichgewicht Konzentration<br />
Massenwirkungs- Freie Reak-<br />
Gesetz tionsenthalpie Temperatur<br />
Gleichgewichts- Reaktions-<br />
Konstante K geschwindigkeit<br />
Katalysator<br />
Begriffsnetz (concept-map) zum Chemischen Gleichgewicht<br />
Wählen Sie aus der folgenden Liste 8 zutreffende Relationen aus <strong>und</strong> tragen Sie<br />
die entsprechende Zahl in die vorgesehenen Kästchen auf den Pfeilen des obigen<br />
Begriffsnetzes ein. Jede Zahl darf nur einmal eingetragen werden.<br />
Die eingetragenen Zahlen symbolisieren folgende Relationen:<br />
1 ist ein(e)<br />
2 ist Teil von<br />
3 ist Voraussetzung für<br />
4 beeinflusst<br />
5 beeinflusst nicht<br />
6 lässt sich berechnen mit<br />
7 macht Aussage über den Einfluss von<br />
8 laufen im GGW mit gleicher Geschwin-<br />
digkeit ab<br />
9 erhöht<br />
10 beschreibt quantitativ<br />
11 führt zur Bildung von<br />
12 im Zähler steht die Konzentration der<br />
13 im Nenner steht die Konzentration der<br />
14 hat den Wert 0 im eingestellten<br />
15 stehen im GGW mit<br />
16 wenn K < 1, liegt GGW auf Seite von<br />
17 wenn K > 1, liegt GGW auf Seite von
Aufgabe 7 (Bei 7.1 bis 7.3 müssen Sie keine Rechnungen <strong>und</strong> Begründungen aufschreiben)<br />
100 ml Natronlauge NaOH(aq)<br />
wurden pH-metrisch mit<br />
Salzsäure, c = 0,25 mol/l titriert.<br />
Die Messwerte sind im nebenstehenden<br />
Diagramm mit pH<br />
als Ordinate dargestellt.<br />
7.1.Zeichnen Sie in das vorgegebene<br />
Koordinatennetz mit<br />
der Stromstärke I als Ordinate<br />
die konduktometrische Titrationskurve<br />
ein, die man bei<br />
dieser Titration erhalten würde.<br />
Bezeichnen Sie diese Kurve<br />
mit A.<br />
7.2 100 ml Bariumhydroxid-<br />
Lösung Ba(OH)2 der gleichen<br />
Konzentration wie die<br />
Natronlauge werden mit<br />
Salzsäure, c = 0,25 mol/l titriert.<br />
Zeichnen Sie die zu erwartende<br />
konduktometrische Titrationskurve<br />
ein <strong>und</strong> bezeichnen<br />
Sie sie mit B.<br />
7.3 Zeichnen Sie die zu erwartende pH-Titrationskurve ein, wenn 80 ml Bariumhydroxid-<br />
Lösung der gleichen Konzentration wie die Natronlauge mit Salzsäure, c = 0,25 mol/l titriert<br />
werden (Kurve C).<br />
7.4 Berechnen Sie die Konzentration der titrierten Natronlauge <strong>und</strong> tragen Sie das Ergebnis<br />
hier ein (Die Reaktionsgleichung <strong>und</strong> die Rechnungen bitte auf die Rückseite oder anderes<br />
Blatt!).<br />
c(NaOH) = ................. mol/l<br />
7.5 Berechnen Sie die Masse des in der Ba(OH)2-Lösung von 7.2 gelösten Bariumhydroxids<br />
<strong>und</strong> tragen Sie das Ergebnis hier ein. (Die Reaktionsgleichung <strong>und</strong> die Rechnungen bitte auf<br />
die Rückseite oder anderes Blatt!).<br />
m(Ba(OH)2) = .................. g<br />
7.6 Berechnen Sie den pH-Wert der Salzsäure, c = 0,25 mol/l, die bei den Titrationen<br />
eingesetzt wurde. Tragen Sie das Ergebnis hier ein.<br />
pH =.....................<br />
7.7 Welchen pH-Wert hat Essigsäure der gleichen Konzentration wie die Salzsäure aus 7.6 ?<br />
(Rechnungen bitte auf die Rückseite oder auf anderes Blatt; Ergebnis hier eintragen!)<br />
Angabe: pKs(H3CCOOH) = + 4,76<br />
pH =.....................