Chemie und ihre Didaktik, Universität Wuppertal - Bergische ...
Chemie und ihre Didaktik, Universität Wuppertal - Bergische ...
Chemie und ihre Didaktik, Universität Wuppertal - Bergische ...
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
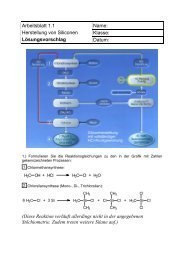
Aufgabe 4<br />
4.4 Was geschieht, wenn man die beiden Elektroden in die Lösungen tiefer eintaucht?<br />
Die Spannung der Zelle U: steigt / fällt / bleibt gleich (bitte zwei Begriffe streichen)<br />
Die Stromstärke der Zelle I: steigt / fällt / bleibt gleich (bitte zwei Begriffe streichen)<br />
4.5 Zeichnen Sie in die obige Skizze Pfeile ein, die den Stromfluss in der Zelle <strong>und</strong> außerhalb der<br />
Zelle verdeutlichen. Schreiben Sie auf die Pfeile die Symbole bzw. Formeln der Teilchen, die<br />
elektrische Ladung transportieren.<br />
Aufgabe 5<br />
Definieren Sie mit wenigen Worten folgende Begriffe:<br />
4.1. Beschriften Sie die Galvanische Zelle mit „+“(Pluspol),<br />
„-„ (Minuspol), „D“ (Donator-Halbzelle) <strong>und</strong> „A“(Akzeptor-<br />
Halbzelle).<br />
4.2. Formulieren Sie die Elektrodenprozesse in den beiden<br />
Halbzellen:<br />
A: ................................................................................<br />
D:.................................................................................<br />
4.3. Wie verändert sich die Spannung U, wenn:<br />
Die Zinksulfat-Lösung verdünnt wird? U steigt/fällt<br />
Die Kupfersulfat-Lösung verdünnt wird? U steigt/fällt<br />
Aktivierungsenergie:...........................................................................................................................<br />
.........................................................................................................................................................<br />
Katalysator:......................................................................................................................................<br />
..........................................................................................................................................................<br />
Reaktionsenthalpie:..........................................................................................................................<br />
...........................................................................................................................................................<br />
Anode: ..............................................................................................................................................<br />
...........................................................................................................................................................<br />
Protolyse: .........................................................................................................................................<br />
..........................................................................................................................................................