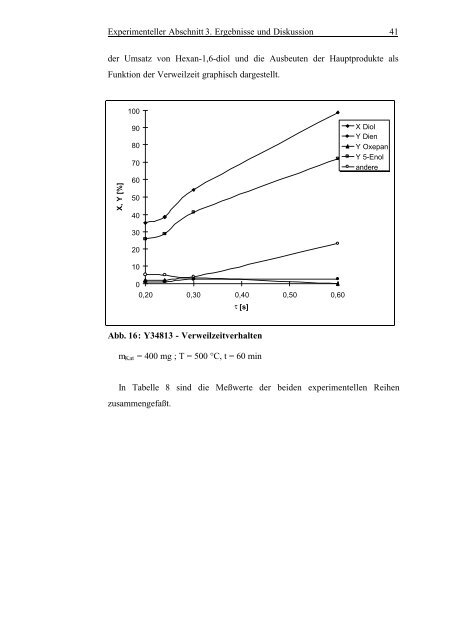
Experimenteller Abschnitt 3. Ergebnisse und Diskussion 41 der Umsatz <strong>von</strong> Hexan-1,6-diol und die Ausbeuten der Hauptprodukte als Funktion der Verweilzeit graphisch dargestellt. 100 90 80 70 X Diol Y Dien Y Oxepan Y 5-Enol andere X, Y [%] 60 50 40 30 20 10 0 0,20 0,30 0,40 0,50 0,60 t [s] Abb. 16: Y34813 - Verweilzeitverhalten m Kat = 400 mg ; T = 500 °C, t = 60 min In Tabelle 8 sind die Meßwerte der beiden experimentellen Reihen zusammengefaßt.
Experimenteller Abschnitt 3. Ergebnisse und Diskussion 42 Tabelle 8: Y34813 - Produktverteilung T[°C] τ[s] X Dien THMP Oxepan 5-Enol 2-Enol andere 400 0,40 3,05 0,00 0,00 0,00 0,63 0,00 2,42 450 0,40 9,26 0,00 0,00 0,63 5,86 0,25 2,52 480 0,40 31,48 1,00 0,00 1,88 23,10 1,03 4,47 485 0,40 35,20 0,68 0,16 1,92 26,50 1,25 4,49 490 0,40 38,60 0,87 0,14 2,03 27,90 1,29 6,12 495 0,40 48,90 1,36 0,00 2,59 36,20 1,71 6,64 497 0,40 77,50 2,03 0,00 3,94 58,70 2,22 10,19 500 0,60 98,75 2,76 0,00 0,00 72,00 0,00 23,35 500 0,40 95,00 2,44 0,81 5,31 63,52 2,72 18,81 500 0,30 54,10 2,49 0,20 3,38 41,18 2,33 4,08 500 0,24 38,48 1,11 0,16 2,20 28,73 1,01 5,05 500 0,20 35,09 0,92 0,18 2,10 25,77 0,81 5,31 520 0,40 97,10 1,25 0,52 2,16 65,80 3,00 23,05 550 0,40 98,00 0,98 0,33 1,61 67,10 3,85 22,72 Formalkinetik: Aus den Umsätzen bei unterschiedlichen Temperaturen und Verweilzeiten ergeben sich die jeweiligen Reaktionsgeschwindigkeiten r A nach Gleichung (1). Für die Reaktion 1. Ordnung gilt das Geschwindigkeitsgesetz in Gleichung (2). Daraus folgt nach Gleichung (3) die Geschwindigkeitskonstante k r als negativer Quotient aus Umsatz und Verweilzeit. Durch Auftragung <strong>von</strong> ln k r als Funktion <strong>von</strong> T -1 im Arrhenius-Diagramm (4) ergeben sich die Aktivierungsenergie E A und der präexponentielle Faktor k 0 . r A X ⋅c = τ A (1) rA = −kr ⋅ cA (2) rA X ⇒ kr = − = − c τ A (3) lnk r E A = lnk0 − (4) RT Die Werte sind in Tabelle 9 dargestellt. Es resultiert die in Abb. 17 graphisch dargestellte Kurve. Durch Linearregression ergibt sich eine Steigung <strong>von</strong> -E A /R = -15223 K und ein Achsenabschnitt <strong>von</strong> ln k 0 = 20,06 und somit eine Aktivierungsenergie <strong>von</strong> E A = 127 kJ mol -1 und ein präexponentieller Faktor <strong>von</strong> k 0 = 514 10 6 s -1 .