Anleitung zum Biochemischen Praktikum für Mediziner Universität zu
Anleitung zum Biochemischen Praktikum für Mediziner Universität zu
Anleitung zum Biochemischen Praktikum für Mediziner Universität zu
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
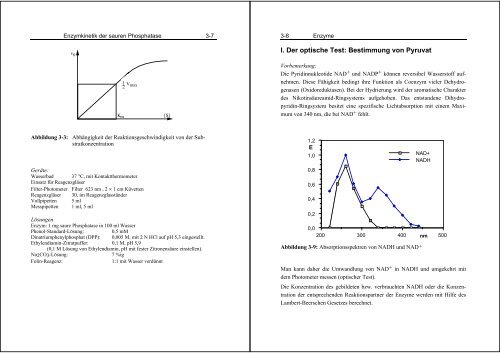
Enzymkinetik der sauren Phosphatase 3-7<br />
v 0<br />
Km<br />
1<br />
2 Vmax<br />
Abbildung 3-3: Abhängigkeit der Reaktionsgeschwindigkeit von der Substratkonzentration<br />
Geräte:<br />
Wasserbad 37 °C, mit Kontaktthermometer<br />
Einsatz <strong>für</strong> Reagenzgläser<br />
Filter-Photometer Filter 623 nm , 2 × 1 cm Küvetten<br />
Reagenzgläser 30, im Reagenzglasständer<br />
Vollpipetten 5 ml<br />
Messpipetten 1 ml, 5 ml<br />
Lösungen<br />
Enzym: 1 mg saure Phosphatase in 100 ml Wasser<br />
Phenol-Standard-Lösung: 0,5 mM<br />
Dinatriumphenylphosphat (DPP): 0,005 M, mit 2 N HCl auf pH 5,3 eingestellt.<br />
Ethylendiamin-Zitratpuffer: 0,1 M, pH 5,9<br />
(0,1 M Lösung von Ethylendiamin, pH mit fester Zitronensäure einstellen).<br />
Na2CO3-Lösung: 7 %ig<br />
Folin-Reagenz: 1:1 mit Wasser verdünnt<br />
[S]<br />
3-8 Enzyme<br />
I. Der optische Test: Bestimmung von Pyruvat<br />
Vorbemerkung:<br />
Die Pyridinnukleotide NAD + und NADP + können reversibel Wasserstoff aufnehmen.<br />
Diese Fähigkeit bedingt ihre Funktion als Coenzym vieler Dehydrogenasen<br />
(Oxidoreduktasen). Bei der Hydrierung wird der aromatische Charakter<br />
des Nikotinsäureamid-Ringsystems aufgehoben. Das entstandene Dihydropyridin-Ringsystem<br />
besitzt eine spezifische Lichtabsorption mit einem Maximum<br />
von 340 nm, die bei NAD + fehlt.<br />
1,2<br />
E<br />
1,0<br />
0,8<br />
0,6<br />
0,4<br />
0,2<br />
0,0<br />
200<br />
300<br />
400<br />
Abbildung 3-9: Absorptionsspektren von NADH und NAD+<br />
NAD+<br />
NADH<br />
Man kann daher die Umwandlung von NAD + in NADH und umgekehrt mit<br />
dem Photometer messen (optischer Test).<br />
Die Konzentration des gebildeten bzw. verbrauchten NADH oder die Konzentration<br />
der entsprechenden Reaktionspartner der Enzyme werden mit Hilfe des<br />
Lambert-Beerschen Gesetzes berechnet.<br />
nm<br />
500