Ärzteblatt August 2010 - Ärztekammer Mecklenburg-Vorpommern
Ärzteblatt August 2010 - Ärztekammer Mecklenburg-Vorpommern
Ärzteblatt August 2010 - Ärztekammer Mecklenburg-Vorpommern
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
WISSeNSCHAFt UND FORSCHUNG<br />
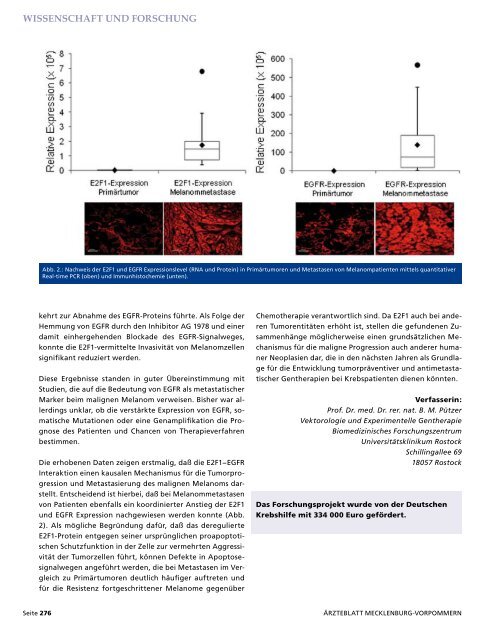
Abb. 2.: Nachweis der E2F1 und EGFR Expressionslevel (RNA und Protein) in Primärtumoren und Metastasen von Melanompatienten mittels quantitativer<br />
Real-time PCR (oben) und Immunhistochemie (unten).<br />
kehrt zur Abnahme des EGFR-Proteins führte. Als Folge der<br />
Hemmung von EGFR durch den Inhibitor AG 1978 und einer<br />
damit einhergehenden Blockade des EGFR-Signalweges,<br />
konnte die E2F1-vermittelte Invasivität von Melanomzellen<br />
signifikant reduziert werden.<br />
Diese Ergebnisse standen in guter Übereinstimmung mit<br />
Studien, die auf die Bedeutung von EGFR als metastatischer<br />
Marker beim malignen Melanom verweisen. Bisher war allerdings<br />
unklar, ob die verstärkte Expression von EGFR, somatische<br />
Mutationen oder eine Genamplifikation die Prognose<br />
des Patienten und Chancen von Therapieverfahren<br />
bestimmen.<br />
Die erhobenen Daten zeigen erstmalig, daß die E2F1−EGFR<br />
Interaktion einen kausalen Mechanismus für die Tumorprogression<br />
und Metastasierung des malignen Melanoms darstellt.<br />
Entscheidend ist hierbei, daß bei Melanommetastasen<br />
von Patienten ebenfalls ein koordinierter Anstieg der E2F1<br />
und EGFR Expression nachgewiesen werden konnte (Abb.<br />
2). Als mögliche Begründung dafür, daß das deregulierte<br />
E2F1-Protein entgegen seiner ursprünglichen proapoptotischen<br />
Schutzfunktion in der Zelle zur vermehrten Aggressivität<br />
der Tumorzellen führt, können Defekte in Apoptosesignalwegen<br />
angeführt werden, die bei Metastasen im Vergleich<br />
zu Primärtumoren deutlich häufiger auftreten und<br />
für die Resistenz fortgeschrittener Melanome gegenüber<br />
Chemotherapie verantwortlich sind. Da E2F1 auch bei anderen<br />
Tumorentitäten erhöht ist, stellen die gefundenen Zusammenhänge<br />
möglicherweise einen grundsätzlichen Mechanismus<br />
für die maligne Progression auch anderer humaner<br />
Neoplasien dar, die in den nächsten Jahren als Grundlage<br />
für die Entwicklung tumorpräventiver und antimetastatischer<br />
Gentherapien bei Krebspatienten dienen könnten.<br />
Verfasserin:<br />
Prof. Dr. med. Dr. rer. nat. B. M. Pützer<br />
Vektorologie und Experimentelle Gentherapie<br />
Biomedizinisches Forschungszentrum<br />
Universitätsklinikum Rostock<br />
Schillingallee 69<br />
18057 Rostock<br />
Das Forschungsprojekt wurde von der Deutschen<br />
Krebshilfe mit 334 000 Euro gefördert.<br />
Seite 276 ÄRZTEBLATT MECKLENBURG-VORPOMMERN