Angewandte Fluororganische Chemie: Synthese ... - Fluorine
Angewandte Fluororganische Chemie: Synthese ... - Fluorine
Angewandte Fluororganische Chemie: Synthese ... - Fluorine
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
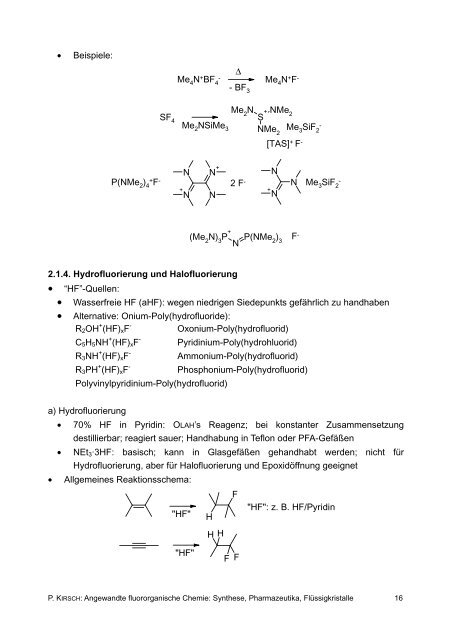
• Beispiele:<br />
P(NMe 2 ) 4 + F -<br />
Me 4 N + BF 4 -<br />
S + NMe Me N 2 2<br />
SF4 Me2NSiMe3 Me3SiF -<br />
2<br />
+<br />
N<br />
N<br />
N N<br />
+<br />
- BF 3<br />
Me 4 N + F -<br />
NMe 2<br />
P. KIRSCH: <strong>Angewandte</strong> fluororganische <strong>Chemie</strong>: <strong>Synthese</strong>, Pharmazeutika, Flüssigkristalle 16<br />
+<br />
Δ<br />
2 F -<br />
N<br />
N<br />
(Me 2 N) 3 P N P(NMe 2 ) 3<br />
[TAS] + F -<br />
+<br />
N<br />
F -<br />
Me 3 SiF 2 -<br />
2.1.4. Hydrofluorierung und Halofluorierung<br />
• “HF”-Quellen:<br />
• Wasserfreie HF (aHF): wegen niedrigen Siedepunkts gefährlich zu handhaben<br />
• Alternative: Onium-Poly(hydrofluoride):<br />
R2OH + (HF)xF - Oxonium-Poly(hydrofluorid)<br />
C5H5NH + (HF)xF - Pyridinium-Poly(hydrohluorid)<br />
R3NH + (HF)xF - Ammonium-Poly(hydrofluorid)<br />
R3PH + (HF)xF - Phosphonium-Poly(hydrofluorid)<br />
Polyvinylpyridinium-Poly(hydrofluorid)<br />
a) Hydrofluorierung<br />
• 70% HF in Pyridin: OLAH’s Reagenz; bei konstanter Zusammensetzung<br />
destillierbar; reagiert sauer; Handhabung in Teflon oder PFA-Gefäßen<br />
• NEt3·3HF: basisch; kann in Glasgefäßen gehandhabt werden; nicht für<br />
Hydrofluorierung, aber für Halofluorierung und Epoxidöffnung geeignet<br />
• Allgemeines Reaktionsschema:<br />
"HF"<br />
"HF"<br />
H<br />
H H<br />
F<br />
F<br />
F<br />
"HF": z. B. HF/Pyridin