COMBO ĐỀ HSG MÔN TOÁN, VẬT LÝ, HÓA HỌC LỚP 8 CẤP HUYỆN NHỮNG NĂM GẦN ĐÂY (CÓ ĐÁP ÁN CHI TIẾT)
https://app.box.com/s/8zu9uan6fp6a5appv6hbmr8iy6wzshdo
https://app.box.com/s/8zu9uan6fp6a5appv6hbmr8iy6wzshdo
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
https://twitter.com/daykemquynhon<br />
plus.google.com/+DạyKèmQuyNhơn<br />
www.facebook.com/daykem.quynhon<br />
https://daykemquynhon.blogspot.com<br />
http://daykemquynhon.ucoz.com<br />
Nơi bồi dưỡng kiến thức Toán - Lý - Hóa cho học sinh cấp 2+3 /<br />
Diễn Đàn Toán - Lý - Hóa Quy Nhơn 1000B Trần Hưng Đạo Tp.Quy Nhơn Tỉnh Bình Định<br />
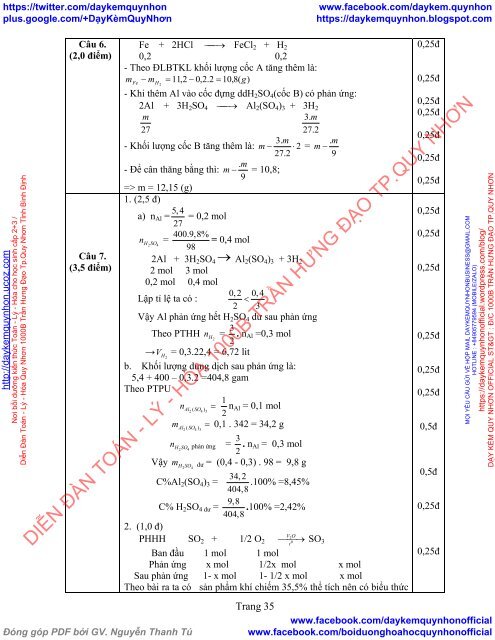
Câu 6.<br />
(2,0 điểm)<br />
Câu 7.<br />
(3,5 điểm)<br />
Fe + 2HCl FeCl 2 + H 2<br />
0,2 0,2<br />
- Theo ĐLBTKL khối lượng cốc A tăng thêm là:<br />
mFe<br />
mH<br />
11,2 0,2.2 10,8( g)<br />
2<br />
- Khi thêm Al vào cốc đựng ddH 2 SO 4 (cốc B) có phản ứng:<br />
2Al + 3H 2 SO 4 Al 2 (SO 4 ) 3 + 3H 2<br />
m<br />
3.<br />
m<br />
27<br />
27.2<br />
3. m .m<br />
- Khối lượng cốc B tăng thêm là: m 2 = m <br />
27.2 9<br />
.m<br />
- Để cân thăng bằng thì: m = 10,8;<br />
9<br />
=> m = 12,15 (g)<br />
1. (2,5 đ)<br />
a) n Al = 5,4 = 0,2 mol<br />
27<br />
n<br />
H2SO<br />
= 400.9,8% = 0,4 mol<br />
4<br />
98<br />
2Al + 3H 2 SO 4<br />
Al 2 (SO 4 ) 3 + 3H 2<br />
2 mol 3 mol<br />
0,2 mol 0,4 mol<br />
Lập tỉ lệ ta có :<br />
0,2 0,4<br />
<br />
2 3<br />
Vậy Al phản ứng hết H 2 SO 4 dư sau phản ứng<br />
Theo PTHH n<br />
H<br />
= 3<br />
2<br />
2 . n Al =0,3 mol<br />
→V H 2<br />
= 0,3.22,4 = 6,72 lit<br />
b. Khối lượng dung dịch sau phản ứng là:<br />
5,4 + 400 – 0,3.2 =404,8 gam<br />
Theo PTPU<br />
n 1 2 n Al = 0,1 mol<br />
m<br />
Al2 ( SO4 ) 3<br />
Al2 ( SO4 ) 3<br />
H2SO4<br />
0,1 . 342 = 34,2 g<br />
n phản ứng = 3 2 . n Al = 0,3 mol<br />
Vậy m<br />
H2SO<br />
dư = (0,4 - 0,3) . 98 = 9,8 g<br />
4<br />
C%Al 2 (SO 4 ) 3 =<br />
34,2<br />
.100% =8,45%<br />
404,8<br />
9,8<br />
C% H 2 SO 4 dư = .100% =2,42%<br />
404,8<br />
2. (1,0 đ)<br />
PHHH SO 2 + 1/2 O 2<br />
V O<br />
<br />
20 SO<br />
t 3<br />
Ban đầu 1 mol 1 mol<br />
Phản ứng x mol 1/2x mol x mol<br />
Sau phản ứng 1- x mol 1- 1/2 x mol x mol<br />
Theo bài ra ta có sản phẩm khí chiếm 35,5% thể tích nên có biểu thức<br />
0,25đ<br />
0,25đ<br />
0,25đ<br />
0,25đ<br />
0,25đ<br />
0,25đ<br />
0,25đ<br />
0,25đ<br />
0,25đ<br />
0,25đ<br />
0,25đ<br />
0,25đ<br />
0,25đ<br />
0,5đ<br />
0,5đ<br />
0,25đ<br />
DIỄN ĐÀN <strong>TO<strong>ÁN</strong></strong> - <strong>LÝ</strong> - <strong>HÓA</strong> 1000B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
Đóng góp PDF bởi GV. Nguyễn Thanh Tú<br />
0,25đ<br />
MỌI YÊU CẦU GỬI VỀ HỘP MAIL DAYKEMQUYNHONBUSINESS@GMAIL.COM<br />
HOTLINE : +84905779594 (MOBILE/ZALO)<br />
https://daykemquynhonofficial.wordpress.com/blog/<br />
DẠY KÈM QUY NHƠN OFFICIAL ST> : Đ/C 1000B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
Trang 35<br />
www.facebook.com/daykemquynhonofficial<br />
www.facebook.com/boiduonghoahocquynhonofficial