Descargar PDF (2545 KB) - Enresa
Descargar PDF (2545 KB) - Enresa
Descargar PDF (2545 KB) - Enresa
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
tencial de manera cíclica a una frecuencia relativamente<br />
alta de manera que se produzca una respuesta<br />
sinusoidal de la corriente, que es la variable<br />
que se registra. De esta manera se obtienen curvas<br />
intensidad de corriente – potencial que permiten estudiar<br />
los distintos sistemas electroquímicos.<br />
Debido a las propiedades altamente reductoras del<br />
neodimio, la investigación de la reducción del<br />
Nd(III) depende del intervalo de potencial en el que<br />
el medio salino permite investigar dicho proceso.<br />
Los estudios termodinámicos previos indicaron que<br />
en medios salinos como LiF o LiF-CaF2 era posible<br />
observar la reducción del Nd(III).<br />
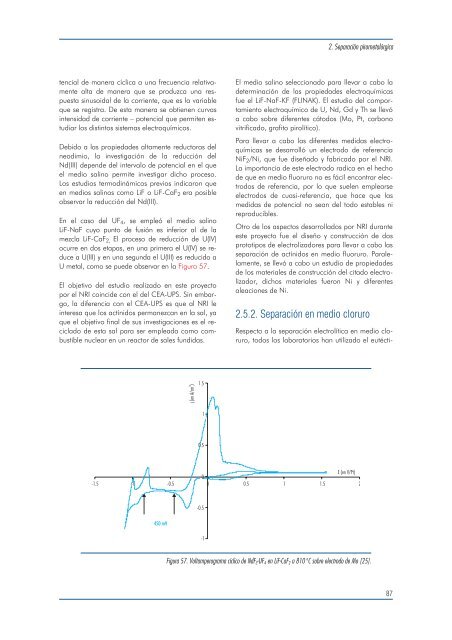
En el caso del UF4, se empleó el medio salino<br />
LiF-NaF cuyo punto de fusión es inferior al de la<br />
mezcla LiF-CaF2, El proceso de reducción de U(IV)<br />
ocurre en dos etapas, en una primera el U(IV) se reduce<br />
a U(III) y en una segunda el U(III) es reducido a<br />
U metal, como se puede observar en la Figura 57.<br />
El objetivo del estudio realizado en este proyecto<br />
por el NRI coincide con el del CEA-UPS. Sin embargo,<br />
la diferencia con el CEA-UPS es que al NRI le<br />
interesa que los actínidos permanezcan en la sal, ya<br />
que el objetivo final de sus investigaciones es el reciclado<br />
de esta sal para ser empleada como combustible<br />
nuclear en un reactor de sales fundidas.<br />
1.5<br />
1<br />
0.5<br />
-0.5<br />
-1<br />
2. Separación pirometalúrgica<br />
El medio salino seleccionado para llevar a cabo la<br />
determinación de las propiedades electroquímicas<br />
fue el LiF-NaF-KF (FLINAK). El estudio del comportamiento<br />
electroquímico de U, Nd, Gd y Th se llevó<br />
a cabo sobre diferentes cátodos (Mo, Pt, carbono<br />
vitrificado, grafito pirolítico).<br />
Para llevar a cabo las diferentes medidas electroquímicas<br />
se desarrolló un electrodo de referencia<br />
NiF2/Ni, que fue diseñado y fabricado por el NRI.<br />
La importancia de este electrodo radica en el hecho<br />
de que en medio fluoruro no es fácil encontrar electrodos<br />
de referencia, por lo que suelen emplearse<br />
electrodos de cuasi-referencia, que hace que las<br />
medidas de potencial no sean del todo estables ni<br />
reproducibles.<br />
Otro de los aspectos desarrollados por NRI durante<br />
este proyecto fue el diseño y construcción de dos<br />
prototipos de electrolizadores para llevar a cabo las<br />
separación de actínidos en medio fluoruro. Paralelamente,<br />
se llevó a cabo un estudio de propiedades<br />
de los materiales de construcción del citado electrolizador,<br />
dichos materiales fueron Ni y diferentes<br />
aleaciones de Ni.<br />
2.5.2. Separación en medio cloruro<br />
Respecto a la separación electrolítica en medio cloruro,<br />
todos los laboratorios han utilizado el eutécti-<br />
0<br />
E (en V/Pt)<br />
-1.5 -1<br />
-0.5<br />
0<br />
0.5<br />
1<br />
1.5<br />
2<br />
450 mV<br />
j (en A/cm )<br />
3<br />
Figura 57. Voltamperograma cíclico de NdF 3-UF 4 en LiF-CaF 2 a 810 o C sobre electrodo de Mo [25].<br />
87