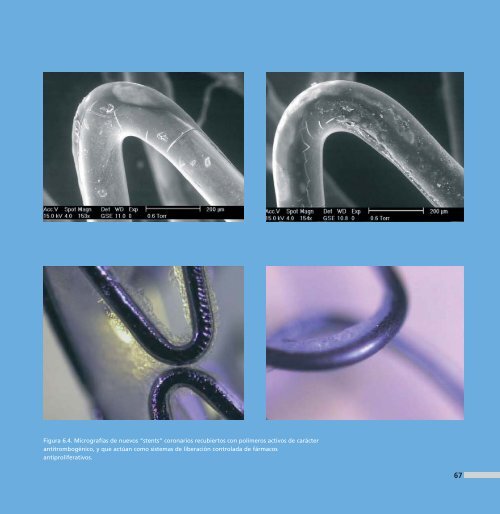
Figura 6.4. Micrografías de nuevos “st<strong>en</strong>ts” coronarios recubiertos con polímeros activos de carácter antitrombogénico, y que actúan como sistemas de liberación controlada de fármacos antiproliferativos. 67
proporcion<strong>en</strong> una interfaz congru<strong>en</strong>te con el tejido óseo circundante. Una v<strong>en</strong>taja importante de la incorporación de elem<strong>en</strong>tos bioactivos <strong>en</strong> la superficie de las prótesis ortopédicas es que permite y estimula la formación de <strong>en</strong>laces <strong>en</strong>tre el compon<strong>en</strong>te bioactivo y las fibrillas de colág<strong>en</strong>o del compon<strong>en</strong>te óseo circundante, que llegan a t<strong>en</strong>er una resist<strong>en</strong>cia incluso superior a la normalm<strong>en</strong>te establecida <strong>en</strong>tre las fibrillas de colág<strong>en</strong>o del hueso, probablem<strong>en</strong>te como consecu<strong>en</strong>cia de la formación de una capa d<strong>en</strong>sa nanométrica de aglomerados cristalinos de hidroxi-carbonato apatita, que se un<strong>en</strong> a las fibrillas de colág<strong>en</strong>o, como así ha señalado Larry H<strong>en</strong>ch reci<strong>en</strong>tem<strong>en</strong>te. La aportación de c<strong>en</strong>tros del CSIC <strong>en</strong> el desarrollo de sistemas cerámicos y biovidrios a base de derivados de calcio como wollastonita, así como de eutecticos wollastonita-fosfato tricálcico, y de materiales compuestos con sistemas poliméricos reabsorbibles, constituye un tema de actualidad y trasc<strong>en</strong>d<strong>en</strong>cia <strong>en</strong> el desarrollo de nuevos biomateriales que tratan de mimetizar a los compon<strong>en</strong>tes de bu<strong>en</strong>a parte de nuestro sistema esquelético. Uno de los aspectos más interesantes del desarrollo de nuevos biomateriales relacionado con la gran versatilidad que aportan los sistemas 68 poliméricos es la posibilidad de aplicar recubrimi<strong>en</strong>tos activos, con propiedades mecánicas adecuadas y posibilidades de que actú<strong>en</strong> como sistemas farmacológicam<strong>en</strong>te activos, y como sistemas de liberación controlada de fármacos específicos. En este s<strong>en</strong>tido, el CSIC está trabajando activam<strong>en</strong>te <strong>en</strong> colaboración con empresas españolas <strong>en</strong> el desarrollo de nuevos “st<strong>en</strong>ts” coronarios recubiertos con polímeros activos, y que actúan como sistemas de liberación controlada de ag<strong>en</strong>tes antiproliferativos celulares. En la figura 6.4. se muestran unas fotografías obt<strong>en</strong>idas por microscopía óptica y electrónica de sistemas que se están estudiando y que se <strong>en</strong>cu<strong>en</strong>tran <strong>en</strong> fase muy avanzada de desarrollo con bu<strong>en</strong>as posibilidades de su comercialización <strong>en</strong> un breve periodo de tiempo. Reg<strong>en</strong>eración de tejidos e “Ing<strong>en</strong>iería Tisular” Los avances producidos <strong>en</strong> los últimos años sobre el control de los procesos de división y crecimi<strong>en</strong>to celular utilizando líneas muy variadas que van desde células madre hasta las más difer<strong>en</strong>ciadas, fibroblastos, condrocitos, osteoblastos, <strong>en</strong>doteliales, etc., ha estimulado el desarrollo de un atractivo y nuevo campo de actividad que constituye el reto de futuro desarrollo de aplicaciones <strong>en</strong> los procesos de reg<strong>en</strong>eración de tejidos y órganos, como se indica esquemáticam<strong>en</strong>te <strong>en</strong> la figura 6.1. La nueva disciplina, conocida como Ing<strong>en</strong>iería de Tejidos ti<strong>en</strong>e como objeto aprovechar los conocimi<strong>en</strong>tos de la Bioing<strong>en</strong>iería, la Biología, la Ci<strong>en</strong>cia de los Biomateriales, para conseguir controlar procesos de reg<strong>en</strong>eración de tejidos <strong>en</strong> medios de cultivo apropiados, a partir de una pequeña biopsia de un paci<strong>en</strong>te, para después conseguir sufici<strong>en</strong>te cantidad de tejido <strong>en</strong> un tiempo razonable, que pueda ser implantado <strong>en</strong> el organismo defectuoso. Las perspectivas de esta nueva actividad son <strong>en</strong>ormes tanto desde un punto de vista básico, académico, como desde el punto de vista socioeconómico, y a ella se está dedicando gran esfuerzo desde las instituciones más repres<strong>en</strong>tativas. Su desarrollo está basado <strong>en</strong> dos conceptos difer<strong>en</strong>tes pero complem<strong>en</strong>tarios: el primero de ellos considera el proceso de reg<strong>en</strong>eración de tejidos a partir de cultivos celulares específicos “in vitro”, utilizando un soporte (normalm<strong>en</strong>te un sistema polimérico poroso y biodegradable) y su posterior implantación <strong>en</strong> el organismo; el segundo está basado <strong>en</strong> la aplicación de un sistema soporte que conti<strong>en</strong>e los