3. Adición del conjugadoPipetear 100µL de conjugado a cada pocillo, secar la parte de arriba de los pocillos con un pañuelo de papel paraeliminar salpicaduras. Nota: Para evitar contaminación, nunca devolver el exceso de conjugado a la botella.Incubar 30 minutos a temperatura ambiente.4. LavadoRepetir punto 2.5. Adición del substrato (TMB)Pipetear 100µL de substrato TMB en cada pocillo, secar la parte de arriba de los pocillos con un pañuelo de papelpara eliminar salpicaduras. Nota: Para evitar contaminación, nunca devolver el exceso de TMB a la botella. Incubar30 minutos a oscuras y a temperatura ambiente.6. ParadaPipetear 100µL de la solución de parada en cada pocillo. Esto dará un cambio de color de azul a amarillo.7. Medición de la densidad ópticaLeer la densidad óptica (OD) de cada pocillo a 450nm en un lector de micro placas en los siguientes 30 minutos ala reacción.Control de Calidad1. Control de calidadPara que el ensayo se dé como válido, deben cumplirse los siguientes criterios:• Deben incluirse controles cut-off y positivo en cada serie.• La DO del cut-off y el resultado <strong>ENA</strong> de los controles positivos deben estar en los rangosespcificados en el Certificado QC.Si los criterios anteriores no se cumplen el resultado no es válido y deberárepetirse el ensayo.2. Cálculo del resultado de muestra y control positivoUtilizar la siguiente fórmula para calcular el resultado <strong>ENA</strong> para cada muestra:DO de lamuestra ocontrol positivo x 10 =DO del controlcut-offValor control o muestra(U/mL)Las muestras que dan resultados en el rango ‘Dudoso’ deberan ser confirmados en el ELISA <strong>ENA</strong> específicopertinente.3. Calibración del ensayoEl ensayo se calibra contra una referencia arbitraria. Los resultados <strong>ENA</strong> son semicuantitativos y vienen dados por lafórmula anterior.4. Interpretación de valores de Sm y RNPSi una muestra es negativa para anticuerpos Sm pero positiva en el ELISA RNP, entonces la reactividad es debida ala presencia de anticuerpos anti-RNP aislados.Si el valor del ELISA Sm es positivo y equivalente al valor del ELISARNP, entonces la actividad es debida principalmente a la presencia de anticuerpos anti-Sm. Una muestra Sm positivapero que da un valor de menos que 80% del valor de RNP deberá reportarse como positiva para ambos anticuerposSm y RNP. Es difícil estimar la actividad específica RNP de muestras dando densidades ópticas superiores a las quepueden medirse con el lector ELISA. Diluir la muestra 1:200 o 1:400 permitirá discernir si la actividad de RNP esmayor que la de Sm.Limitaciones del Procedimiento• Estos kits se emplean solo como soporte al diagnóstico. Un resultado positivo sugiere cierta patología que debe confirmarsepor otras certezas clínicas y otros tests serológicos.• Los resultados obtenidos mediante este ensayo no son una prueba diagnóstica de presencia o ausencia de enfermedad.Valores EsperadosEl rango de normalidad se determinó en sueros de 120 donantes de sangre normales. El control de cut-off se ha definido comoun punto equivalente al límite normal superior resultante de 3 diferentes muestras que se encontraron positivas para SSB, RNPy Scl-70. Los resultados para todas las 120 muestras se confirmaron utilizando los respectivos kits <strong>EIA</strong> BINDAZYME deespecifidad individual. Se indican los rangos sólo como orientación. Los análisis Elisa son muy sensibles y capaces de detectarpequeñas diferencias en poblaciones de muestra. Se recomienda que cada laboratorio determine su propio rango denormalidad, basado en la población y las tecnicas y equipo empleados.Resultado <strong>ENA</strong> Interpretación12,0 PositivoCaracterísticas de funcionamientoPrecisiónLa precisión intra-ensayo se midió por la suma de 12 replicas de un valor medio de muestra para cada especificidad a través dela columna adecuada de una única placa.PRECISIÓN INTRA-ENSAYOEspecificidad Valor medio (densidad óptica) % C.V.SSA 3,10 1,8SSB 1,31 5,9Sm 2,41 3,8Sm/RNP 2,16 3,0Scl-70 2,19 2,9Jo-1 1,44 2,6La precisión inter-ensayo se midió añadiendo una muestra negativa, positiva baja y positiva elevada para cada especificidad en4
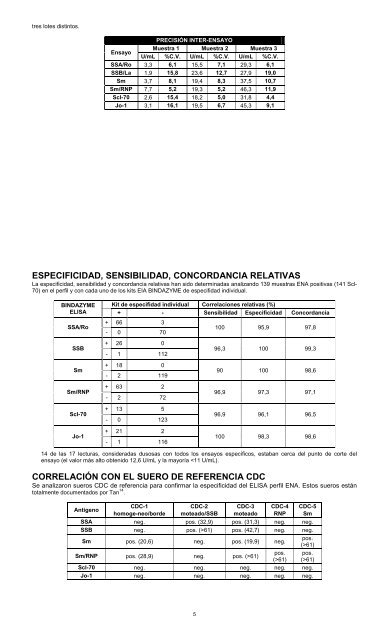
tres lotes distintos.PRECISIÓN INTER-ENSAYOEnsayoMuestra 1 Muestra 2 Muestra 3U/mL %C.V. U/mL %C.V. U/mL %C.V.SSA/Ro 3,3 6,1 15,5 7,1 29,3 6,1SSB/La 1,9 15,8 23,6 12,7 27,9 19,0Sm 3,7 8,1 19,4 8,3 37,5 10,7Sm/RNP 7,7 5,2 19,3 5,2 46,3 11,9Scl-70 2,6 15,4 18,2 5,0 31,8 4,4Jo-1 3,1 16,1 19,5 6,7 45,3 9,1ESPECIFICIDAD, SENSIBILIDAD, CONCORDANCIA RELATIVASLa especificidad, sensibilidad y concordancia relativas han sido determinadas analizando 139 muestras <strong>ENA</strong> positivas (141 Scl-70) en el perfil y con cada uno de los kits <strong>EIA</strong> BINDAZYME de especifidad individual.BINDAZYMEELISASSA/RoSSBKit de especifidad individual Correlaciones relativas (%)+ - Sensibilidad Especificidad Concordancia+ 66 3100 95,9 97,8- 0 70+ 26 0- 1 11296,3 100 99,3SmSm/RNPScl-70Jo-1+ 18 0- 2 119+ 63 2- 2 72+ 13 5- 0 123+ 21 2- 1 11690 100 98,696,9 97,3 97,196,9 96,1 96,5100 98,3 98,614 de las 17 lecturas, consideradas dusosas con todos los ensayos específicos, estaban cerca del punto de corte delensayo (el valor más alto obtenido 12,6 U/mL y la mayoría 61) pos. (42,7) neg. neg.Sm pos. (20,6) neg. pos. (19,9) neg.pos.(>61)Sm/RNP pos. (28,9) neg. pos. (>61)pos. pos.(>61) (>61)Scl-70 neg. neg. neg. neg. neg.Jo-1 neg. neg. neg. neg. neg.5