Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Materias primas<br />
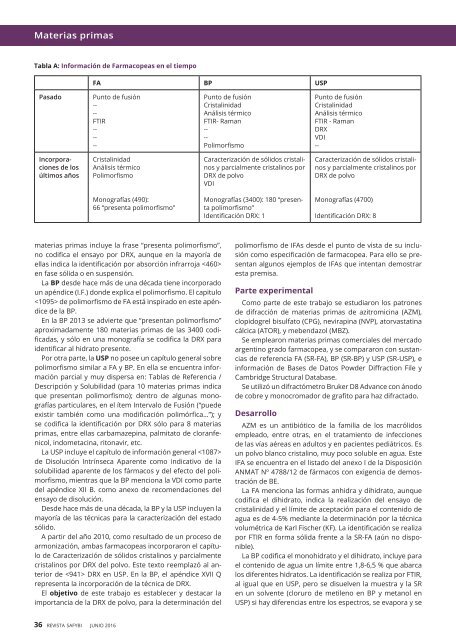
Tabla A: Información de Farmacopeas en el tiempo<br />
FA BP USP<br />
Pasado<br />
Punto de fusión<br />
--<br />
--<br />
FTIR<br />
--<br />
--<br />
--<br />
Punto de fusión<br />
Cristalinidad<br />
Análisis térmico<br />
FTIR- Raman<br />
--<br />
--<br />
Polimorfismo<br />
Punto de fusión<br />
Cristalinidad<br />
Análisis térmico<br />
FTIR - Raman<br />
DRX<br />
VDI<br />
--<br />
Incorporaciones<br />
de los<br />
últimos años<br />
Cristalinidad<br />
Análisis térmico<br />
Polimorfismo<br />
Caracterización de sólidos cristalinos<br />
y parcialmente cristalinos por<br />
DRX de polvo<br />
VDI<br />
Caracterización de sólidos cristalinos<br />
y parcialmente cristalinos por<br />
DRX de polvo<br />
Monografías (490):<br />
66 “presenta polimorfismo”<br />
Monografías (3400): 180 “presenta<br />
polimorfismo”<br />
Identificación DRX: 1<br />
Monografías (4700)<br />
Identificación DRX: 8<br />
materias primas incluye la frase “presenta polimorfismo”,<br />
no codifica el ensayo por DRX, aunque en la mayoría de<br />
ellas indica la identificación por absorción infrarroja <br />
en fase sólida o en suspensión.<br />
La BP desde hace más de una década tiene incorporado<br />
un apéndice (I.F.) donde explica el polimorfismo. El capitulo<br />
de polimorfismo de FA está inspirado en este apéndice<br />
de la BP.<br />
En la BP 2013 se advierte que “presentan polimorfismo”<br />
aproximadamente 180 materias primas de las 3400 codificadas,<br />
y sólo en una monografía se codifica la DRX para<br />
identificar al hidrato presente.<br />
Por otra parte, la USP no posee un capítulo general sobre<br />
polimorfismo similar a FA y BP. En ella se encuentra información<br />
parcial y muy dispersa en: Tablas de Referencia /<br />
Descripción y Solubilidad (para 10 materias primas indica<br />
que presentan polimorfismo); dentro de algunas monografías<br />
particulares, en el ítem Intervalo de Fusión (“puede<br />
existir también como una modificación polimórfica…”); y<br />
se codifica la identificación por DRX sólo para 8 materias<br />
primas, entre ellas carbamazepina, palmitato de cloranfenicol,<br />
indometacina, ritonavir, etc.<br />
La USP incluye el capítulo de información general <br />
de Disolución Intrínseca Aparente como indicativo de la<br />
solubilidad aparente de los fármacos y del efecto del polimorfismo,<br />
mientras que la BP menciona la VDI como parte<br />
del apéndice XII B. como anexo de recomendaciones del<br />
ensayo de disolución.<br />
Desde hace más de una década, la BP y la USP incluyen la<br />
mayoría de las técnicas para la caracterización del estado<br />
sólido.<br />
A partir del año 2010, como resultado de un proceso de<br />
armonización, ambas farmacopeas incorporaron el capítulo<br />
de Caracterización de sólidos cristalinos y parcialmente<br />
cristalinos por DRX del polvo. Este texto reemplazó al anterior<br />
de DRX en USP. En la BP, el apéndice XVII Q<br />
representa la incorporación de la técnica de DRX.<br />
El objetivo de este trabajo es establecer y destacar la<br />
importancia de la DRX de polvo, para la determinación del<br />
polimorfismo de IFAs desde el punto de vista de su inclusión<br />
como especificación de farmacopea. Para ello se presentan<br />
algunos ejemplos de IFAs que intentan demostrar<br />
esta premisa.<br />
Parte experimental<br />
Como parte de este trabajo se estudiaron los patrones<br />
de difracción de materias primas de azitromicina (AZM),<br />
clopidogrel bisulfato (CPG), nevirapina (NVP), atorvastatina<br />
cálcica (ATOR), y mebendazol (MBZ).<br />
Se emplearon materias primas comerciales del mercado<br />
argentino grado farmacopea, y se compararon con sustancias<br />
de referencia FA (SR-FA), BP (SR-BP) y USP (SR-USP), e<br />
información de Bases de Datos Powder Diffraction File y<br />
Cambridge Structural Database.<br />
Se utilizó un difractómetro Bruker D8 Advance con ánodo<br />
de cobre y monocromador de grafito para haz difractado.<br />
Desarrollo<br />
AZM es un antibiótico de la familia de los macrólidos<br />
empleado, entre otras, en el tratamiento de infecciones<br />
de las vías aéreas en adultos y en pacientes pediátricos. Es<br />
un polvo blanco cristalino, muy poco soluble en agua. Este<br />
IFA se encuentra en el listado del anexo I de la Disposición<br />
ANMAT Nº 4788/12 de fármacos con exigencia de demostración<br />
de BE.<br />
La FA menciona las formas anhidra y dihidrato, aunque<br />
codifica el dihidrato, indica la realización del ensayo de<br />
cristalinidad y el límite de aceptación para el contenido de<br />
agua es de 4-5% mediante la determinación por la técnica<br />
volumétrica de Karl Fischer (KF). La identificación se realiza<br />
por FTIR en forma sólida frente a la SR-FA (aún no disponible).<br />
La BP codifica el monohidrato y el dihidrato, incluye para<br />
el contenido de agua un límite entre 1,8-6,5 % que abarca<br />
los diferentes hidratos. La identificación se realiza por FTIR,<br />
al igual que en USP, pero se disuelven la muestra y la SR<br />
en un solvente (cloruro de metileno en BP y metanol en<br />
USP) si hay diferencias entre los espectros, se evapora y se<br />
36 revista safybi junio 2016