BỘ ĐỀ THI+HƯỚNG DẪN CHẤM CHÍNH THỨC CÁC SỞ GIÁO DỤC KÌ THI CHỌN HỌC SINH GIỎI CẤP TỈNH LỚP 9 THCS NĂM HỌC 2011-2012 MÔN HÓA HỌC
LINK DOCS.GOOGLE: https://drive.google.com/file/d/0B_NNtKpVZTUYSGNvaGlNdVl0LXM/view?usp=sharing
LINK DOCS.GOOGLE:
https://drive.google.com/file/d/0B_NNtKpVZTUYSGNvaGlNdVl0LXM/view?usp=sharing
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
www.twitter.com/daykemquynhon<br />
www.google.com/+DạyKèmQuyNhơn<br />
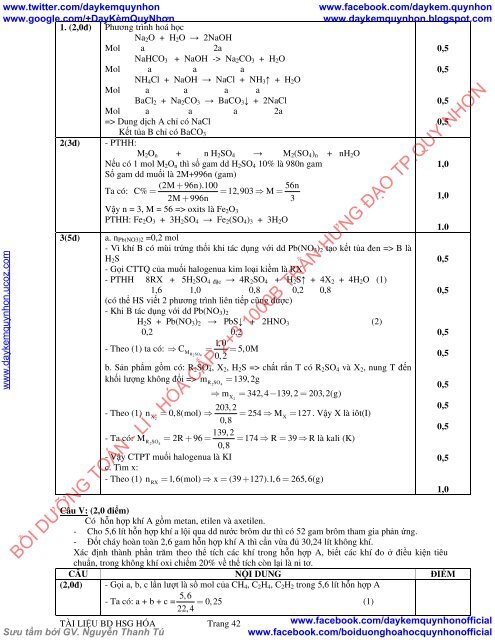
1. (2,0đ) Phương trình hoá học<br />
Na 2 O + H 2 O → 2NaOH<br />
Mol a 2a<br />
NaHCO 3 + NaOH -> Na 2 CO 3 + H 2 O<br />
Mol a a a<br />
NH 4 Cl + NaOH → NaCl + NH 3 ↑ + H 2 O<br />
Mol a a a a<br />
BaCl 2 + Na 2 CO 3 → BaCO 3 ↓ + 2NaCl<br />
Mol a a a 2a<br />
=> Dung dịch A chỉ có NaCl<br />
Kết tủa B chỉ có BaCO 3<br />
2(3đ) - PTHH:<br />
www.daykemquynhon.ucoz.com<br />
3(5đ)<br />
M 2 O n + n H 2 SO 4 → M 2 (SO 4 ) n + nH 2 O<br />
Nếu có 1 mol M 2 O n thì số gam dd H 2 SO 4 10% là 980n gam<br />
Số gam dd muối là 2M+996n (gam)<br />
(2M + 96n).100 56n<br />
Ta có: C% = = 12,903 ⇒ M =<br />
2M + 996n 3<br />
Vậy n = 3, M = 56 => oxits là Fe 2 O 3<br />
PTHH: Fe 2 O 3 + 3H 2 SO 4 → Fe 2 (SO 4 ) 3 + 3H 2 O<br />
a. n Pb(NO3)2 =0,2 mol<br />
- Vì khí B có mùi trứng thối khi tác dụng với dd Pb(NO 3 ) 2 tạo kết tủa đen => B là<br />
H 2 S<br />
- Gọi CTTQ của muối halogenua kim loại kiềm là RX<br />
- PTHH 8RX + 5H 2 SO 4 đặc → 4R 2 SO 4 + H 2 S↑ + 4X 2 + 4H 2 O (1)<br />
1,6 1,0 0,8 0,2 0,8<br />
(có thể HS viết 2 phương trình liên tiếp cũng được)<br />
- Khi B tác dụng với dd Pb(NO 3 ) 2<br />
H 2 S + Pb(NO 3 ) 2 → PbS↓ + 2HNO 3 (2)<br />
0,2 0,2<br />
1,0<br />
- Theo (1) ta có: ⇒ CM<br />
= = 5,0M<br />
H2SO4<br />
0,2<br />
b. Sản phẩm gồm có: R 2 SO 4 , X 2 , H 2 S => chất rắn T có R 2 SO 4 và X 2 , nung T đến<br />
khối lượng không đổi => m = 139, 2g<br />
R 2SO4<br />
TÀI LIỆU BD HSG <strong>HÓA</strong> Trang 42<br />
Sưu tầm bởi GV. Nguyễn Thanh Tú<br />
⇒ m = 342,4− 139,2 = 203,2(g)<br />
X 2<br />
203, 2<br />
- Theo (1) n<br />
X 2<br />
= 0,8(mol) ⇒ = 254 ⇒ MX<br />
= 127 . Vậy X là iôt(I)<br />
0,8<br />
139,2<br />
- Ta có: MR2SO<br />
= 2R + 96 = = 174 ⇒ R = 39 ⇒ R là kali (K)<br />
4<br />
0,8<br />
- Vậy CTPT muối halogenua là KI<br />
c. Tìm x:<br />
- Theo (1) n<br />
RX<br />
= 1,6(mol) ⇒ x = (39 + 127).1,6 = 265,6(g)<br />
Câu V: (2,0 điểm)<br />
Có hỗn hợp khí A gồm metan, etilen và axetilen.<br />
- Cho 5,6 lít hỗn hợp khí a lội qua dd nước brôm dư thì có 52 gam brôm tham gia phản ứng.<br />
- Đốt cháy hoàn toàn 2,6 gam hỗn hợp khí A thì cần vừa đủ 30,24 lít không khí.<br />
Xác định thành phần trăm theo thể tích các khí trong hỗn hợp A, biết các khí đo ở điều kiện tiêu<br />
chuẩn, trong không khí oxi chiếm 20% về thể tích còn lại là ni tơ.<br />
CÂU NỘI DUNG ĐIỂM<br />
(2,0đ) - Gọi a, b, c lần lượt là số mol của CH 4 , C 2 H 4 , C 2 H 2 trong 5,6 lít hỗn hợp A<br />
- Ta có: a + b + c = 5,6 0, 25<br />
22, 4 = (1)<br />
www.facebook.com/daykem.quynhon<br />
www.daykemquynhon.blogspot.com<br />
BỒI DƯỠNG TOÁN - LÍ - <strong>HÓA</strong> <strong>CẤP</strong> 2+3 1000B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
www.facebook.com/daykemquynhonofficial<br />
www.facebook.com/boiduonghoahocquynhonofficial<br />
0,5<br />
0,5<br />
0,5<br />
0,5<br />
1,0<br />
1,0<br />
1.0<br />
0,5<br />
0,5<br />
0,5<br />
0,5<br />
0,5<br />
0,5<br />
0,5<br />
0,5<br />
1,0