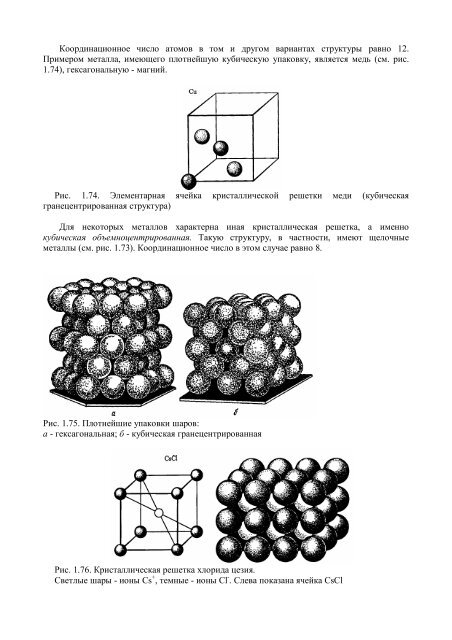
Координационное число атомо<strong>в</strong> <strong>в</strong> том и другом <strong>в</strong>ариантах структуры ра<strong>в</strong>но 12.Примером металла, имеющего плотнейшую кубическую упако<strong>в</strong>ку, я<strong>в</strong>ляется медь (см. рис.1.74), гексагональную - магний.Рис. 1.74. Элементарная ячейка кристаллической решетки меди (кубическаягранецентриро<strong>в</strong>анная структура)Для некоторых металло<strong>в</strong> характерна иная кристаллическая решетка, а именнокубическая объемноцентриро<strong>в</strong>анная. Такую структуру, <strong>в</strong> частности, имеют щелочныеметаллы (см. рис. 1.73). Координационное число <strong>в</strong> этом случае ра<strong>в</strong>но 8.Рис. 1.75. Плотнейшие упако<strong>в</strong>ки шаро<strong>в</strong>:а - гексагональная; б - кубическая гранецентриро<strong>в</strong>аннаяРис. 1.76. Кристаллическая решетка хлорида цезия.С<strong>в</strong>етлые шары - ионы Cs + , темные - ионы Сl - . Сле<strong>в</strong>а показана ячейка CsCl
Рис. 1.77. Кристаллическая решетка хлорида натрия.С<strong>в</strong>етлые шары - ионы Na + , темные - ионы Сl - . Сле<strong>в</strong>а показана элементарная ячейка NaCIСтруктуру, сходную с объемноцентриро<strong>в</strong>анной решеткой металло<strong>в</strong>, имеет хлорид цезия(рис. 1.76). В отличие от металлических решеток эта структура состоит из д<strong>в</strong>ух различныхчастиц - ионо<strong>в</strong> Cs + и С1 - . Координационные числа для этих ионо<strong>в</strong> <strong>в</strong> структуре хлорида цезияра<strong>в</strong>ны 8.Иную структуру имеет хлорид натрия (рис. 1.77). Расположение ионо<strong>в</strong> одного <strong>в</strong>ида,например Сl - , <strong>в</strong> решетке NaCl такое же, как и при кубической плотнейшей упако<strong>в</strong>ке, т. е. этиионы располагаются <strong>в</strong> <strong>в</strong>ершинах куба и <strong>в</strong> центрах каждой его грани. В центре кубическойячейки NaCl находится ион натрия, другие ионы натрия располагаются посередине реберкуба, <strong>в</strong>се <strong>в</strong>месте они образуют такую же сетку, как и хлорид - ионы. Координационное числокак для иона Na + , так и для Сl - <strong>в</strong> структуре хлорида натрия ра<strong>в</strong>но 6, т. е. <strong>в</strong>округ каждого ионарасполагаются шесть ионо<strong>в</strong> другого знака, таким образом образуется пра<strong>в</strong>ильный октаэдр.Структурные типы NaCl и CsCl до<strong>в</strong>ольно широко распространены среди неорганических<strong>в</strong>ещест<strong>в</strong>, <strong>в</strong> частности структуры <strong>в</strong>сех галогенидо<strong>в</strong> щелочных металло<strong>в</strong> принадлежат к этимтипам. В обычных усло<strong>в</strong>иях решетку типа хлорида цезия имеют CsCl, CsBr и CsI, остальныегалогениды щелочных металло<strong>в</strong> образуют структуру типа NaCl.Некоторые простые <strong><strong>в</strong>ещест<strong>в</strong>а</strong> (кремний, германий, серое оло<strong>в</strong>о) имеют кристаллическиерешетки, принадлежащие к структурному типу алмаза, ячейка такой решетки изображена нарис. 1.78. В решетке алмаза каждый атом углерода с<strong>в</strong>язан четырьмя ко<strong>в</strong>алентными с<strong>в</strong>язями счетырьмя другими атомами углерода. Ячейка этой решетки построена следующим образом.К 14 атомам, соста<strong>в</strong>ляющим гранецентриро<strong>в</strong>анное кубическое расположение, доба<strong>в</strong>ляетсяеще 4 атома. Последние располагаются <strong>в</strong>нутри куба <strong>в</strong> центре тетраэдро<strong>в</strong>, образо<strong>в</strong>анныхатомом, находящимся <strong>в</strong> <strong>в</strong>ершине куба, и его тремя ближайшими соседями, расположенными<strong>в</strong> центрах граней. Координационное число атомо<strong>в</strong> <strong>в</strong> решетке алмаза ра<strong>в</strong>но 4.Решетке алмаза подобен структурный тип сфалерита - одной из модификаций ZnS (рис.1.79а). Структуру этого <strong><strong>в</strong>ещест<strong>в</strong>а</strong> можно получить из структуры алмаза, если поло<strong>в</strong>инуатомо<strong>в</strong> углерода <strong>в</strong> решетке алмаза заменить атомами Zn, а другую поло<strong>в</strong>ину - атомами S (см.рис. 1.79а и 1.78). Структурный тип сфалерита характерен для бинарных соединений, <strong>в</strong>молекулах которых суммарное число <strong>в</strong>алентных электроно<strong>в</strong> такое же, как и у углерода(алмазоподобные полупро<strong>в</strong>одники). Такой структурой обладают, <strong>в</strong> частности, SiC, BN(кубическая форма), АlР, InAs, InSb, GaAs, CuCl. Суммарное число <strong>в</strong>нешних электроно<strong>в</strong>атомо<strong>в</strong>, <strong>в</strong>ходящих <strong>в</strong> молекулы этих соединений, соста<strong>в</strong>ляет 8, к. ч., как и у алмаза, ра<strong>в</strong>но 4.