Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
00<br />
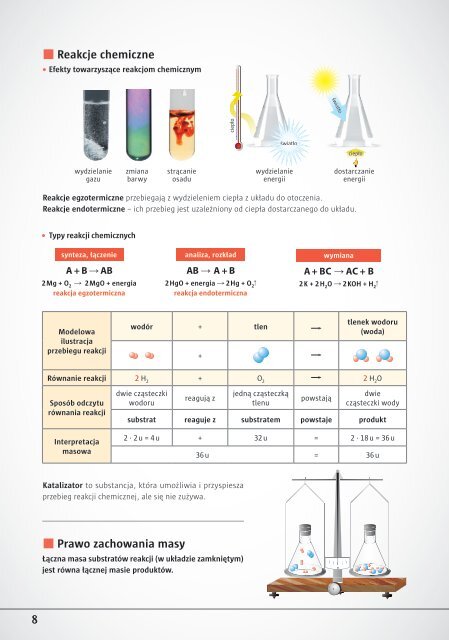
• Reakcje chemiczne<br />
• Efekty towarzyszące reakcjom chemicznym<br />
wydzielanie<br />
gazu<br />
zmiana<br />
barwy<br />
strącanie<br />
osadu<br />
wydzielanie<br />
energii<br />
dostarczanie<br />
energii<br />
Reakcje egzotermiczne przebiegają z wydzieleniem ciepła z układu do otoczenia.<br />
Reakcje endotermiczne – ich przebieg jest uzależniony od ciepła dostarczanego do układu.<br />
• Typy reakcji chemicznych<br />
synteza, łączenie<br />
analiza, rozkład<br />
wymiana<br />
2Mg + O 2 2MgO + energia<br />
reakcja egzotermiczna<br />
2HgO + energia 2Hg + O 2<br />
reakcja endotermiczna<br />
2K + 2H 2 O 2KOH + H 2<br />
Modelowa<br />
ilustracja<br />
przebiegu reakcji<br />
wodór + tlen<br />
+<br />
tlenek wodoru<br />
(woda)<br />
Równanie reakcji 2 H 2<br />
+ O 2<br />
2 H 2<br />
O<br />
Sposób odczytu<br />
równania reakcji<br />
Interpretacja<br />
masowa<br />
dwie cząsteczki<br />
wodoru<br />
reagują z<br />
jedną cząsteczką<br />
tlenu<br />
powstają<br />
dwie<br />
cząsteczki wody<br />
substrat reaguje z substratem powstaje produkt<br />
2 · 2 u = 4 u + 32 u = 2 · 18 u = 36 u<br />
36 u = 36 u<br />
Katalizator to substancja, która umożliwia i przyspiesza<br />
przebieg reakcji chemicznej, ale się nie zużywa.<br />
• Prawo zachowania masy<br />
Łączna masa substratów reakcji (w układzie zamkniętym)<br />
jest równa łącznej masie produktów.<br />
8