Vo Analytische Chemie I Komplexometrie 1
Vo Analytische Chemie I Komplexometrie 1
Vo Analytische Chemie I Komplexometrie 1
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
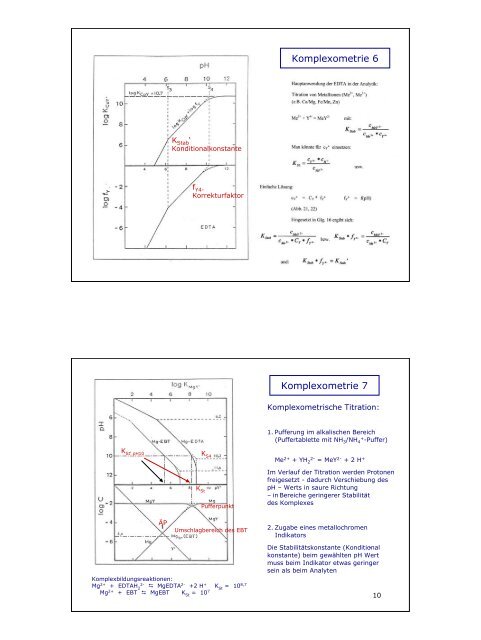
<strong>Komplexometrie</strong> 6<br />
K Stab ‘<br />
Konditionalkonstante<br />
f Y4-<br />
Korrekturfaktor<br />
9<br />
<strong>Komplexometrie</strong> 7<br />
Komplexometrische Titration:<br />
K St‘ pH10<br />
K St<br />
K S4<br />
Pufferpunkt<br />
1. Pufferung im alkalischen Bereich<br />
(Puffertablette mit NH 3 /NH 4+ -Puffer)<br />
Me 2+ + YH 2<br />
2- = MeY 2- + 2 H +<br />
Im Verlauf der Titration werden Protonen<br />
freigesetzt - dadurch Verschiebung des<br />
pH – Werts in saure Richtung<br />
– in Bereiche geringerer Stabilität<br />
des Komplexes<br />
ÄP<br />
Umschlagbereich des EBT<br />
Komplexbildungsreaktionen:<br />
Mg 2+ + EDTAH 2<br />
2- MgEDTA 2- +2 H + K St = 10 8,7<br />
Mg 2+ + EBT MgEBT K St = 10 7<br />
2. Zugabe eines metallochromen<br />
Indikators<br />
Die Stabilitätskonstante (Konditional -<br />
konstante) beim gewählten pH Wert<br />
muss beim Indikator etwas geringer<br />
sein als beim Analyten<br />
10