Synthese und Charakterisierung neuer schwach koordinierender ...
Synthese und Charakterisierung neuer schwach koordinierender ...
Synthese und Charakterisierung neuer schwach koordinierender ...
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Ergebnisse <strong>und</strong> Diskussion<br />
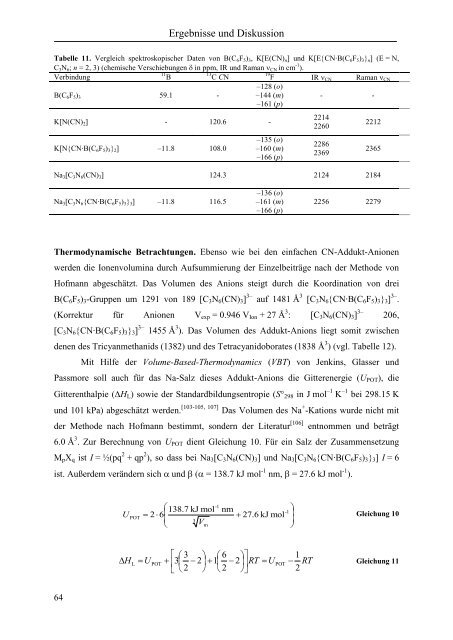
Tabelle 11. Vergleich spektroskopischer Daten von B(C 6 F 5 ) 3 , K[E(CN) n ] <strong>und</strong> K[E{CN∙B(C 6 F 5 ) 3 } n ] (E = N,<br />
C 3 N 6 ; n = 2, 3) (chemische Verschiebungen in ppm, IR <strong>und</strong> Raman CN in cm -1 ).<br />
Verbindung<br />
11 B<br />
13 C CN<br />
19 F IR CN Raman CN<br />
B(C 6 F 5 ) 3 59.1 -<br />
–128 (o)<br />
–144 (m)<br />
–161 (p)<br />
- -<br />
K[N(CN) 2 ] - 120.6 -<br />
K[N{CN∙B(C 6 F 5 ) 3 } 2 ] –11.8 108.0<br />
–135 (o)<br />
–160 (m)<br />
–166 (p)<br />
2214<br />
2260<br />
2286<br />
2369<br />
Na 3 [C 3 N 6 (CN) 3 ] 124.3 2124 2184<br />
2212<br />
2365<br />
Na 3 [C 3 N 6 {CN∙B(C 6 F 5 ) 3 } 3 ] –11.8 116.5<br />
–136 (o)<br />
–161 (m)<br />
–166 (p)<br />
2256 2279<br />
Thermodynamische Betrachtungen. Ebenso wie bei den einfachen CN-Addukt-Anionen<br />
werden die Ionenvolumina durch Aufsummierung der Einzelbeiträge nach der Methode von<br />
Hofmann abgeschätzt. Das Volumen des Anions steigt durch die Koordination von drei<br />
B(C 6 F 5 ) 3 -Gruppen um 1291 von 189 [C 3 N 6 (CN) 3 ] 3– auf 1481 Å 3 [C 3 N 6 {CN∙B(C 6 F 5 ) 3 } 3 ] 3– .<br />
(Korrektur für Anionen V exp = 0.946 V Ion + 27 Å 3 : [C 3 N 6 (CN) 3 ] 3– 206,<br />
[C 3 N 6 {CN∙B(C 6 F 5 ) 3 } 3 ] 3– 1455 Å 3 ). Das Volumen des Addukt-Anions liegt somit zwischen<br />
denen des Tricyanmethanids (1382) <strong>und</strong> des Tetracyanidoborates (1838 Å 3 ) (vgl. Tabelle 12).<br />
Mit Hilfe der Volume-Based-Thermodynamics (VBT) von Jenkins, Glasser <strong>und</strong><br />
Passmore soll auch für das Na-Salz dieses Addukt-Anions die Gitterenergie (U POT ), die<br />
Gitterenthalpie (H L ) sowie der Standardbildungsentropie (S° 298 in J mol –1 K –1 bei 298.15 K<br />
<strong>und</strong> 101 kPa) abgeschätzt werden. [103-105, 107] Das Volumen des Na + -Kations wurde nicht mit<br />
der Methode nach Hofmann bestimmt, sondern der Literatur [106] entnommen <strong>und</strong> beträgt<br />
6.0 Å 3 . Zur Berechnung von U POT dient Gleichung 10. Für ein Salz der Zusammensetzung<br />
M p X q ist I = ½(pq 2 + qp 2 ), so dass bei Na 3 [C 3 N 6 (CN) 3 ] <strong>und</strong> Na 3 [C 3 N 6 {CN∙B(C 6 F 5 ) 3 } 3 ] I = 6<br />
ist. Außerdem verändern sich <strong>und</strong> ( = 138.7 kJ mol -1 nm, = 27.6 kJ mol -1 ).<br />
<br />
-1<br />
<br />
<br />
138.7 kJ mol nm<br />
-1<br />
U <br />
<br />
<br />
POT<br />
2 6<br />
27.6 kJ mol<br />
Gleichung 10<br />
3<br />
Vm<br />
<br />
3 6 <br />
1<br />
H<br />
L<br />
U<br />
POT<br />
3<br />
2 1<br />
2<br />
RT U<br />
POT<br />
RT<br />
2 2<br />
<br />
Gleichung 11<br />
<br />
2<br />
64