2017-07-06 CHPS Working Paper No 7 Amnog_ mit ISSN
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
Lurasidon Takeda GmbH Schizophrenie<br />
Microbielle Collagenese Pfizer Pharma GmbH Dupuytren’sche Kontraktur<br />
Mirabegron Astellas Pharma GmbH Überaktive Blase<br />
Osimertinib AstraZeneca GmbH Lungenkarzinom<br />
Perampanel Eisai GmbH Epilepsie<br />
Pitavastatin Merckle Recordati GmbH Hypercholesterinämie<br />
Regorafenib Bayer Vital GmbH Kolorektalkarzinom<br />
Retigabin GlaxoS<strong>mit</strong>hKline GmbH & Co. KG Epilepsie<br />
Sipuleucel-T Dendreon UK Li<strong>mit</strong>ed Prostatakarzinom<br />
Tafluprost/Timolol Santen GmbH Offenwinkelglaukom, okuläre<br />
Hypertension<br />
Vildagliptin <strong>No</strong>vartis Pharma GmbH Diabetes mellitus Typ 2<br />
Vildagliptin, Metformin <strong>No</strong>vartis Pharma GmbH Diabetes mellitus Typ 2<br />
Quelle: Eigene Darstellung nach Greiner W., Witte J. (2016); Gemeinsamer Bundesausschuss (2016); DAZ online (2016a);<br />
DAZ online (2016b); GKV-Spitzenverband (2016b).<br />
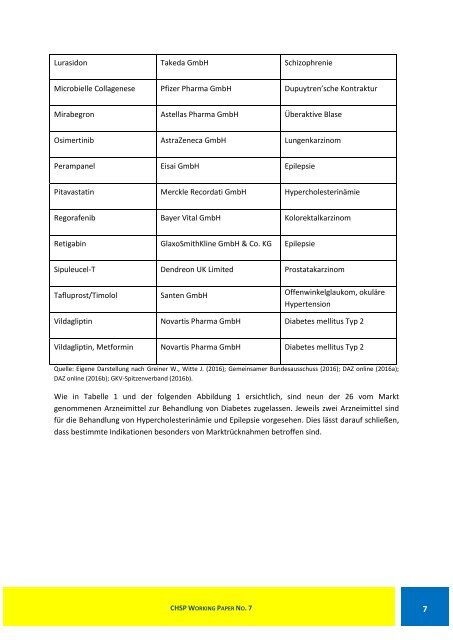
Wie in Tabelle 1 und der folgenden Abbildung 1 ersichtlich, sind neun der 26 vom Markt<br />
genommenen Arznei<strong>mit</strong>tel zur Behandlung von Diabetes zugelassen. Jeweils zwei Arznei<strong>mit</strong>tel sind<br />
für die Behandlung von Hypercholesterinämie und Epilepsie vorgesehen. Dies lässt darauf schließen,<br />
dass bestimmte Indikationen besonders von Marktrücknahmen betroffen sind.<br />
CHSP WORKING PAPER NO. 7<br />
7