apunts 16 - IES Guillem Cifre de Colonya
apunts 16 - IES Guillem Cifre de Colonya
apunts 16 - IES Guillem Cifre de Colonya
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
6<br />
2 EL CONTROL DEL METABOLISME<br />
Reactius i productes<br />
Moltes substàncies químiques quan reaccionen, <strong>de</strong>sprenen energia<br />
calorífica son les anomena<strong>de</strong>s reaccions exergòniques. Això es<br />
pot comprovar experimentalment observant com augmenta la<br />
temperatura <strong>de</strong>l medi en el qual es produeix la reacció. Aquest<br />
<strong>de</strong>spreniment es dóna perquè l’energia interna total <strong>de</strong> les<br />
substàncies reaccionants o reactius (també anomenada energia<br />
química perquè és l’energia emmagatzemada en els enllaços<br />
químics), és superior a l’energia interna <strong>de</strong> les substàncies<br />
produï<strong>de</strong>s o productes. Malgrat això. aquestes reaccions no es donen<br />
espontàniament. ja que, per iniciar una reacció, primer cal<br />
subministrar prou energia per <strong>de</strong>bilitar els enllaços <strong>de</strong>ls reactius i<br />
així possibilitar-ne la ruptura.<br />
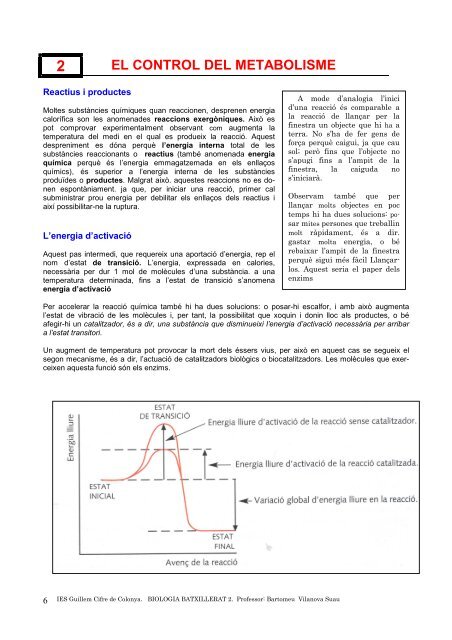
L’energia d’activació<br />
Aquest pas intermedi, que requereix una aportació d’energia, rep el<br />
nom d’estat <strong>de</strong> transició. L’energia, expressada en calories,<br />
necessària per dur 1 mol <strong>de</strong> molècules d’una substància. a una<br />
temperatura <strong>de</strong>terminada, fins a l’estat <strong>de</strong> transició s’anomena<br />
energia d’activació<br />
Per accelerar la reacció química també hi ha dues solucions: o posar-hi escalfor, i amb això augmenta<br />
l’estat <strong>de</strong> vibració <strong>de</strong> les molècules i, per tant, la possibilitat que xoquin i donin lloc als productes, o bé<br />
afegir-hi un catalitzador, és a dir, una substància que disminueixi l’energia d’activació necessària per arribar<br />
a l’estat transitori.<br />
Un augment <strong>de</strong> temperatura pot provocar la mort <strong>de</strong>ls éssers vius, per això en aquest cas se segueix el<br />
segon mecanisme, és a dir, l’actuació <strong>de</strong> catalitzadors biològics o biocatalitzadors. Les molècules que exerceixen<br />
aquesta funció són els enzims.<br />
<strong>IES</strong> <strong>Guillem</strong> <strong>Cifre</strong> <strong>de</strong> <strong>Colonya</strong>. BIOLOGIA BATXILLERAT 2. Professor: Bartomeu Vilanova Suau<br />
A mo<strong>de</strong> d’analogia l’inici<br />
d’una reacció és comparable a<br />
la reacció <strong>de</strong> llançar per la<br />
finestra un objecte que hi ha a<br />
terra. No s’ha <strong>de</strong> fer gens <strong>de</strong><br />
força perquè caigui, ja que cau<br />
sol; però fins que l’objecte no<br />
s’apugi fins a l’ampit <strong>de</strong> la<br />
finestra, la caiguda no<br />
s’iniciarà.<br />
Observam també que per<br />
llançar molts objectes en poc<br />
temps hi ha dues solucions: posar<br />
mites persones que treballin<br />
molt ràpidament, és a dir.<br />
gastar molta energia, o bé<br />
rebaixar l’ampit <strong>de</strong> la finestra<br />
perquè sigui més fàcil Llançarlos.<br />
Aquest seria el paper <strong>de</strong>ls<br />
enzims