EQUILIBRIS IÒNICS HETEROGENIS - textos online
EQUILIBRIS IÒNICS HETEROGENIS - textos online
EQUILIBRIS IÒNICS HETEROGENIS - textos online
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
g solut/100 g aigua<br />
60<br />
50<br />
40<br />
30<br />
20<br />
10<br />
0<br />
Ce2(SO4)3<br />
KClO4<br />
KNO3<br />
0 10 20 30 40 50 60<br />
Temperatura (ºC)<br />
Li2SO4<br />
K2SO4<br />
NH4Cl<br />
NaCl<br />
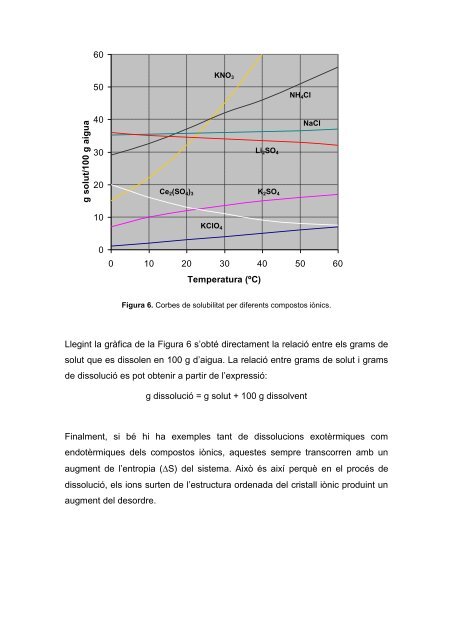
Figura 6. Corbes de solubilitat per diferents compostos iònics.<br />
Llegint la gràfica de la Figura 6 s’obté directament la relació entre els grams de<br />
solut que es dissolen en 100 g d’aigua. La relació entre grams de solut i grams<br />
de dissolució es pot obtenir a partir de l’expressió:<br />
g dissolució = g solut + 100 g dissolvent<br />
Finalment, si bé hi ha exemples tant de dissolucions exotèrmiques com<br />
endotèrmiques dels compostos iònics, aquestes sempre transcorren amb un<br />
augment de l’entropia (S) del sistema. Això és així perquè en el procés de<br />
dissolució, els ions surten de l’estructura ordenada del cristall iònic produint un<br />
augment del desordre.