rituximab
rituximab
rituximab
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
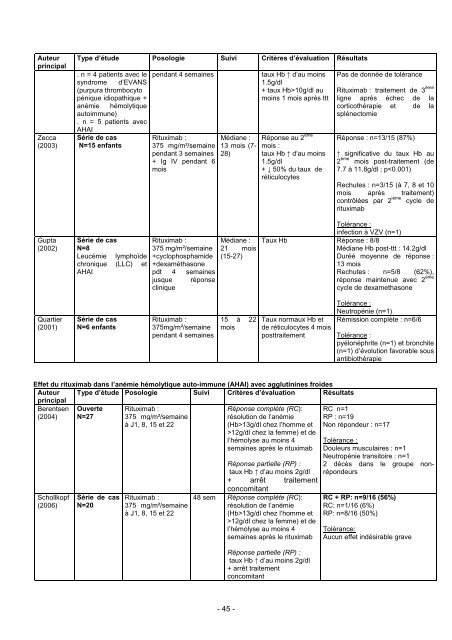
AuteurprincipalZecca(2003)Type d’étude Posologie Suivi Critères d’évaluation Résultats. n = 4 patients avec le pendant 4 semainessyndrome d’EVANS(purpura thrombocytopénique idiopathique +anémie hémolytiqueautoimmune). n = 5 patients avecAHAISérie de casRituximab :N=15 enfants 375 mg/m²/semainependant 3 semaines+ Ig IV pendant 6moisMédiane :13 mois (7-28)taux Hb ↑ d’au moins1.5g/dl+ taux Hb>10g/dl aumoins 1 mois après tttRéponse au 2 èmemois :taux Hb ↑ d’au moins1.5g/dl+ ↓ 50% du taux deréticulocytesPas de donnée de toléranceRituximab : traitement de 3 èmeligne après échec de lacorticothérapie et de lasplénectomieRéponse : n=13/15 (87%)↑ significative du taux Hb au2 ème mois post-traitement (de7.7 à 11.8g/dl ; p13g/dl chez l’homme et>12g/dl chez la femme) et del’hémolyse au moins 4semaines après le <strong>rituximab</strong>Réponse partielle (RP) :taux Hb ↑ d’au moins 2g/dl+ arrêt traitementconcomitant48 sem Réponse complète (RC):résolution de l’anémie(Hb>13g/dl chez l’homme et>12g/dl chez la femme) et del’hémolyse au moins 4semaines après le <strong>rituximab</strong>Réponse partielle (RP) :taux Hb ↑ d’au moins 2g/dl+ arrêt traitementconcomitantRC n=1RP : n=19Non répondeur : n=17Tolérance :Douleurs musculaires : n=1Neutropénie transitoire : n=12 décès dans le groupe nonrépondeursRC + RP: n=9/16 (56%)RC: n=1/16 (6%)RP: n=8/16 (50%)Tolérance:Aucun effet indésirable grave- 45 -