You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
6.2.3. Hukum Perbandingan berganda<br />
Dalton juga mengamati molekul dan difokuskan<br />
pada beberapa senyawa yang memiliki kesamaan<br />
dalam atom‐atom penyusunnya. Misalnya gas<br />
karbon monoksida (CO) dengan karbon dioksida<br />
(CO2), yang lain seperti air (H2O) dengan Hidrogen<br />
Peroksida (H2O2).<br />
Dalton menyimpulkan “dapat terjadi dua macam<br />
unsur membentuk dua senyawa atau lebih, jika<br />
unsur pertama memiliki massa yang sama, maka<br />
unsur kedua dalam senyawa‐senyawa tersebut<br />
memiliki perbandingan sebagai bilangan bulat dan<br />
sederhana”.<br />
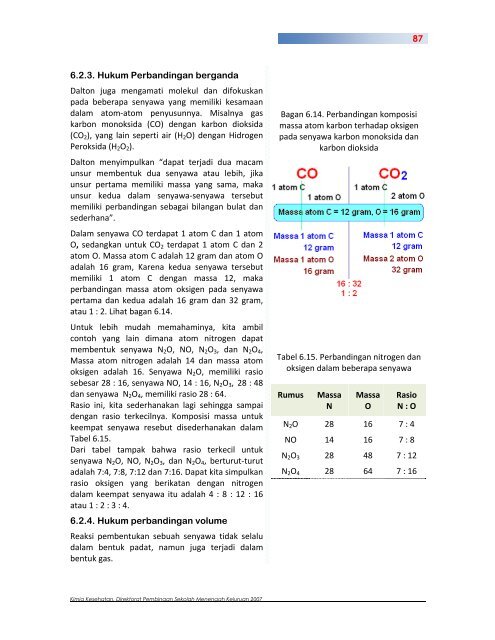
Dalam senyawa CO terdapat 1 atom C dan 1 atom<br />
O, sedangkan untuk CO2 terdapat 1 atom C dan 2<br />
atom O. Massa atom C adalah 12 gram dan atom O<br />
adalah 16 gram, Karena kedua senyawa tersebut<br />
memiliki 1 atom C dengan massa 12, maka<br />
perbandingan massa atom oksigen pada senyawa<br />
pertama dan kedua adalah 16 gram dan 32 gram,<br />
atau 1 : 2. Lihat bagan 6.14.<br />
Untuk lebih mudah memahaminya, kita ambil<br />
contoh yang lain dimana atom nitrogen dapat<br />
membentuk senyawa N2O, NO, N2O3, dan N2O4,<br />
Massa atom nitrogen adalah 14 dan massa atom<br />
oksigen adalah 16. Senyawa N2O, memiliki rasio<br />
sebesar 28 : 16, senyawa NO, 14 : 16, N2O3, 28 : 48<br />
dan senyawa N2O4, memiliki rasio 28 : 64.<br />
Rasio ini, kita sederhanakan lagi sehingga sampai<br />
dengan rasio terkecilnya. Komposisi massa untuk<br />
keempat senyawa resebut disederhanakan dalam<br />
Tabel 6.15.<br />
Dari tabel tampak bahwa rasio terkecil untuk<br />
senyawa N2O, NO, N2O3, dan N2O4, berturut‐turut<br />
adalah 7:4, 7:8, 7:12 dan 7:16. Dapat kita simpulkan<br />
rasio oksigen yang berikatan dengan nitrogen<br />
dalam keempat senyawa itu adalah 4 : 8 : 12 : 16<br />
atau 1 : 2 : 3 : 4.<br />
6.2.4. Hukum perbandingan volume<br />
Reaksi pembentukan sebuah senyawa tidak selalu<br />
dalam bentuk padat, namun juga terjadi dalam<br />
bentuk gas.<br />
Kimia Kesehatan, Direktorat Pembinaan Sekolah Menengah Kejuruan 2007<br />
87<br />
Bagan 6.14. Perbandingan komposisi<br />
massa atom karbon terhadap oksigen<br />
pada senyawa karbon monoksida dan<br />
karbon dioksida<br />
Tabel 6.15. Perbandingan nitrogen dan<br />
oksigen dalam beberapa senyawa<br />
Rumus Massa<br />
N<br />
Massa<br />
O<br />
Rasio<br />
N : O<br />
N2O 28 16 7 : 4<br />
NO 14 16 7 : 8<br />
N2O3 28 48 7 : 12<br />
N2O4 28 64 7 : 16