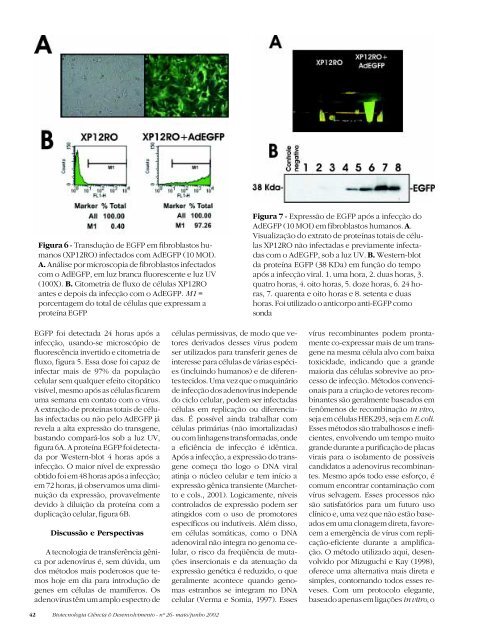
Figura 6 - Transdução de EGFP em fibroblastos humanos(XP12RO) infectados com AdEGFP (10 MOI).A. Análise por microscopia de fibroblastos infectadoscom o AdEGFP, em luz branca fluorescente e luz UV(100X). B. Citometria de fluxo de células XP12ROantes e depois da infecção com o AdEGFP. M1 =porcentagem do total de células que expressam aproteína EGFPFigura 7 - Expressão de EGFP após a infecção doAdEGFP (10 MOI) em fibroblastos humanos. A.Visualização do extrato de proteínas totais de célulasXP12RO não infectadas e previamente infectadascom o AdEGFP, sob a luz UV. B. Western-blotda proteína EGFP (38 KDa) em função do tempoapós a infecção viral. 1. uma hora, 2. duas horas, 3.quatro horas, 4. oito horas, 5. doze horas, 6. 24 horas,7. quarenta e oito horas e 8. setenta e duashoras. Foi utilizado o anticorpo anti-EGFP comosondaEGFP foi detectada 24 horas após ainfecção, usando-se microscópio defluorescência invertido e citometria defluxo, figura 5. Essa dose foi capaz deinfectar mais de 97% da populaçãocelular sem qualquer efeito citopáticovisível, mesmo após as células ficaremuma semana em contato com o vírus.A extração de proteínas totais de célulasinfectadas ou não pelo AdEGFP járevela a alta expressão do transgene,bastando compará-los sob a luz UV,figura 6A. A proteína EGFP foi detectadapor Western-blot 4 horas após ainfecção. O maior nível de expressãoobtido foi em 48 horas após a infecção;em 72 horas, já observamos uma diminuiçãoda expressão, provavelmentedevido à diluição da proteína com aduplicação celular, figura 6B.Discussão e PerspectivasA tecnologia de transferência gênicapor adenovírus é, sem dúvida, umdos métodos mais poderosos que temoshoje em dia para introdução degenes em células de mamíferos. Osadenovírus têm um amplo espectro decélulas permissivas, de modo que vetoresderivados desses vírus podemser utilizados para transferir genes deinteresse para células de várias espécies(incluindo humanos) e de diferentestecidos. Uma vez que o maquináriode infecção dos adenovírus independedo ciclo celular, podem ser infectadascélulas em replicação ou diferenciadas.É possível ainda trabalhar comcélulas primárias (não imortalizadas)ou com linhagens transformadas, ondea eficiência de infecção é idêntica.Após a infecção, a expressão do transgenecomeça tão logo o DNA viralatinja o núcleo celular e tem início aexpressão gênica transiente (Marchettoe cols., 2001). Logicamente, níveiscontrolados de expressão podem seratingidos com o uso de promotoresespecíficos ou indutíveis. Além disso,em células somáticas, como o DNAadenoviral não integra no genoma celular,o risco da freqüência de mutaçõesinsercionais e da atenuação daexpressão genética é reduzido, o quegeralmente acontece quando genomasestranhos se integram no DNAcelular (Verma e Somia, 1997). Essesvírus recombinantes podem prontamenteco-expressar mais de um transgenena mesma célula alvo com baixatoxicidade, indicando que a grandemaioria das células sobrevive ao processode infecção. Métodos convencionaispara a criação de vetores recombinantessão geralmente baseados emfenômenos de recombinação in vivo,seja em células HEK293, seja em E.coli.Esses métodos são trabalhosos e ineficientes,envolvendo um tempo muitogrande durante a purificação de placasvirais para o isolamento de possíveiscandidatos a adenovirus recombinantes.Mesmo após todo esse esforço, écomum encontrar contaminação comvírus selvagem. Esses processos nãosão satisfatórios para um futuro usoclínico e, uma vez que não estão baseadosem uma clonagem direta, favorecema emergência de vírus com replicação-eficientedurante a amplificação.O método utilizado aqui, desenvolvidopor Mizuguchi e Kay (1998),oferece uma alternativa mais direta esimples, contornando todos esses reveses.Com um protocolo elegante,baseado apenas em ligações in vitro, o42 <strong>Biotecnologia</strong> Ciência & Desenvolvimento - nº 26- maio/junho 2002
procedimento utiliza técnicas básicasde biologia molecular para incorporarDNA exógeno no esqueleto de umadenovirus humano do tipo 5, comreplicação-deficiente. Uma das maioresvantagens desse método consistena obtenção de quantias razoáveis ehomogêneas de vírus sem passar porqualquer procedimento de purificaçãode placas virais. O uso do gene marcadorEGFP torna possível ainda visualizartodo o processo de uma formaextremamente conveniente.O vírus recombinante carregando ocDNA egfp (AdEGFP) é capaz de infectar100% de uma população decélulas humanas, sem o menor traçode citotoxicidade, com um elevadonível de expressão do transgene. Aexpressão desse gene marcador começacom 4 horas e ainda podia serdetectado 5 dias após a infecção nascélulas utilizadas. A estabilidade daproteína a ser expressa e o padrão dereplicação da célula alvo podem modificaro modelo de expressão do transgene.Trabalhando com células primáriasem confluência, foi possível detectara expressão de proteínas funcionaistransduzidas por esses adenovírus recombinantesem até dois meses apósa infecção (Muotri e cols., 2002). Essesresultados mostram que o AdEGFPpossui uma alta capacidade de infecçãoe de transferência gênica, resultandonuma alta expressão de EGFP emfibroblastos humanos. A eficiência dessesvetores para uso clínico está sendoexplorada pela indústria biofarmacêutica,que visa à sua utilização na genômicafuncional. Qualquer modificaçãoque venha a melhorar a escala e arapidez do processo de criação deadenovírus recombinantes vai causarum impacto direto no número de genesque podem ser estudados. Acreditamosque o sistema como existe hojejá consegue suportar a produção depequenas bibliotecas de transgenesem adenovirus de forma eficiente. Alémdo mais, vírus com modificações específicasno transgene (previamente produzidaspor PCR degenerativo, porexemplo) podem ser selecionados invivo a partir de uma população originalcom base direta em ensaios funcionaisna célula alvo. Logicamente, o problemaimunológico e a característica epissomaldos adenovírus devem ser levadosem conta, principalmente quandose trabalha in vivo. O uso desses vetoresem terapia gênica deve levar aindaem consideração a resposta imune emhumanos, e o uso da última geração devetores adenovirais, com a maioria dosgenes virais ausentes, representa, comcerteza, um dos recentes avanços queserão, em breve, assimilados pela indústria.AgradecimentosAgradecemos os órgãos financiadores:CNPq e FAPESP.ReferênciasBranton, PE, Bayley, ST, Graham, FL.1985. Transformation by humanadenoviruses. Biophys. Acta. 780:67-94.Chalfie M, Tu Y, Euskirchen G, WardW, Prasher D. 1994. Green fluorescentprotein as a marker for geneexpression. Science. 96: 2988-2993.Cormack B, Valdivia R, Falkow S. 1996.FACs-optimized mutants of greenfluorescent protein (GFP). Gene.173: 33-38.Dani, SU. 2000. Terapia Gênica, vetorespara terapia gênica. <strong>Biotecnologia</strong>Ciência e Desenvolvimento.12: 28-33.Enders, JF, Bell, JA, Dingle, JH. 1956.“Adenoviruses”: group name proposedfor new respiratory-tract viruses.Science. 124: 119-120.Galos, RS, Williams, J, Shenk, T, Jones,J. 1980. Physical location of hostrangemutations of adenovirus type5, deletion and marker-rescue mapping.Virology. 104: 510-513.Graham FL, Smiley J, Russel WC, NarinR. 1977. Characteristics of a humancell line transformed by DNA fromhuman adenovirus type 5. J GenVirol. 36: 58-74.Graham FL. 2000. Adenovirus vectorsfor high-efficiency gene transferinto mammalian cells. Trends inImmunology Today. 21: 426-428.Hierholzer, JC. 1992. Adenoviruses inthe immunocompromised host. Cin.Microbiol. Rev. 5: 262-274.Hilleman, MR, Werner, JH. 1954. Recoveryof new agent from patientswith acute respiratory illness. ProcSoc Exp Biol Med. 85: 183-188.Horwitz MS. 1996. Adenovirus, p. 2149-2171. In. B.N. Fields, D.M. Knipeand P.M. Howley. (ed). Fields Virology,3 rd ed. Lippincott-Raven, Philadelphia,PA.Marchetto, MCN, Muotri, AR, Zerbini,LFC, Liebermann, TA, Ventura, A eMenck, CFM. 2001. The EGFP recombinantadenovirus: an examplefor efficient gene delivery and expressionin human cells. Virus RevRes. 6: 23-33.Mizuguchi, H., Kay, M.A. 1998. Efficientconstruction of a recombinant adenovirusvector by improved in vitroligation method. Hum. Gene. Ther.9: 2577-2583.Morral N, O’Neil Wanda, Rice K, LelandM, Kaplan J, Piedra PA, Zhou H,Parks R, Velji R, Aguilar-Córdova E,Wadsworth S, Graham FL, KochanekS, Dee Carey K, Beaudet AL. 1999.Administration of helper-dependentadenoviral vectors and sequentialdelivery of different vector serotypefor long-term liver-directed genetransfer in baboons. Proc Natl AcadSci USA. 96: 12816-12821.Muotri, AR, Marchetto, MCN, Zerbini,LC, Lieberman, T, Ventura, AM, Sarasin,A, Menck, CFM. 2002. Complementationof the DNA repair deficiencyin xeroderma pigmentosumgoup A and C cells by recombinantadenovirus-mediated gene transfer.Submetido.Rowe, WP, Huebner, RJ, Gilmore, LK.1953. Isolation of cytopathogenicagent from human adenoids undergoingspontaneous degeneration intissue culture. Proc. Soc. Exp. Biol.Med. 84: 570-573.Trentin, JJ, Yabe, Y, Taylo, G. 1962. Thequest for human cancer virus. Science.137: 835-849.Van Ormondt H, Maat J, Van BeverenCP. 1980. The nucleotide sequenceof the transforming early region E1of adenovirus type 5 DNA. Gene, 11:299-309.Ventura AM. 2000. Adenovirus vectorsand their application in gene therapy.Virus Rev Res. 5: 7-12.Verma, IM, Somia, N. 1997. Gene therapy– promises and prospects. Nature.389: 239-242.Yang Y, Nunes FA, Berencsi K, Furth EE,Gonczol E e Wilson JM. 1994. Cellularimmunity to viral antigens limitsE1-deleted adenoviruses for genetherapy. Proc Natl Acad Sci USA.91:4407-11.<strong>Biotecnologia</strong> Ciência & Desenvolvimento - nº 26- maio/junho 2002 43