Arbeitsplan Chemie G7 - KGS Wittmund
Arbeitsplan Chemie G7 - KGS Wittmund
Arbeitsplan Chemie G7 - KGS Wittmund
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
<strong>Arbeitsplan</strong> <strong>Chemie</strong> <strong>G7</strong> 2012/13<br />
Themen des Schuljahres im Überblick<br />
• Stoffe und ihre Eigenschaften/Teilchenmodell<br />
• Die chemische Reaktion<br />
• Luft und Verbrennung<br />
Lehrbuch: <strong>Chemie</strong> heute - Sekundarbereich I Schroedel 86043-8<br />
Leistungsbewertung: eine Klassenarbeit pro Halbjahr, gem. Fachkonferenzbeschluss Gewichtung ca. 1/3 schriftliche zu 2/3 sonstige u. mündliche Leistungen<br />
Im Jahrgang 7 ist verbindlich durch jede(n) Schüler(in) mindestens ein Stundenprotokoll anzufertigen, dessen Bewertung in die sonstigen<br />
Leistungen mit einfließt..<br />
Basiskonzepte StTB = Stoff-Teilchen-Beziehungen; SEB = Struktur-Eigenschafts-Beziehungen; ChR = Chemische Reaktion; EBSt = Energetische Betrachtung bei Stoffumwandlungen<br />
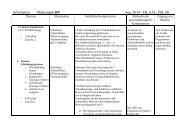
Inhaltsbezogene Kompetenz:<br />
Fachwissen<br />
Stoffe und ihre Eigenschaften/Teilchenmodell (15 Std.)<br />
Die Schülerinnen und Schüler ...<br />
wiederholen, erweitern bzw. erlernen die<br />
folgenden Stoffeigenschaften: Farbe,<br />
Geruch, Geschmack, Härte,<br />
Verformbarkeit, Löslichkeit, pH-Wert<br />
Bestimmung der Dichte von Feststoffen<br />
und Flüssigkeiten<br />
nutzen diese Eigenschaften fachgerecht<br />
bei der Erstellung eines Steckbriefes, oder<br />
bei der Analyse eines unbekannten Stoffes<br />
erklären die Aggregatzustände und das<br />
Lösen eines Stoffes mit dem Modell der<br />
kleinsten Teilchen<br />
Prozessbezogene Kompetenzen<br />
(E)rkenntnisgewinnung, (K)ommunikation, (B)ewertung<br />
(E) experimentieren sachgerecht nach Anleitung<br />
(E) beachten Sicherheitsaspekte<br />
(E) beobachten und beschreiben sorgfältig<br />
(E) erkennen und entwickeln einfache Fragestellungen, die mit Hilfe der<br />
<strong>Chemie</strong> bearbeitet werden können<br />
(E) planen einfache Experimente zur Hypothesenüberprüfung<br />
(E) entwickeln Strategien zur Trennung von Stoffgemischen<br />
(E) planen selbständig Experimente und wenden Nachweisreaktionen an<br />
(E) unterscheiden zwischen Stoffebene und Teilchenebene<br />
(E) wenden ein Teilchenmodell zur Erklärung von<br />
Aggregatzustandsänderungen an<br />
(K) protokollieren einfache Experimente<br />
(K) stellen Ergebnisse vor<br />
(K) nutzen verschiedene Informationsquellen<br />
(K) erklären chemische Sachverhalte unter Anwendung der Fachsprache<br />
Methoden, Medien / Weitere Materialien<br />
gemäß Methodencurriculum/Mediencurriculum /<br />
Fachbücher, Internet-Seiten, Software<br />
• Lehrbuch Kap. 2 und 3<br />
• Versuchsapparaturen z.B. zur Destillation oder<br />
Papierchromatographie,<br />
• Dichtebestimmung aus der Physik, Senkwaage<br />
• Konzept von Dr. Flint zur kontextorientierten<br />
Einführung von Säuren und Basen (hier allerdings nur<br />
ausgewählte Experimente)
erfahren über den Alkohol-Wasser-<br />
Versuch weitere Eigenschaften der kl.<br />
Teilchen<br />
stellen eine Übersicht homogener und<br />
heterogener Stoffgemische zusammen<br />
lernen exemplarische wichtige<br />
Trennverfahren auch in<br />
Anwendungssituationen kennen<br />
(K) stellen gewonnene Erkenntnisse im Modell dar • Alkohol-Wasser-Versuch, Erbsensamen und<br />
Leinsamen als „Teilchenmodelle“<br />
(E) unterscheiden zwischen Einstoff und Gemisch<br />
(B) stellen Anwendungsbereiche und Berufsfelder dar<br />
(B) stellen Bezüge zur Mathematik her (proportionale Zuordnung am Bsp. der<br />
Dichte)<br />
(K) kommunizieren fachgerecht korrekt unter Anwendung neuer Begriffe<br />
• Lehrbuch Kap. 3.2<br />
(E) erkennen in Texten und Darstellungen chemische Zusammenhänge wieder • Literatur zur Abwasserreinigung (z.B. Kläranlage,<br />
Benzinabscheider, Fettabscheider…), Ölherstellung,<br />
Doping usw.<br />
Fachbegriffe: Stoffeigenschaften: Aggregatzustände, Brennbarkeit, Löslichkeit, saure, neutrale, alkalische Lösungen, Siedetemperatur, Schmelztemperatur, Umgang mit<br />
dem Gasbrenner; Trennverfahren: Papierchromatographie, Destillation.
Inhaltsbezogene Kompetenz:<br />
Fachwissen<br />
Die chemische Reaktion (15 Std.)<br />
Die Schülerinnen und Schüler ...<br />
beschreiben, dass nach einer chemischen<br />
Reaktion die Ausgangsstoffe nicht mehr<br />
vorliegen und gleichzeitig immer neue<br />
Stoffe entstehen<br />
beschreiben, dass chemische Reaktionen<br />
immer mit einem Energieumsatz<br />
verbunden sind<br />
beschreiben, dass chemische Reaktionen<br />
grundsätzlich umkehrbar sind.<br />
beschreiben den prinzipiellen<br />
Zusammenhang zwischen<br />
Bewegungsenergie der<br />
Teilchen/Bausteine und der Temperatur<br />
beschreiben, dass sich Stoffe in ihrem<br />
Energiegehalt unterscheiden<br />
beschreiben, dass Systeme bei chemischen<br />
Reaktionen Energie mit der Umgebung,<br />
z.B. in Form von Wärme, austauschen<br />
können und dadurch ihren Energiegehalt<br />
verändern<br />
beschreiben die Wirkung eines<br />
Katalysators auf die Aktivierungsenergie<br />
Prozessbezogene Kompetenzen<br />
(E)rkenntnisgewinnung, (K)ommunikation, (B)ewertung<br />
(E) formulieren Vorstellungen zu Edukten und Produkten<br />
(E) planen Überprüfungsexperimente und führen sie unter Beachtung von<br />
Sicherheitsaspekten durch<br />
(E) entwickeln und vergleichen Verbesserungsvorschläge von<br />
Versuchsdurchführungen<br />
(E) erstellen Energiediagramme<br />
(E) deuten Prozesse der Energieübertragung mit dem einfachen<br />
Teilchenmodell<br />
(K) beschreiben, veranschaulichen oder erklären chemische Sachverhalte mit<br />
den passenden Modellen unter Anwendung der Fachsprache<br />
(K) aufstellen von Reaktionsschematas<br />
(K) unterscheiden Fachsprache von Alltagssprache beim Beschreiben<br />
chemischer Reaktionen<br />
(K) argumentieren fachlich korrekt über ihre Versuche<br />
(K) diskutieren Einwände selbstkritisch<br />
(K) kommunizieren fachsprachlich unter Anwendung energetischer Begriffe<br />
(B) erkennen, dass chemische Reaktionen in der Alltagswelt stattfinden<br />
(B) erkennen die Bedeutung chemischer Reaktionen für Natur und Technik<br />
(B) stellen Bezüge zur Physik und Biologie (innere Energie, Fotosynthese,<br />
Atmung) her<br />
(E) erstellen Energiediagramme <br />
Fachbegriffe exotherme und endotherme chemische Reaktionen; Aktivierungsenergie; Sauerstoffübertragungsreaktionen<br />
Methoden, Medien / Weitere Materialien<br />
gemäß Methodencurriculum/Mediencurriculum /<br />
Fachbücher, Internet-Seiten, Software<br />
Lehrbuch Kap. 4<br />
Typische Kennzeichen einer exothermen chemischen<br />
Reaktion lassen sich an der Reaktion zwischen einem<br />
Metall (Cu, Fe) und Schwefel erarbeiten.<br />
Als Beispiel für eine endotherme chemische Reaktion<br />
eignet sich blaues Kupfersulfat-Hydrat, das im Rgl.<br />
fortlaufend erhitzt wird<br />
Wärmekissen<br />
Thermische Zerlegung von Quecksilberoxid als<br />
Beispiel für eine endotherme chem. Reaktion<br />
(Erstellung eines Filmprotokolls)<br />
Lehrbuch Kap. 3 und 4<br />
Internetrecherchen, Posterpräsentationen
Inhaltsbezogene Kompetenz:<br />
Fachwissen<br />
Luft und Verbrennung (20 Std.)<br />
Die Schülerinnen und Schüler ...<br />
lernen die Oxidation als Reaktion mit<br />
Sauerstoff kennen, bei der Oxide<br />
entstehen<br />
erkennen langsame und schnelle<br />
Oxidationen (Rosten und Atmen)<br />
Prozessbezogene Kompetenzen<br />
(E)rkenntnisgewinnung, (K)ommunikation, (B)ewertung<br />
(E) vertiefen und erweitern ihre Kenntnisse zum Ablauf von chemischen<br />
Reaktionen<br />
Methoden, Medien / Weitere Materialien<br />
gemäß Methodencurriculum/Mediencurriculum /<br />
Fachbücher, Internet-Seiten, Software<br />
• Lehrbuch Kap.4.4<br />
• Verbrennung von Mg-Band und Eisenwolle als<br />
Beispiele für eine Oxidation<br />
• Untersuchungen an einer Kerzenflamme<br />
(E) erkennen die Bedeutung der Protokollführung für den Erkenntnisprozess • Rosten von Eisenwolle als langsame Oxidation<br />
• Quantitative Untersuchung der Zusammensetzung der<br />
Luft<br />
Erfahren die Zusammensetzung der Luft (E) zeigen exemplarisch Verknüpfungen zwischen chemischen Reaktionen im<br />
Alltag und im Labor<br />
führen Nachweisreaktionen durch (K) stellen chemische Reaktionen durch Aufstellung eines Reaktionsschemas<br />
(Wortgleichung) unter Einbeziehung des Energieumsatzes und der<br />
Aggregatzustände fachgerecht auf<br />
lernen Oxidationsvorgänge in der Umwelt<br />
kennen<br />
lernen die Reduktion als Reaktion kennen,<br />
bei der Sauerstoff abgegeben wird<br />
erkennen die Redoxreaktion als eine<br />
chem. Reaktion, bei der Oxidation und<br />
Reduktion gleichzeitig ablaufen<br />
leiten die Redoxreihe der Metalle durch<br />
Experimente ab<br />
lernen Anwendungsbeispiele von<br />
Redoxreaktionen im Alltag kennen<br />
(Metallgewinnung, Stahlerzeugung,<br />
Schweißen)<br />
(K) stellen gewonnene Daten in Emissionsdiagrammen dar bzw.<br />
(E ) nutzen diese zur Bewertung von Umweltproblemen<br />
(K) präsentieren ihre Arbeit als Team<br />
(K) argumentieren fachlich korrekt und folgerichtig über ihre Versuche<br />
(B) erkennen, dass chemische Reaktionen in der Alltagswelt stattfinden<br />
(B) erkennen die Bedeutung chemischer Reaktionen für Natur und Technik<br />
• Nachweis von Sauerstoff mithilfe der<br />
Glimmspanprobe<br />
• Verbrennungsvorgange abhängig vom jeweiligen<br />
Zerteilungsgrad (<strong>Chemie</strong> am Gartengrill)<br />
• Reduktion von Kupferoxid<br />
•<br />
• Gewinnung von Metallen ,Exkurs: Ötzi<br />
• Thermitgemisch, Stahlgewinnung,<br />
• Nachweis von Kohlenstoffdioxid mithilfe von<br />
Kalkwasser<br />
• Reduktion von Kohlenstoffdioxid mithilfe von<br />
brennendem Mg-Band<br />
▪ Redoxreaktionen mithilfe geeigneter Redoxpaare,<br />
Redoxreihe der Metalle<br />
(K) präsentieren ihre Arbeit im Team • Referate (z.B. Rauchgasreinigung,<br />
Brandbekämpfung, Schweißen ,Metallgewinnung…)<br />
• Exkurs Metalle, Legierungen<br />
Fachbegriffe: Verbrennungsprozess als chemische Reaktion, Sauerstoffübertragungsreaktionen; Nachweis von Sauerstoff (Glimmspanprobe) und Kohlenstoffdioxid<br />
(Kalkwassertrübung); Redoxreaktion