Alkene, Additionsreaktionen - Organische Chemie
Alkene, Additionsreaktionen - Organische Chemie
Alkene, Additionsreaktionen - Organische Chemie
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
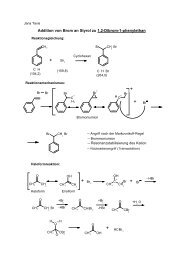
1.3. Ektrophile Additionen von H δ+ -X δ- an <strong>Alkene</strong><br />
H-X: H-OH,<br />
H-F, H-Cl, H-Br, H-I<br />
Addition von Halogenwasserstoffen.<br />
Die Halogenwasserstoffe können als konzentrierte Säuren oder aber<br />
gasförmig in die Lösung eines Alkens eingebracht werden. Die H + X - -<br />
Moleküle können in solvatisierte Ionen dissoziieren.<br />
In der Technik werden gasförmige <strong>Alkene</strong> mit gasförmigen<br />
Halogenwasserstoffen mit LEWIS-Säuren als Katalysatoren. Warum?<br />
δ +<br />
δ −<br />
R-CH=CH 2 + H----Br-AlBr 3 ----------> R-CHBr-CH 3<br />
Regel von Markownikow: "bei der HX-Addition an <strong>Alkene</strong> wird stets<br />
bevorzugt dar Wasserstoff am C-Atom mit weniger H-Atomen angelagert.<br />
Heute ist der Reaktionsmechanismus klar:<br />
Das Proton [H + ] addiert sich so an die Doppelbindung, dass sich das<br />
stabilere Carbeniumion bildet.<br />
H<br />
H<br />
H<br />
CH 3<br />
H<br />
H<br />
H<br />
H 3<br />
C<br />
C<br />
H 3<br />
H<br />
H 3<br />
C<br />
C<br />
H 3<br />
H<br />
H<br />
δ+ δ−<br />
H Cl<br />
egal<br />
C H 3<br />
Cl<br />
C H 3<br />
>. 98%<br />
H<br />
H<br />
H<br />
C H 3<br />
Cl<br />
CH 3<br />
H 3<br />
C H<br />
H<br />
auch etwas vom<br />
anderen Isomer!<br />
H<br />
Cl<br />
H<br />
H<br />
H<br />
H<br />
Cl<br />
H<br />
eher 50:50<br />
Matthäus 25, 29, erster Halbsatz<br />
7