Methanol-Vergiftung
Methanol-Vergiftung
Methanol-Vergiftung
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
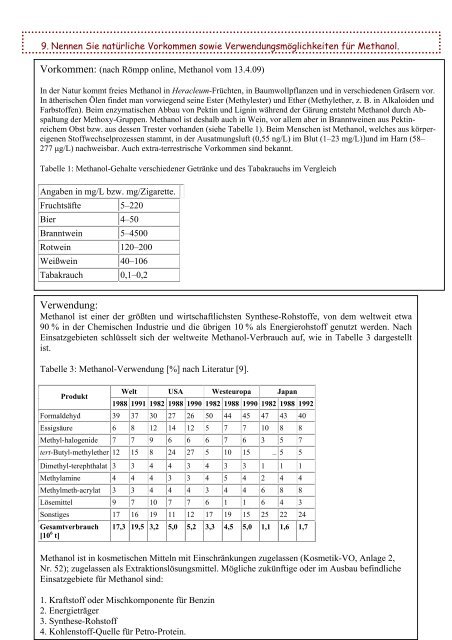
9. Nennen Sie natürliche Vorkommen sowie Verwendungsmöglichkeiten für <strong>Methanol</strong>.<br />
Vorkommen: (nach Römpp online, <strong>Methanol</strong> vom 13.4.09)<br />
In der Natur kommt freies <strong>Methanol</strong> in Heracleum-Früchten, in Baumwollpflanzen und in verschiedenen Gräsern vor.<br />
In ätherischen Ölen findet man vorwiegend seine Ester (Methylester) und Ether (Methylether, z. B. in Alkaloiden und<br />
Farbstoffen). Beim enzymatischen Abbau von Pektin und Lignin während der Gärung entsteht <strong>Methanol</strong> durch Abspaltung<br />
der Methoxy-Gruppen. <strong>Methanol</strong> ist deshalb auch in Wein, vor allem aber in Branntweinen aus Pektinreichem<br />
Obst bzw. aus dessen Trester vorhanden (siehe Tabelle 1). Beim Menschen ist <strong>Methanol</strong>, welches aus körpereigenen<br />
Stoffwechselprozessen stammt, in der Ausatmungsluft (0,55 ng/L) im Blut (1–23 mg/L)]und im Harn (58–<br />
277 µg/L) nachweisbar. Auch extra-terrestrische Vorkommen sind bekannt.<br />
Tabelle 1: <strong>Methanol</strong>-Gehalte verschiedener Getränke und des Tabakrauchs im Vergleich<br />
Angaben in mg/L bzw. mg/Zigarette.<br />
Fruchtsäfte 5–220<br />
Bier 4–50<br />
Branntwein 5–4500<br />
Rotwein 120–200<br />
Weißwein 40–106<br />
Tabakrauch 0,1–0,2<br />
Verwendung:<br />
<strong>Methanol</strong> ist einer der größten und wirtschaftlichsten Synthese-Rohstoffe, von dem weltweit etwa<br />
90 % in der Chemischen Industrie und die übrigen 10 % als Energierohstoff genutzt werden. Nach<br />
Einsatzgebieten schlüsselt sich der weltweite <strong>Methanol</strong>-Verbrauch auf, wie in Tabelle 3 dargestellt<br />
ist.<br />
Tabelle 3: <strong>Methanol</strong>-Verwendung [%] nach Literatur [9].<br />
Produkt<br />
Welt USA Westeuropa Japan<br />
1988 1991 1982 1988 1990 1982 1988 1990 1982 1988 1992<br />
Formaldehyd 39 37 30 27 26 50 44 45 47 43 40<br />
Essigsäure 6 8 12 14 12 5 7 7 10 8 8<br />
Methyl-halogenide 7 7 9 6 6 6 7 6 3 5 7<br />
tert-Butyl-methylether 12 15 8 24 27 5 10 15 – 5 5<br />
Dimethyl-terephthalat 3 3 4 4 3 4 3 3 1 1 1<br />
Methylamine 4 4 4 3 3 4 5 4 2 4 4<br />
Methylmeth-acrylat 3 3 4 4 4 3 4 4 6 8 8<br />
Lösemittel 9 7 10 7 7 6 1 1 6 4 3<br />
Sonstiges 17 16 19 11 12 17 19 15 25 22 24<br />
Gesamtverbrauch<br />
[10 6 t]<br />
17,3 19,5 3,2 5,0 5,2 3,3 4,5 5,0 1,1 1,6 1,7<br />
<strong>Methanol</strong> ist in kosmetischen Mitteln mit Einschränkungen zugelassen (Kosmetik-VO, Anlage 2,<br />
Nr. 52); zugelassen als Extraktionslösungsmittel. Mögliche zukünftige oder im Ausbau befindliche<br />
Einsatzgebiete für <strong>Methanol</strong> sind:<br />
1. Kraftstoff oder Mischkomponente für Benzin<br />
2. Energieträger<br />
3. Synthese-Rohstoff<br />
4. Kohlenstoff-Quelle für Petro-Protein.