Diagnostik des variablen Immundefektsyndroms (CVID) - Karger
Diagnostik des variablen Immundefektsyndroms (CVID) - Karger
Diagnostik des variablen Immundefektsyndroms (CVID) - Karger
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
SackU, Tárnok A, RotheG(Hrsg):Zellulä re<strong>Diagnostik</strong>.Grundlagen,Methodenundklinische<br />
AnwendungenderDurchflusszytometrie.Basel,<strong>Karger</strong>,2007,pp 721–740<br />
..............................<br />
<strong>Diagnostik</strong><strong>des</strong><strong>variablen</strong><br />
<strong>Immundefektsyndroms</strong> (<strong>CVID</strong>)<br />
Klaus Warnatz,MichaelSchlesier<br />
AbteilungRheumatologieundKlinischeImmunologie, MedizinischeKlinik,<br />
Universitä tsklinikum Freiburg, Freiburgi. Br.,Deutschland<br />
Einleitung<br />
Das <strong>CVID</strong> (commonvariable immunodeficiency) ist die hä ufigste klinisch<br />
relevante Immundefekterkrankung. In den westlichen Ländern liegt die Inzidenz<br />
zwischen 1:20 000 und 1:200 000 [1]. Bei dieser Erkrankung handelt es<br />
sich umein Antikö rpermangelsyndrom mit einer Erniedrigung von min<strong>des</strong>tens<br />
zwei der Antikö rperklassen IgG, IgM und IgA um min<strong>des</strong>tens zwei Standardabweichungen<br />
unter den altersentsprechenden Mittelwert ( www.esid.org ). Nach<br />
den Diagnosekriterien der European Society of Immunodeficiency (ESID) beginnt<br />
die Immundefizienz nach dem 2.Lebensjahr, und Impfantworten fehlen<br />
meist. Da es sich bei dem <strong>CVID</strong> um eine Ausschlussdiagnose handelt, müssen<br />
bekannte genetische, infektiöse und toxische Ursachen ausgeschlossen werden<br />
(Tab. 1).<br />
Ungefähr 20%derFälle[2,3]zeigeneinefamiliä reHä ufungundlasseneine<br />
genetischeUrsachevermuten. EinegenetischeVerbindungbesteht zu derhä ufigeren,abermeist<br />
klinischinapparentenselektivenIgA-Defizienz [4].Klinischfallen<br />
die Patienten hä ufig erst als Jugendliche oder junge Erwachsene vor allem durch<br />
rezidivierende respiratorischeInfektederoberenundunterenAtemwegeauf.Diese<br />
fü hren unbehandelt zu einem irreversiblen Umbau der Bronchien und schließlich<br />
zu einer schweren Lungenerkrankung. Im Gegensatz zu Patienten mit schweren<br />
kombiniertenImmundefektenkommt esbei<strong>CVID</strong>-Patientenvor allemzuInfektionenmit<br />
bekapseltenBakterien. AtypischeInfektesindselten. Zusä tzlichleidenvie-
Tab.1. Differentialdiagnose <strong>des</strong> Antikö rpermangels (Quelle: www.esid.org )<br />
Pathogenese Beispiele<br />
Medikamenteninduziert Antimalariamittel<br />
Captopril<br />
Carbamazepin<br />
Glucokortikoide<br />
Fenclofenac<br />
Goldsalze<br />
Penicillamin<br />
Phenytoin<br />
Sulfasalazin<br />
Methotrexat<br />
Genetische Erkrankungen Ataxia telangiectasia<br />
autosomale Formen <strong>des</strong> SCID<br />
Hyper-IgM-Syndrom<br />
Transcobalamin-II-Defizienz und Hypogammaglobulinä mie<br />
X-chromosomale Agammaglobulinä mie<br />
X-chromosomales lymphoproliferatives Syndrom (EBV-assoziiert)<br />
X-chromosomales SCID<br />
metabolische Störungen<br />
Chromosomenanomalien<br />
Chromosom-18q-Syndrom<br />
Monosomie 22<br />
Trisomie 8<br />
Trisomie 21<br />
Infektionskrankheiten HIV<br />
kongenitale Rö telninfektion<br />
kongenitale CMV-Infektion<br />
kongenitale Infektion mit Toxoplasma gondii<br />
EBV-Infektion<br />
Hämatologische Tumoren Chronisch-lymphatische Leukä mie<br />
Immundefizienz mit Thymom<br />
Non-Hodgkin-Lymphome<br />
B-Zell-Lymphome<br />
Systemerkrankungen Immundefizienz durch Hyperkatabolismus von Immunglobulinen<br />
Darmerkrankungen Lymphangiektasie<br />
Schwere Diarrhö mit Proteinverlust<br />
Malabsorption<br />
Nierenerkrankung Nephrose<br />
Schwere Verbrennungen Proteinverlust<br />
Indikationen<br />
722 Warnatz/Schlesier
Indikationen<br />
le der Patienten imVerlauf der Erkrankung unter gastrointestinalen Infekten. Die<br />
weitere Klinik umfasst Autoimmunphä nomene, Lymphoproliferation (Splenomegalie,<br />
Lymphadenopathie), Lymphome und granulomatöse Entzündungsreaktionen[5].<br />
Die Pathogenese diesesSyndroms ist weitgehend unklar und sicherlich heterogen.<br />
In der Vergangenheit wurden sowohl Störungen der T-Zell- als auch<br />
der B-Zell-Differenzierung und -Funktion beschrieben [6 – 8]. Die <strong>Diagnostik</strong><br />
umfasst neben der gründlichen Anamnese und Untersuchung <strong>des</strong> Patienten die<br />
serologische Bestimmung der Antikö rpertiter, den serologischen Ausschluss<br />
von Paraproteinen und auslösenden Infektionen, die Knochenmarkpunktion sowie<br />
bildgebende Verfahren zur Erfassung von Organschä den. Die Durchflusszytometrie<br />
ergänzt diese <strong>Diagnostik</strong> durch die Bestimmung der Lymphozytenpopulationen<br />
imperipheren Blut und durch die Untersuchung auf bekannte<br />
genetische Defekte. Die Bestimmung der Lymphozytenpopulationen dient dabei<br />
dem Ausschluss schwerer Störungen <strong>des</strong> Immunsystems, großer monoklonaler<br />
Populationen und der Identifizierung früher Störungen der B-Zell-Differenzierung<br />
mit sehr niedrigen B-Zell-Zahlen im peripheren Blut, wie zum<br />
Beispiel der X-chromosomalen Agammaglobulinä mie (Morbus Bruton) bei<br />
Defekt der Bruton-Tyrosinkinase (BTK) [9].Durch Zusatzuntersuchungenwerden<br />
die Hyper-IgM-Syndrome bei Defekten von CD40-Ligand (CD40L) und<br />
CD40 [10] ausgeschlossen. Im Jahr 2003 wurde mit dem Nachweis einer homozygoten<br />
ICOS-Defizienz (ICOS ¼ induzierbarer Kostimulator) bei zwei Familien<br />
mit je zwei Patienten die erste monogenetische Ursache eines <strong>variablen</strong><br />
Immundefekts gefunden [11]. ICOS ist ein kostimulatorisches Molekül der<br />
CD28-Familie, das nach Aktivierung auf T-Zellen exprimiert wird [12]. Dieser<br />
Defekt lä sst sich imFACS nach Aktivierung von T-Zellen nachweisen. Die anderen<br />
Unterformen <strong>des</strong> Hyper-IgM-Syndroms bei AID-, UNG- und NEMO-<br />
Defizienz [10]dagegen kö nnenals Differentialdiagnosendurchdurchflusszytometrische<br />
Untersuchungen bisher genauso wenig ausgeschlossen werden wie<br />
die Unterformen <strong>des</strong> X-chromosomalen lymphoproliferativen Syndroms (XLP)<br />
[13] bei SAP-Defizienz.<br />
In letzter Zeit gewinnt die Durchflusszytometrie zunehmend anBedeutung<br />
in der Klassifikation <strong>des</strong> <strong>CVID</strong>. Innerhalb der letzten 2Jahre wurden zwei Klassifikationsschemata<br />
auf der Basis der Analyse der verschiedenen B-Zell-Subpopulationenvorgeschlagen<br />
[14, 15]. Frühere Schemata, die auch T-Zell-Populationen<br />
berücksichtigten [16], wie auch die funktionelle Klassifikation nach<br />
Bryant etal. [17] konnten sich inder Klinik nicht durchsetzen. Zur Zeit wird in<br />
einer europä ischen Multicenter-Studie die Konsistenz und klinische Relevanz<br />
der beiden Klassifikationen getestet (Koordinator K. Warnatz), um sie anschließend<br />
zusammenzufü hren. Leider stand das Ergebnis zum Zeitpunkt <strong>des</strong> Redaktionsschlussesnochaus.<br />
<strong>Diagnostik</strong> <strong>des</strong><strong>variablen</strong><strong>Immundefektsyndroms</strong> (<strong>CVID</strong>) 723
Protokoll<br />
Prinzip<br />
Vierfarbdurchflusszytometrie: Die beschriebenen Färbungensind reine Oberflä<br />
chenfärbungen. Alle Protokolle sind auf Analysen am FACSCalibur (BD Biosciences,<br />
Heidelberg, Deutschland) mit 488-nm-Laser und 635-nm-Dioden-Laser<br />
sowie mit CellQuest-Software (BD Biosciences) ausgelegt. Entsprechende Adaptationen<br />
an andere Zytometer mü ssen gegebenenfalls vorgenommen werden. Die<br />
Grundlagen der Bedienung, Gerä teeinstellungen, Kompensierungen, zweidimensionalen<br />
Punktwolken-Analysen (Dot-Plot) und das Setzenvon Auswertefenstern<br />
(Regions,Gates) werdenals bekanntvorausgesetzt.<br />
Fü rdie Fä rbungen werden periphere mononukleäre Blutzellen (peripheral<br />
blood mononuclear cells; PBMNCs) verwendet, die durch Ficoll-Dichtegradientenzentrifugation<br />
aus EDTA-Blutgewonnenwerden. VollblutfärbungenderB-ZellenmitgewaschenemBlutwerdeninderLiteraturbeschrieben[18],sindaberwegen<br />
der Verwendung von Anti-Immunglobulin-Antikö rpern problematisch, da<br />
Reste von Serumimmunglobulin die Fä rbungen stören. Einzelne Fä rbungen sind<br />
nurnachentsprechenderIn-vitro-Aktivierungmöglich.<br />
KleinerLymphozytenstatus<br />
Indikationen<br />
In einer Vollblutfärbung werden die jeweiligen Anteile der CD4-,<br />
CD8-T-Zellen, B-Zellen und NK-Zellen bestimmt (Tab.3). Durch gleichzeitige<br />
Bestimmung <strong>des</strong> Differentialblutbilds werden zusä tzlich die Absolutwerte ermittelt.<br />
Ausschlussvon Differentialdiagnosen<br />
Grundsä tzlich ist zu bemerken, dass durch die beschriebenen FACS-Untersuchungennur<br />
quantitativeDefekte, aberkeinefunktionellensowieminimalstrukturellen<br />
Verä nderungenerfasst werden. WeiterefunktionelleUntersuchungensind<br />
bei entsprechender Indikation in Speziallabors mö glich. Zum Ausschluss <strong>des</strong> Hyper-IgM-Syndroms<br />
bei CD40-Defekt (ehemalig Typ 3) wird CD40 auf B-Zellen<br />
gefärbt. Sowohl CD40L- als auch ICOS-Defekte lassen sich nur auf aktivierten<br />
T-Zellennachweisen. WährenddieICOS-Induktion nachStimulation in PBMNCs<br />
untersucht werdenkann,empfiehltessichzum Nachweis derOberflä chenexpression<br />
vonCD40L, CD4 þ TZellenvorheraufzureinigen.<br />
Klassifikation <strong>des</strong><strong>CVID</strong><br />
ImJahr 2002 beschriebenwir dieersteKlassifikation <strong>des</strong><strong>CVID</strong> aufderBasis<br />
durchflusszytometrischer Untersuchungen (Freiburg-Klassifikation [14]). Seitdem<br />
724 Warnatz/Schlesier
Indikationen<br />
wurde insbesondere durch die Gruppevon Prof. Ochsenhendler (Paris-Klassifikation,<br />
[15]) eine weitere Klassifikation vorgeschlagen, die sich mit der ersten in<br />
wesentlichenBefundenüberschneidet.<br />
Freiburg-Klassifikation<br />
Die B-Zell-Populationen werden anhand von 2Färbungen evaluiert (Tab.4).<br />
DurchdieersteFä rbungB1werdendieZahlendernaiven(CD19þ CD27 IgM þ<br />
IgD þ ), der IgM-Gedächtnis- (CD19þ CD27þ IgM þ IgD þ )und der klassengewechselten<br />
Gedächtnis-B-Zellen (CD19þ CD27þ IgM IgD )erfasst. Die in<br />
unsererErfahrungmeistnur sehr geringe Zahl an«IgMonly»-Gedä chtnis-B-Zellen<br />
wird hierbei vernachlä ssigt, kann aber ohne Problem aus der Messung abgelesen<br />
werden.<br />
In einer zweiten Färbung B2wird der Anteil an transitionalen (CD19þ<br />
CD21 int CD38 þþ IgM þþ) B-Zellen, Plasmablasten (CD19 low CD21 low<br />
CD38 þþþ IgM – )und einer aktivierten CD21 low -Population (CD19 high CD21 low<br />
CD38 low IgM þ )bestimmt.DieHerkunftderCD21 low -Population istunklar,in der<br />
erstenStudiewurde abereineAssoziation dieserZellenmit Autoimmunphä nomenenundSplenomegalienachgewiesen.<br />
Aus diesenbeidenFärbungenergibt sicheine EinteilungderPatienten,diein<br />
demFlussschemavonAbbildung1dargestelltist.<br />
Abb.1. Flussschema der Freiburg-Klassifikation von Patienten mit <strong>CVID</strong>. Die Klassifikation<br />
beruht auf der Messung der verschiedenen B-Zell-Subpopulationen. Der Typ 1zeichnet sich<br />
durcheineErniedrigungderklassengewechseltenB-Zellenaufunter0,4%derLymphozytenaus,<br />
wä hrend Patienten <strong>des</strong> Typs2eine nahezu normale Anzahl haben. Der Typ 1kann anhand der<br />
Expansion einer CD21 low B-Zell-Population auf ü ber 20% der B-Zellen ineinen Typ 1a und<br />
einenTyp 1b( < 20%) unterschiedenwerden[14].<br />
<strong>Diagnostik</strong> <strong>des</strong><strong>variablen</strong><strong>Immundefektsyndroms</strong> (<strong>CVID</strong>) 725
Paris-Klassifikation<br />
Die Einteilung der <strong>CVID</strong>-Patienten nach dem Pariser Schema [15] beruht<br />
auf einer Färbung, die der Färbung B1der Freiburger Klassifikation entspricht.<br />
Hierbei werden die Gruppen MB2 mit normalen Gedächtnis-B-Zellen, MB1 mit<br />
erniedrigten klassengewechselten und normalen IgM-Gedächtnis-B-Zellen und<br />
MB0 mit einer Reduktion beiderGedächtnis-B-Zell-Populationen unterschieden.<br />
Als erniedrigt gelten Werte die 2Standardabweichungenunterhalb derNorm liegen.<br />
In der untersuchten Kohorte lagen die Werte bei < 11% CD27þ B-Zellen<br />
fü rdie Gruppe MB0 und < 8%klassengewechselte B-Zellen fü rdie Gruppe<br />
MB1.<br />
Material<br />
Probenmaterial<br />
8ml EDTA-antikoaguliertes Blut (nicht ä lter als 24h), bei Bestimmung von<br />
ICOS undCD40LnachAktivierungzusä tzlich8ml.<br />
Reagenzien<br />
– Ficoll-Trennlö sung(1,077g/ml; Biochrom,Berlin,Deutschland)<br />
– RPMI 1640(Biochrom)<br />
– FCS(PANBiotech,Aidenbach,Deutschland)<br />
– FACSFlow 1 (BD Biosciences)<br />
– OptilyseB(Beckman-Coulter,Krefeld, Deutschland)<br />
– IntraPrep(Beckman-Coulter)<br />
– EntionisiertesWasser.<br />
Gerä te<br />
– FACSCalibur mit488-nm-Laserund635-nm-Dioden-Laser<br />
– Standardpipetten<br />
– Zentrifuge<br />
– Zählkammer<br />
– Vortex<br />
– 50-ml-Falcon-Polypropylen-Rö hrchenmit Deckel(BD Biosciences)<br />
– 15-ml-Falcon-Polypropylen-Rö hrchenmit Deckel(BD Biosciences)<br />
– 12 75-mm-Falcon-Polystyrolrö hrchen(BD Biosciences)<br />
– 0,5-ml-Probenrö hrchen mit Deckel (Biozym, Hessisch Oldendorf,<br />
Deutschland).<br />
Antikö rper<br />
DieverwendetenAntikö rpersindin Tabelle2aufgelistet.<br />
Indikationen<br />
726 Warnatz/Schlesier
Indikationen<br />
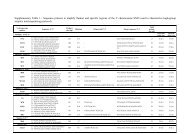
Tab.2. Liste der verwendeten Antikörper a<br />
Antikörper Klon Fluorochrom Bestellnummer Lieferant<br />
CD3 SK7 APC 345767 BD<br />
CD4 13B8,2 FITC IM0448 BC<br />
CD8 B9,11 PE IM0452 BC<br />
CD16 3G8 PE IM1238 BC<br />
CD19 J4,119 FITC IM1284 BC<br />
CD19 J4,119 PC7 IM3628 BC<br />
CD21 B-ly4 PE 555422 BD<br />
CD27 M-T271 FITC F7178 Dako<br />
CD38 HIT2 FITC 555459 BD<br />
CD40 5C3 FITC 555588 BD<br />
CD40-L TRAP1 PE 555700 BD<br />
CD45 2D1 PerCP 345809 BD<br />
CD56 NKH-1 PE IM2073 BC<br />
CD69 FN50 FITC 555530 BD<br />
Anti ICOS ISA-3 PE 12–9948–71 e-bioscience<br />
Anti-IgM Ziege F(ab) 2 Cy5 109–176–129 JIR<br />
Anti-IgD Ziege F(ab) 2 PE 2032–09 SB<br />
Anti-kappa G20–193 FITC 555791 BD<br />
Anti-lambda JDC-12 PE 555797 BD<br />
Isotypkontrolle Maus-IgG1 PE IM0670 BC<br />
BD ¼ BD Biosciences (Heidelberg, Deutschland); BC ¼ Beckman-Coulter (Krefeld, Deutschland);<br />
Dako ¼ DakoCytomation (Hamburg, Deutschland); SB ¼ SouthernBiotech (Biozol,<br />
Eching, Deutschland); JIR ¼ Jackson ImmunoResearch Laboratories (Dianova, Hamburg,<br />
Deutschland), e-bioscience ¼ Biocarta (Hamburg, Deutschland).<br />
a Die hier angegebenen Antikörper werden von den Autoren benutzt. Andere Produkte sind<br />
sicherlich alternativ verwendbar, müssen allerdings vorher selbst getestet werden.<br />
Arbeitsschritte<br />
Vollblutfärbung«KleinerLymphozytenstatus»<br />
DieProtokollezurVollblutfärbungsindunter«CharakterisierungderB-Lymphozyten»<br />
(sieheS.294)beschrieben. DieAntikö rper-Panels sindin Tabelle3dargestellt.<br />
FärbungvonPBMNCs(Klassifikation,CD40-Expression)<br />
Die Fä rbungen zum Ausschluss eines CD40-Defekts, monoklonaler Populationen<br />
und zur Klassifikation finden an PBMNCs nach Aufreinigung ü ber Ficoll-<br />
Dichtegradientenstatt.DietechnischeDurchfü hrungderFärbungenvon PBMNCs,<br />
diemittels Ficollisoliert wurden,wurde bereitsin«CharakterisierungderB-Lymphozyten»;«Arbeitschritte»(sieheS.298)beschriebenDieAntikö<br />
rpermischungen<br />
derFreiburg-Klassifikation sindin Tabelle4zusammengefasst.<br />
<strong>Diagnostik</strong> <strong>des</strong><strong>variablen</strong><strong>Immundefektsyndroms</strong> (<strong>CVID</strong>) 727
Tab.3. Antikörpermischungen fü rkleines Lymphozyten-Panel a<br />
FITC 100 m l PE 100 m l PerCP 50 m l APC 25 m l<br />
K1 CD8 CD4 CD45 CD3<br />
K2 CD19 CD56/16 b CD45 CD3<br />
a Je 15 m lder Antikörpermischung fü rdie Fä rbung von 50 m lVollblut.<br />
b Je 1:2,5 vorverdü nnt.<br />
Tab.4. Antikörpermischungen fü rFreiburg-Klassifikation a<br />
FITC 100 m l PE 100 m l PC7 25 m l FL4 25 m l<br />
B1 CD27 (1 :5) Anti-IgD (1 :40) CD19 Anti-IgM-Cy5 (1 :40)<br />
B2 CD38 CD21 CD19 Anti-IgM-Cy5 (1 :40)<br />
B3 Anti-Kappa (1 :2) Anti-Lambda (1 :2) CD19 Anti-IgM-Cy5 (1 :40)<br />
B4 CD40 ?? CD19 Anti-IgM-Cy5 (1 :40) b<br />
a Je 10 m lder Antikörpermischung fü rdie Fä rbung von 5 10 5 PBNC ¼ 50 m lZellsuspen-<br />
sion.<br />
b Nur bei Verdacht auf Hyper IgM.<br />
Tab.5. Antikörper-Panel zur Bestimmung von Aktivierung von T-Zellen a<br />
FITC PE PerCP APC<br />
A1 CD69 Isotyp G1 CD3 CD4<br />
A2 CD69 ICOS CD3 CD4<br />
A3 CD69 CD40L (CD154) CD3 CD4<br />
a Eswerden je5m lder jeweiligen Antikörper auf 0,5–1,0 10 6 Zellen gegeben.<br />
Indikationen<br />
BestimmungvonCD40L-undICOS-ExpressionaufaktiviertenTZellen/<br />
AktivierungvonT-Zellen<br />
Zur Bestimmung der ICOS-Expression werden 1 10 6 Ficoll-isolierte<br />
PBMNCs in24-Loch-Platten inRPMI 1640/10%FCS aufgenommen und fü r<br />
16– 20 hbei 37 C/5%CO2 mit bzw. ohne 1 m g/ml PHA inkubiert. Die Zellen<br />
werden anschließend in ein FACS-Rö hrchen überfü hrt, einmal inFACS-Medium<br />
gewaschen (5min, 300 g )und mit der Antikö rpermischung entsprechend <strong>des</strong><br />
Protokollsfü rPBMNCsgefärbt. Zum Nachweis derAktivierungwerdendieT-Zellenzusä<br />
tzlichmit CD69 gefärbt(Tab.5, A1 þ A2).<br />
728 Warnatz/Schlesier
Indikationen<br />
DieMethodik zumAusschlusseinesDefekts<strong>des</strong>CD40Lwirdin «Angeborene<br />
Immundefekte»; «X-chromosomales Hyper-IgM-Syndrom (XHIM)» (siehe<br />
S.711)beschrieben(Tab.5, A1 þ A3).<br />
Messung<br />
Voraussetzung fü rdie B-Zell-Messung ist eine gute Gerä teeinstellung fü rdie<br />
PhotomultiplierunddieFluorochrom-Kompensationen. Fü rgut titrierteAntikö rper<br />
istdieKompensation innerhalb<strong>des</strong>Panels einheitlich. InderRegelsinddieGerä -<br />
teeinstellungensehr stabil ü berdieZeit,so dass nicht jedeMessungmitEinzelfärbungen<br />
vorbereitet werden muss; die Gerä tekontrolle mit Beads inallen Farben<br />
reicht aus.<br />
Abb.2. Kleines Lymphozyten-Panel. a Die Lymphozytenregion (R1) wird im Fenster FL3<br />
(CD45)/SSCgesetzt. DieverschiedenenLymphozytenpopulationenwerdendurchdieExpression<br />
von CD3 (T-Zellen, unterteilt nach b CD4 þ und c CD8 þ ), d CD16þ CD56 þ CD3 – (NK-Zellen)<br />
und e CD19þ (B-Zellen) charakterisiert.<br />
<strong>Diagnostik</strong> <strong>des</strong><strong>variablen</strong><strong>Immundefektsyndroms</strong> (<strong>CVID</strong>) 729
Messung«KleinerLympozytenstatus» (Abb.2)<br />
Das Messdokument enthä lt ein zweidimensionales Aufnahmefenster mit den<br />
Achsen FL3 (CD45) und Seitwä rtsstreulicht (side scatter; SSC). Eine AnalyseregionR1definiert<br />
dieLymphozytenpopulation ü berdieExpression vonCD45 und<br />
niedrigesStreulicht.Als weitereFensterwerdendieLymphozyteninFL1vs. FL4<br />
undFL2vs. FL4dargestellt. 5000Lymphozytensolltenmin<strong>des</strong>tens aufgenommen<br />
werden.<br />
MessungzurKlassifikation von<strong>CVID</strong> (Abb.3)<br />
Das Messdokument enthä lt ein zweidimensionales Akquisitionsfenster mit<br />
den Achsen Vorwä rts- (forward scatter; FSC) und SSC. Eine Analyseregion R1<br />
definiert dieLymphozytenpopulation ü berdasStreulicht.Ein weiteresFenstermit<br />
den Achsen FL3 und FL4 enthä lt eine Region R2, die alle CD19þ B-Zellen einschließt.<br />
Alternativ kann hier auch eine Histogrammdarstellung gewä hlt werden.<br />
DieRegionenR1undR2werdenzum Aufnahme-«Gate»«B-Zellen» zusammengefasst.<br />
Ein drittes Fenster stellt FL1 gegen FL2 dar und wird auf die Darstellung<br />
der B-Zellen begrenzt (Gating). Die zu speichernden Ereignisse werden auf 5000<br />
im «Gate» «B-Zellen» und zusä tzlich auf eine Zeitbegrenzung von 5min (fü r<br />
500 m lProbenvolumen) gesetzt. Esempfiehltsich,alleZellenoderwenigstens alle<br />
Lymphozyten zuspeichern, um spä ter die Spezifitä tunerwarteter Ergebnisse an<br />
anderenZellenüberprüfenzukö nnen.<br />
MessungzurBestimmungvonICOS-undCD40L-Expressionaufaktivierten<br />
TZellen(Abb.4)<br />
Die Zellen werden zunä chst ineinem zweidimensionalem Aufnahmefenster,<br />
das bewusst größere Zellen einschließt, ü ber FSC und SSC und ein zusä tzliches<br />
«Gate» auf CD4þ Zellen definiert (cave nach Stimulation ü ber CD3 ist CD3 nur<br />
noch schwach auf der Oberflä che nachweisbar). Zum Nachweis der Aktivierung<br />
werden ineinem zweiten Fenster die CD4þ Zellen (Gate1) entsprechend ihrer<br />
Expression von CD69 (X-Achse) und CD40L bzw. ICOS (Y-Achse) dargestellt.<br />
Min<strong>des</strong>tens 5000CD4 þ Zellensolltenaufgenommenwerden.<br />
Datenanalyse<br />
Indikationen<br />
PeriphereLymphozytenpopulationen<br />
Fü rdie Auswertung <strong>des</strong> kleinen Lymphozytenstatus wird entsprechend der<br />
Abbildung2amitdenAchsenFL3(CD45)undSSC dasLymphozytenfenster(R1)<br />
gesetzt. DerAnteil anCD4-undCD8-T-Zellen(UR,Abb.2bbzw.2c),NK-Zellen<br />
(UL, Abb.2d) und B-Zellen (UL, Abb.2e) wird durch die jeweiligen Quadranten<br />
ermittelt.DieAbsolutwertewerdendurchMultiplikation derGesamtlymphozyten-<br />
730 Warnatz/Schlesier
Indikationen<br />
"/ @H8A8E8
Abb.3b.<br />
"/ @H8A8E8
Indikationen<br />
Abb.3c.<br />
"1 BJ :C:G:>
Abb.4. Nachweis einer monoklonalenPopulation. Inder Darstellungder B-Zellen (R1) im<br />
FensterIgM/CD27 fälltbereitseinedeutlicheExpansionderCD27þ IgM þ Gedächtnis-B-Zellen<br />
(UR, Quadrant 79%) auf. Im zweiten Fenster legt die massive Expansion der kappa-positiven<br />
B-Zellen (kappa:lambda 15:1) eine monoklonale Population nahe. Weitere Untersuchungen ergabenbeidiesemPatientenein<br />
Mantelzelllymphom.<br />
Tab.6. Normalwerte fü rB-Zell-Subpopulationen imperipheren Blut a<br />
B-Zell-Population Kurzbezeichnung Referenzbereich,%<br />
CD19þ in CD45þ Lymphozyten B-Zellen 4,7 – 15,0<br />
IgDþ CD27– in CD19þ B-Zellen naive und transitionale<br />
B-Zellen<br />
7,7 – 36,0<br />
IgDþ CD27þ in CD19þ B-Zellen IgM-Gedächtnis-B-Zellen 7,8–36,0<br />
IgD– CD27þ in CD19þ B-Zellen klassengewechselte<br />
Gedächtnis-B-Zellen und<br />
Plasmablasten<br />
6,5–33,0<br />
Kappa/lambda Leichtkettenverhä ltnis 1,1 – 2,0<br />
CD21– CD38 – in CD19þ B-Zellen CD21– Subpopulation 1,1 – 6,9<br />
M þþ D þþ CD38 þþ<br />
in CD19þ B-Zellen<br />
Transitional-B-Zellen 0,5–3,5<br />
M – CD38 þþ (CD27þþ)<br />
in CD19þ B-Zellen<br />
Plasmablasten 0,5–4,1<br />
a Die Referenzbereiche reprä sentieren die 5. – 95. Perzentile der B-Zell-Subpopulationen ge-<br />
sunder Erwachsener (n ¼ 28).<br />
Indikationen<br />
(z.B. Immunglobulin neg )B-Zell-Populationen oder sogar monoklonale Populationen<br />
(deutlich verschobenes Kappa-lambda-Verhä ltnis) (siehe auch «Durchflusszytometrie<br />
in der Non-Hodgkin-Lymphom-<strong>Diagnostik</strong>», S.1001). Eine weitere<br />
hä matologisch-onkologischeAbklä rungistdringendnotwendig.<br />
734 Warnatz/Schlesier
Indikationen<br />
Freiburg-Klassifikation (Abb.3)<br />
DurchFärbungB1(Abb.3a – c, Panel1)werdenüberdiedifferentielleExpression<br />
von IgM, IgD und CD27 naive (UL, CD27– IgD þ IgM þ ), IgM– (UR,<br />
CD27þ IgD þ IgM þ )und klassengewechselte (LR, CD27þ IgD – IgM – )Gedächtnis-B-Zellen<br />
unterschieden [19]. Die zweite Fä rbung B2(Abb.3a – c, Panel2)enthä<br />
lt die Marker CD21 und CD38 zur Analyse weiterer B-Zell-Differenzierungsstufen.<br />
So ist CD38 auf allen B-Zell-Vorlä ufern stark exprimiert (siehe<br />
auch «Charakterisierung der B-Lymphozyten», S.294). Naive B-Zellen zeigen<br />
eine intermediä re CD38-Oberflä chenexpression, wä hrend Gedä chtnis-B-Zellen<br />
CD38 – sind. Ûber die niedrige Expression von CD21 und CD38 (R3) wird die<br />
CD21 low B-Zell-Population abgegrenzt,diein dasSchemaderFreiburg-Klassifikation<br />
eingeht.<br />
Außerdemdefinierendiehohe IgM- undCD38-Expression dietransitionalen<br />
B-Zellen(R4)[20]unddiefehlende oderniedrige IgM-unddiehöchsteCD38-ExpressiondiePlasmablasten(R5)[21].DiesePopulation<br />
exprimiert CD27 höherals<br />
Gedächtniszellen (Abb.3c, Panel 1)und muss daher bei der Bestimmung der<br />
CD27þ klassengewechselten Gedächtniszellen von den CD27þ IgM Zellen<br />
(LR)abgezogenwerden.<br />
Befund<br />
Die Auswertung und Normwerte fü rdie B-Zell-Subpopulationen sind in Tabelle6angegeben.<br />
Dabei ist es sinnvoll, den Anteil der Gesamt-B-Zellen als Prozent<br />
der Lymphozyten und die Subpopulationen inProzent der B-Zellen anzugeben.<br />
Aus diesenAngabenkö nnengegebenenfallsauchaufLymphozytenbezogene<br />
oderabsoluteWerteberechnetwerden.<br />
Fü rdie Freiburg-Klassifikation wird zunä chst der Anteil an klassengewechselten<br />
Gedächtnis-B-Zellen an den Gesamtlymphozyten bestimmt (Abb.3,Panel1).<br />
Bei einem Anteil unter 0,4%handelt es sich umeinen Typ-1-Patienten<br />
(zirka 75%der Patienten), bei mehr als 0,4%umeinen Typ-2-Patienten (zirka<br />
25%der Patienten). Die Patienten vom Typ 1werden entsprechend dem Anteil<br />
anCD21 low B-Zellenunterteilt ineinenTyp 1a mitdeutlicherExpansion(> 20%)<br />
und einen Typ 1b mit nur geringer oder fehlender Expansion dieser Zellen<br />
(Abb.3,Panel2). Interessanter Weise treten bei Patienten mit > 20%CD21 low<br />
B-Zellen (Typ 1a) vermehrt Autoimmunphä nomene und eine Splenomegalie auf<br />
[14]. Die Auswertung dieser FACS-Panels wird gerade anhand der europä ischen<br />
Studie ü berprüft. Das Ergebnis stand zum Zeitpunkt <strong>des</strong> Redaktionsschlusses<br />
noch aus. Genauere Informationen sind ü ber Dr. K. Warnatz (Klaus.Warnatz@<br />
uniklinik-freiburg.de)<br />
<strong>Diagnostik</strong> <strong>des</strong><strong>variablen</strong><strong>Immundefektsyndroms</strong> (<strong>CVID</strong>) 735
Differentialdiagnose<strong>CVID</strong><br />
Indikationen<br />
AusschlussmonoklonalerB-Zell-Populationen<br />
Die Fä rbung B3 erlaubt Hinweise auf monoklonale B-Zell-Populationen<br />
(Abb.4). Dazu wird nach Selektion von Lymphozyten und B-Zellen die Kappagegen<br />
dieLambda-Leichtkettenexpression dargestellt. DiesesVerhä ltnissolltezirka50:50betragen.<br />
DeutlicheAbweichungenundein nachweisbarerAnteil Leichtketten-negativer<br />
B-Zellen sind nach Ausschluss von Plasmablasten (Färbung B2,<br />
R5)verdächtige Hinweisefü ratypischeB-Zell-Populationen. AbnormePopulationentretenbei<strong>CVID</strong>-PatientengelegentlichaufundsollteninZusammenarbeit<br />
mit<br />
denHämatologengenauerabgeklä rt werden.<br />
AusschlusseinesHyper-IgM-Syndroms beiCD40-Defekt<br />
HierzuwirddieExpressionvon CD40nach«Gating»aufB-Zellenuntersucht,<br />
vondenennahezu 100% positivsein sollten. DieseUntersuchungerlaubt,wiebereits<br />
erwä hnt, lediglich schwere strukturelle Defekte dieses Moleküls nachzuweisen.<br />
DasHyper-IgM-SyndromaufgrundeinesDefekts<strong>des</strong>CD40-Rezeptorsist extrem<br />
selten (< 1% der Patienten mit Hyper-IgM-Syndrom) und wurde bisher nur<br />
beiManifestation im frühenKin<strong>des</strong>alterbeschrieben. DieUntersuchungisteinfach<br />
und ohne großen Aufwand durchzufü hren. Bei keinem der von uns untersuchten<br />
<strong>CVID</strong>-Patientenkonntenwir mitHilfe dieserUntersuchungbishereineAbnormalitä<br />
tnachweisen. BeipositivemErgebnissindweiterfü hrende genetischeundfunktionelleUntersuchungenzur<br />
Diagnosesicherungnotwendig.<br />
AusschlusseinesHyper-IgM-Syndroms beiCD40L-Defekt<br />
Der Ausschluss von CD40L-Defekten ist aufwendig. Deshalb sollte dieses<br />
Verfahrennur beibegründetemVerdacht angewendetwerden,d.h.beimä nnlichen<br />
Patienten mit möglichst positiver Familienanamnese, bei denen der Serum-IgM-<br />
Wert im oberenNormbereichliegtodererhö ht ist.<br />
Dazu werden die aktivierten CD4 þ TZellen und nicht aktivierten Kontrollzellen<br />
entsprechend Abbildung 5ausgewertet. Die aktivierten Zellen exprimieren<br />
zunä chst hö here Mengen an CD69, bevor sie CD40L hochregulieren. Nicht aktivierte<br />
T-Zellen sollten CD40L – sein. Als Kontrolle müssen parallel Zellen einer<br />
gesundenKontrollestimuliert werden.<br />
AusschlusseinesICOS-Defekts<br />
Bei <strong>CVID</strong>-Patienten mit Hinweis auf eine autosomale Vererbung der Krankheit<br />
sollte ein Defekt der ICOS-Expression untersucht werden. Auch diese Untersuchung<br />
ist fü rdie Routine zu aufwendig. ICOS wird innerhalb weniger Stunden<br />
aufaktiviertenT-Zellenexprimiert undistnach16him Gegensatz zu unstimulierten<br />
Zellen gut nachzuweisen (Abb.5). Aufgrund der T-Zell-spezifischen Expres-<br />
736 Warnatz/Schlesier
Indikationen<br />
HD<br />
Pat.<br />
sion können andere Lymphozytenpopulationen als negative Kontrolle dienen. Als<br />
positive Kontrolle muss auch hier eine gesunde Person mitgefü hrt werden. Die<br />
Auswertung fü hren wir nach der Eingrenzung auf CD4þ T-Zellen analog zu der<br />
Auswertung vonCD40L durch. DieEingrenzungauf CD4þ T-Zellen ist notwendig,<br />
da die Expression <strong>des</strong> ICOS-Rezeptors auf CD4þ T-Zellen hö her als auf<br />
CD8 þ T-Zellenist.<br />
Kommentar<br />
Isotyp<br />
Anti-CD154 Anti-ICOS<br />
CD69<br />
Abb.5. Nachweis eines ICOS-Defekts. Nach Aktivierung von T-Zellen über 16hin vitro<br />
können nach «Gating» auf CD4þ T-Zellen bei Gesunden (HD) sowohl CD40L als auch ICOS<br />
deutlichaufderOberflä chenachgewiesenwerden. Als KontrollederAktivierungwirddieerhö hte<br />
Expressionvon CD69 ausgenutzt. Im Vergleich zeigt der Patient (Pat.) zwar eine nahezu normale<br />
CD40L-Expression, aberkeineICOS-Expression. Eshandelt sichhierbei um1der 9bisher<br />
identifizierten<strong>CVID</strong>-Patientenmit genetischem Defekt <strong>des</strong> ICOS [11]. Zusä tzlichsoll immer ein<br />
unstimulierterKontrollansatz mitgefü hrtwerden(hiernicht dargestellt).<br />
InunsererAbteilungwerdenroutinemä ßigdaskleineLymhozyten-Panelund<br />
das B-Zell-Panel zur Klassifikation und zum Ausschluss atypischer Populationen<br />
durchgefü hrt. Die Abgrenzung der unter «Differentialdiagnose <strong>CVID</strong>» (siehe<br />
oben) aufgefü hrtenDifferentialdiagnosenbleibtbesonderenFällenvorbehalten. Im<br />
Labor habensichdieB-Zell-FärbungenanFicoll-separiertenPBMNCsaus EDTAantikoaguliertem<br />
Material sehr bewä hrt. Einige Labors fü hren B-Zell-Färbungen<br />
<strong>Diagnostik</strong> <strong>des</strong><strong>variablen</strong><strong>Immundefektsyndroms</strong> (<strong>CVID</strong>) 737
mitgewaschenemVollblutdurch. DiesesVorgehenstellteineAlternativedar,muss<br />
abermit denentsprechendenKontrollenetabliert sein.Seit Redaktionsschlusssind<br />
neuegenetischeDefektebei<strong>CVID</strong>-Patientenidentifiziert worden(TACI,BAFF-R,<br />
CD19),diehiernicht mehr berücksichtigtwerdenkonnten.<br />
Qualitä tskontrolle<br />
NebenderKontrollederspezifischenFärbungmitHilfe vonIsotypkontrollen<br />
solltebeijederUntersuchungmöglichsteinegesunde Kontrollemitlaufen,um bei<br />
stark abweichendenSubpopulationenFärbungsfehlerauszuschließen. DieStimulationsexperimente<br />
sollten ebenfalls einerseits eine Mediumkontrolle (unstimuliert)<br />
und eine gesunde Kontrollperson enthalten. Hochpathologische Befunde sollten<br />
durcheineunabhä ngige zweiteMessungbestä tigtwerden.<br />
Troubleshooting<br />
InunseremBereichhaltenwir Auswertungenvon B-Zellenvon unter1%nur<br />
beiausreichendemAusgangsmaterialfü rverwertbar. Derartige Auswertungensind<br />
anderenfalls mit Vorsicht zu interpretieren. Unterschiedliche spezifische Antikö rper<br />
und/oder Konjugate (z.B. CD38-PE vs. CD38-APC) fü hren zuunterschiedlichenErgebnissen,diebeiderAuswertungberücksichtigtwerdenmü<br />
ssen. Hiersei<br />
insbesondere auch auf die deutlich unterschiedliche Qualitä tder Anti-ICOS-Antikörperverwiesen.<br />
DieProblemederIn-vitro-Stimulation vonT-Zellensindzahlreich.<br />
ErwarteteErgebnisse<br />
DieerwartetenErgebnissefü rdieB-Zell-Subpopulationensindin denjeweiligenAbschnittenundAbbildungenaufgefü<br />
hrt.<br />
BenötigteZeit<br />
Indikationen<br />
Die Prä paration der PBMNCs dauert etwa 1,5 h. Ebenso viel Zeit ist fü rdie<br />
Oberflä chenfärbung einzuplanen. Die T-Zell-Stimulation zum Nachweis von<br />
CD40L benötigt 0,5 ham ersten Tagzur Vorbereitung der Platten, 2ham 2.Tag<br />
zurReinigungundInkubation derPBMNCs,dienach16 – 20 hÛber-Nacht-Kultur<br />
738 Warnatz/Schlesier
Indikationen<br />
weiterverarbeitetwerdenkö nnen. Fü rdieDatenaufnahmevon2000 – 5000deruntersuchtenZellenbenötigtmanpro<br />
Färbungbis zu 5min.<br />
Zusammenfassung<br />
Das <strong>CVID</strong> ist ein heterogenes Antikö rpermangelsyndrom, das sich klinisch<br />
entweder inder Kindheit (nach dem 2.Lebensjahr) oder inder 2. – 3. LebensdekadedurchrezidivierenderespiratorischeundgastrointestinaleInfektemanifestiert.Da<br />
essichbeim <strong>CVID</strong> um eineAusschlussdiagnosehandelt,müssenbekannte<br />
genetische, infektiöse und toxische Ursachen ausgeschlossen werden. Die<br />
Diagnosekriterien sind durch die ESID ( www.esid.org )festgelegt. Die Durchflusszytometrie<br />
dient neben der Abgrenzung von X-chromosomalen und autosomal<br />
rezessiven Hyper-IgM-Syndromen (ehemalig Typ 1und 3) undder Agammaglobulinä<br />
mie (B-Zell-Zahl < 1%) inletzter Zeit zunehmend auch der Klassifikation diesesheterogenenSyndroms.DazuwerdenPatientenentsprechend<strong>des</strong>Anteilsverschiedener<br />
B-Zell-Populationen imperipheren Blut eingeteilt. Aktuell wird im<br />
Rahmen einer europä ischen Studie versucht, die Vorschlä ge aus der Freiburger<br />
und der Pariser Klassifikation zu einer einheitlichen Klassifikation zusammenzufü<br />
hren. Weitere durchflusszytometrische Analysen sind aktuell der Forschung<br />
vorbehalten.<br />
Literatur<br />
1 Pfluger H, Helbling A,Mordasini CPichler WJ: <strong>CVID</strong> (common variable immunodeficiency): Heterogene<br />
Krankheitsmanifestation dieses hä ufigsten symptomatischen primä ren Immundefekts. Schweiz<br />
MedWochenschr 2000;130:1590– 1599.<br />
2 Spickett GP: Current perspectives oncommon variable immunodeficiency (<strong>CVID</strong>). Clin Exp Allergy<br />
2001;31:536– 542.<br />
3 Rump JA, Jakschiess D, Walker U, Schlesier M, von Wussow P, Peter HH: Common variable<br />
immunodeficiency (<strong>CVID</strong>) and MxA-protein expression in blood leucocytes. Clin Exp Immunol<br />
1995;101:89 – 93.<br />
4 Vorechovsky I, Zetterquist H, Paganelli R, Koskinen S, Webster AD, Bjorkander J, Smith CI, Hammarstrom<br />
L: Family and linkage study ofselective IgA deficiency and commonvariable immunodeficiency.<br />
ClinImmunol Immunopathol 1995;77:185– 192.<br />
5 Cunningham-Rundles C, Bodian C: Common variable immunodeficiency: clinical and immunological<br />
featuresof248 patients. ClinImmunol 1999;92:34 – 48.<br />
6 Thon V, Wolf HM, Sasgary M, Litzman J, Samstag A, Hauber I, Lokaj J, Eibl MM: Defective integration<br />
of activating signals derived from the Tcell receptor (TCR) and costimulatory molecules inboth<br />
CD4 þ and CD8þ Tlymphocytes ofcommon variable immunodeficiency (<strong>CVID</strong>) patients. Clin Exp<br />
Immunol 1997;110:174 – 181.<br />
7 DiRenzoM, Serrano D, Zhou Z, George I, BeckerK, Cunningham-RundlesC: EnhancedTcell apoptosis<br />
incommon variable immunodeficiency: negative role of the fas/fasligand system and of the Bcl-2<br />
family proteinsandpossibleroleofTNF-RS.ClinExp Immunol 2001;125:117 – 122.<br />
8 Groth C, DragerR, Warnatz K, Wolff-Vorbeck G, Schmidt S, Eibel H, Schlesier M, Peter HH: Impaired<br />
up-regulation of CD70 and CD86 innaive (CD27– )Bcells from patients with commonvariable immunodeficiency(<strong>CVID</strong>).<br />
ClinExp Immunol 2002;129:133 – 139.<br />
<strong>Diagnostik</strong> <strong>des</strong><strong>variablen</strong><strong>Immundefektsyndroms</strong> (<strong>CVID</strong>) 739
Indikationen<br />
9 Kanegane H,Tsukada S,Iwata T,Futatani T, Nomura K,Yamamoto J, Yoshida T, Agematsu K, Komiyama<br />
A,Miyawaki T: Detection of Bruton’s tyrosine kinase mutations inhypogammaglobulinaemic<br />
males registered as commonvariable immunodeficiency (<strong>CVID</strong>) inthe Japanese Immunodeficiency Registry.<br />
ClinExp Immunol 2000;120:512– 517.<br />
10 Durandy A, Revy P, Fischer A: Human models ofinherited immunoglobulin class switchrecombination<br />
andsomatichypermutation defects (hyper-IgMsyndromes).AdvImmunol 2004;82:295 – 330.<br />
11 Grimbacher B, Hutloff A, Schlesier M, Glocker E, Warnatz K, Drager R, Eibel H, Fischer B, Schaffer<br />
AA, Mages HW, Kroczek RA, Peter HH: Homozygous loss ofICOS is associated with adult-onset<br />
commonvariableimmunodeficiency. NatImmunol 2003;4:261 – 268.<br />
12 Hutloff A, Dittrich AM, Beier KC, Eljaschewitsch B, Kraft R, Anagnostopoulos I, Kroczek RA: ICOS<br />
is an inducible T-cell co-stimulator structurally and functionally related to CD28. Nature<br />
1999;397:263 – 266.<br />
13 Engel P, Eck MJ, Terhorst C: The SAP and SLAM families inimmuneresponses and X-linked lymphoproliferativedisease.NatRevImmunol<br />
2003;3:813– 821.<br />
14 Warnatz K, Denz A, Drager R, Braun M, Groth C, Wolff-Vorbeck G, Eibel H, Schlesier M, Peter HH:<br />
Severe deficiency ofswitched memory Bcells (CD27þ IgM IgD )insubgroups ofpatients with<br />
common variable immunodeficiency: a new approach to classify a heterogeneous disease. Blood<br />
2002;99:1544 – 1551.<br />
15 PiquerasB, Lavenu-Bombled C, GalicierL, Bergeron-vanderCruyssenF, Mouthon L, ChevretS, Debre<br />
P, Schmitt C, Oksenhendler E: Common variable immunodeficiency patient classification based on impaired<br />
Bcell memory differentiation correlateswithclinicalaspects.JClinImmunol 2003;23:385– 400.<br />
16 Aukrust P, Lien E, Kristoffersen AK, Muller F, Haug CJ, Espevik T, Froland SS: Persistent activation of<br />
the tumor necrosis factor system inasubgroup of patients with common variable immunodeficiency –<br />
possibleimmunologicandclinicalconsequences. Blood1996;87:674 – 681.<br />
17 Bryant A, Calver NC, Toubi E, Webster AD, Farrant J: Classification of patients with commonvariable<br />
immunodeficiency by Bcell secretion of IgM and IgG in response to anti-IgM and interleukin-2. Clin<br />
Immunol Immunopathol 1990;56:239 – 248.<br />
18 Ferry BL, Jones J, Bateman EA, Woodham N, Warnatz K, Schlesier M, Misbah SA, Peter HH, Chapel<br />
HM: Measurement of peripheral Bcell subpopulations incommon variable immunodeficiency (<strong>CVID</strong>)<br />
usingawholebloodmethod.Clin. Exp Immunol 2005;140:532– 539.<br />
19 Klein U, Kuppers R, Rajewsky K: Evidence for alarge compartment ofIgM-expressing memory Bcells<br />
in humans.Blood1997;89:1288– 1298.<br />
20 Carsetti R, Rosado MM, Wardmann H: Peripheral development of Bcells inmouse and man. Immunol<br />
Rev2004;197:179 – 191.<br />
21 Odendahl M, Jacobi A, Hansen A, Feist E, Hiepe F,Burmester GR, Lipsky PE, Radbruch A, Dorner T:<br />
Disturbed peripheral B lymphocyte homeostasis in systemic lupus erythematosus. J Immunol<br />
2000;165:5970 – 5979.<br />
740 Warnatz/Schlesier