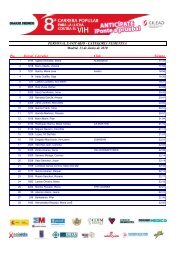
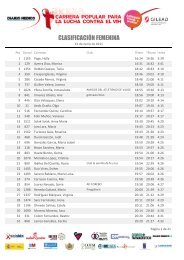
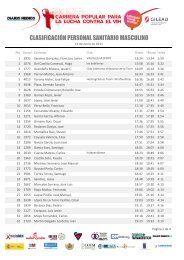
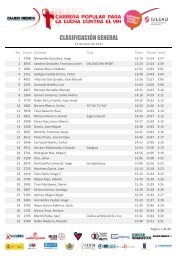
CF 17 al 23 mayo de 2010 Nª412 - Diario Médico
CF 17 al 23 mayo de 2010 Nª412 - Diario Médico
CF 17 al 23 mayo de 2010 Nª412 - Diario Médico
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
CORREO FARMACÉUTICO SEMANA DEL <strong>17</strong> AL <strong>23</strong> DE MAYO DE <strong>2010</strong>´FARMACOLOGIA21EMPRESASPfizeradquiere unmedicamentoen fase II paraHTA pulmonar<strong>CF</strong>. Pfizer y Ergonex hananunciado un acuerdopor el que la primera adquiriráterguri<strong>de</strong>, untratamiento potenci<strong>al</strong><strong>de</strong> la hipertensión arteri<strong>al</strong>pulmonar (HAP) enfase II. Pfizer apoyará lafinanciación <strong>de</strong>l estudioclínico <strong>de</strong> terguri<strong>de</strong>, unantagonista or<strong>al</strong> <strong>de</strong> losreceptores <strong>de</strong> la serotonina5-HT2B y 5-HT2A,que ha recibido la <strong>de</strong>signación<strong>de</strong> huérfano en laUnión Europea y en EstadosUnidos. Pfizer obtendrí<strong>al</strong>os <strong>de</strong>rechosmundi<strong>al</strong>es en exclusiva<strong>de</strong> comerci<strong>al</strong>ización, exceptoJapón, y Ergonextendrá <strong>de</strong>recho a recibirpagos puntu<strong>al</strong>es por objetivos.La nueva empresa, cuya se<strong>de</strong> estará en V<strong>al</strong>ladolid, <strong>de</strong>sarrollará tresmoléculas y una potenci<strong>al</strong> vacuna terapéutica contra la enfermedadDigna crea una compañíacentrada en hepatitis C<strong>CF</strong>correofarmaceutico@correofarmaceutico.comLa biotecnológica navarraDigna Biotech y el fondo <strong>de</strong>capit<strong>al</strong> riesgo Seguranza,promovido por la Consejería<strong>de</strong> Economía y Empleo<strong>de</strong> la Junta <strong>de</strong> Castilla yLeón, anunciaron la semanapasada la creación <strong>de</strong> laempresa HepaCyL Therapeutics,que se centrará enel <strong>de</strong>sarrollo <strong>de</strong> tratamientoscontra la hepatitis C.HepaCyl (cuyo nombre esun acrónimo Hepatitis yCastilla y León) se encargará<strong>de</strong> <strong>de</strong>sarrollar cuatro patentes<strong>de</strong> tratamientos potenci<strong>al</strong>escontra la hepatitisC <strong>de</strong> Digna Biotech. Setrata <strong>de</strong> oncostatina M asociadaa interferón; el interAPO,una molécula que resulta<strong>de</strong> la fusión <strong>de</strong>l interferón<strong>al</strong>fa-5 y la apoproteínaA1; el péptido P60, queinhibe un mecanismo clavepara activar la respuestainmune <strong>al</strong>terada con lahepatitis C, y un prototipo<strong>de</strong> vacuna terapéutica contr<strong>al</strong>a enfermedad.MERCADO PROMETEDORSegún explicó Pablo Ortiz,director gener<strong>al</strong> <strong>de</strong> DignaBiotech, cuando se hizo públicoel acuerdo, la hepatitisC ofrece buenas opcionesterapéuticas y <strong>de</strong> mercado:“En la actu<strong>al</strong>idad, seestima que esta enfermedadafecta a un 3 por ciento<strong>de</strong> la población mundi<strong>al</strong> ytiene un mercado <strong>de</strong> 2.500millones <strong>de</strong> euros, con uncrecimiento <strong>mayo</strong>r a un 20por ciento anu<strong>al</strong>”.A<strong>de</strong>más, la creación <strong>de</strong>HepaCyl, cuya se<strong>de</strong> estaráen V<strong>al</strong>ladolid, también reportaríabeneficios a la región:“HepaCyl constituye elfruto <strong>de</strong> muchos meses <strong>de</strong>trabajo conjunto, y abre laposibilidad <strong>de</strong> implantaruna empresa lí<strong>de</strong>r en biotecnologíaen la Comunidad<strong>de</strong> Castilla y León”, afirmóRicardo Pérez Merino, subdirectorgener<strong>al</strong> <strong>de</strong> ClaveMayor, la empresa que hagestionado la operación.HepaCyL nace con un capit<strong>al</strong><strong>de</strong> 10 millones <strong>de</strong> euros.Está participada porSeguranza, por la propiaDigna Biotech y por inversoresparticulares.Digna Biotech nació en elaño 2003. Des<strong>de</strong> entonces,<strong>de</strong>sarrolla los productos investigadospor el Centro <strong>de</strong>Investigación Médica Aplicada(CIMA), un organismo<strong>de</strong>pendiente <strong>de</strong> la Universidad<strong>de</strong> Navarra.ESCAPARATE‘Misulmylan’, nuevo antipsicótico atípico <strong>de</strong> MylanPharmaceutic<strong>al</strong>s, indicado para el tratamiento <strong>de</strong> la esquizofreniaM i s u lmyl a n(amisulprida)es el nuevo lanzamiento<strong>de</strong>Mylan <strong>de</strong>ntro<strong>de</strong>l área <strong>de</strong>l sistema nervioso centr<strong>al</strong>. Se trata <strong>de</strong> un potenteantipsicótico atípico indicado para el tratamientocontra la esquizofrenia, con afinidad a los subtiposD2 / D3 <strong>de</strong>l receptor dopaminérgico humano, y quecarece <strong>de</strong> afinidad por los subtipos D1, D4 y D5 <strong>de</strong>lreceptor. Presenta una escasa ten<strong>de</strong>ncia a producirefectos secundarios extrapiramid<strong>al</strong>es, que pue<strong>de</strong> estarrelacionada con su actividad límbica preferenci<strong>al</strong>.Misulmylan se comerci<strong>al</strong>iza en presentaciones <strong>de</strong> comprimidos<strong>de</strong> 100, 200 y 400 mg.Novartis comerci<strong>al</strong>iza ‘Pantoloc Control’, nuevo medicamento sinreceta para el tratamiento <strong>de</strong>l ardorNovartis anuncia el lanzamiento <strong>de</strong> Pantoloc Control(pantoprazol), un nuevo medicamento sin receta parael tratamiento <strong>de</strong>l ardor, queafecta a 13,6 millones <strong>de</strong> personasen España. Pantoprazol,un inhibidor <strong>de</strong> la bomba<strong>de</strong> protones (IBP), constituyela primera molécula <strong>de</strong> sufamilia en obtener la aprobación<strong>de</strong> la agencia europeaEMA para su comerci<strong>al</strong>izacióncomo OTC. Con un único comprimido <strong>al</strong> día, PantolocControl <strong>al</strong>ivia los síntomas <strong>de</strong>l reflujo (por ejemplo, laregurgitación o el ardor), y está clínicamente <strong>de</strong>mostradoque el producto tiene un menor potenci<strong>al</strong> <strong>de</strong> interaccióncon otros fármacos que otros IBP.