You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
GENETIQUE DE LA LEVURE
• But: Détermination du rôle et <strong>de</strong> <strong>la</strong> régu<strong>la</strong>tion <strong>de</strong> chaque<br />
gène et produit <strong>de</strong> gène<br />
• Pour ceci, <strong>de</strong> nombreuses approches ont été développées<br />
<strong>de</strong>puis 30 ans<br />
• Aux analyses c<strong>la</strong>ssiques d’étu<strong>de</strong> d’un mécanisme donné par<br />
différentes approches (cribles génétiques, analyse <strong>de</strong> mutants,<br />
biochimie, biologie cellu<strong>la</strong>ire et molécu<strong>la</strong>ire...), s’est ajouté <strong>de</strong><br />
nombreux programmes d’analyses systématiques: délétion<br />
systématique <strong>de</strong> tous les gènes, coup<strong>la</strong>ge à <strong>de</strong>s marqueurs<br />
fluorescent (GFP), analyse globale <strong>de</strong> <strong>la</strong> transcription <strong>de</strong>s<br />
gènes, analyse globale <strong>de</strong>s interactions protéines-protéines....
I. Souches et marqueurs<br />
• Les marqueurs génétiques sont utilisés pour suivre une<br />
mutation lors <strong>de</strong> croisement <strong>de</strong> souches ou pour<br />
sélectioner les cellules ayant inégré un p<strong>la</strong>smi<strong>de</strong>.<br />
• Ce sont pour <strong>la</strong> plupart <strong>de</strong>s marqueurs d’auxotrophie:<br />
HIS3, URA3, TRP1, LEU2, LYS2, ADE2<br />
• Comme chez E. coli certains gènes <strong>de</strong> résistance aux<br />
antibiotiques peuvent être utilisés: kanamycin resistance,<br />
kanR<br />
• Il existe plusieurs souches <strong>de</strong> <strong>la</strong>boratoire dont les<br />
propriétés peuvent varier:<br />
W303-1A, S288C, S1278b, SK1, BY4741....<br />
• le génotype d’une souche se présente ainsi:<br />
W303-1A: MATa leu2-3/112 ura3-1 trp1-1 his3-11/15<br />
a<strong>de</strong>2-1
MATa leu2-3/112 ura3-1 trp1-1 his3-11/15 a<strong>de</strong>2-1<br />
• Un mutant d’auxotrophie ne poussera pas sur milieu<br />
minimum si tous les nutriments qui lui sont essentiels ne<br />
sont pas fournis <strong>de</strong> façon exogène:<br />
• Un mutant ura3 ne peut pas pousser sur milieu minimum<br />
sans uracile<br />
Par contre le même mutant poussera sur milieu minimum<br />
sans uracile si on introduit un p<strong>la</strong>smi<strong>de</strong> portant le gène<br />
sauvage URA3.
• La génétique <strong>de</strong> <strong>la</strong> levure est basée sur <strong>la</strong> possiblité <strong>de</strong> croiser <strong>de</strong>ux souches haploï<strong>de</strong>s<br />
portant <strong>de</strong>s mutations différentes pour former une souche diploï<strong>de</strong>.<br />
• Le diploï<strong>de</strong> peut alors être induit à sporuler pour former une tétra<strong>de</strong>. Les tétra<strong>de</strong>s peuvent<br />
ensuite être disséquées avec un micromanipu<strong>la</strong>teur. Les spores isolées formeront chacune<br />
une colonie.<br />
• Par le passé, ces croisements génétiques ont permis d’établir les cartes chromosomiques<br />
en utilisant <strong>la</strong> fréquence <strong>de</strong> recombinaison entre <strong>de</strong>ux mutations comme mesure <strong>de</strong> <strong>la</strong><br />
distance génétique.<br />
• Aujourd’hui les croisements sont utilisés pour générer <strong>de</strong>s souches avec <strong>de</strong> nouvelles<br />
combinaison <strong>de</strong> mutations et pour analyser les re<strong>la</strong>tions génétiques entre différentes<br />
mutations.
• expl: MATa leu2 URA3 x MATalpha LEU2 ura3<br />
• le diploï<strong>de</strong> est hétérozygote pour les marqueurs URA3 et<br />
LEU2 et peut être selectionné sur milieu minimum sans<br />
leucine et uracile.<br />
• sporu<strong>la</strong>tion sur milieu carencé en azote<br />
• La paroi <strong>de</strong> <strong>la</strong> tétra<strong>de</strong> est digérée et les spores séparés<br />
avec un micromanipu<strong>la</strong>teur.<br />
• Les spores vont germer et chaque spore donner une<br />
colonie qui peut être analysée individuellement.<br />
• Ce qui veut dire que le produit <strong>de</strong> <strong>la</strong> méiose peut être<br />
analysé directement.<br />
• La taille <strong>de</strong>s colonies issues <strong>de</strong> chaque spore peut déja<br />
donner une indication <strong>de</strong> l’effet d’une double mutation<br />
sur <strong>la</strong> croissance<br />
• Sinon, les colonies sont répliquées sur différents<br />
milieux afin <strong>de</strong> caractériser leurs propriétés et <strong>de</strong> suivre<br />
les marqueurs génétiques.
II. Production <strong>de</strong> mutants<br />
• Les mutations qui augmentent ou diminuent <strong>la</strong> fonction<br />
du produit d’un gène sont extrèmement utiles pour<br />
étudier un système cellu<strong>la</strong>ire. L’étu<strong>de</strong> <strong>de</strong> l’effet <strong>de</strong> <strong>la</strong><br />
mutation (phénotype) donne <strong>de</strong>s indications sur <strong>la</strong><br />
protéine elle-même et sur <strong>la</strong> voie dans <strong>la</strong>quelle elle agit.<br />
• Mutation au hasard ou mutation ciblée<br />
- La mutagénèse au hasard (par <strong>de</strong>s agents<br />
mutagènes) a pour but <strong>de</strong> lier une fonction à un ou<br />
plusieurs gènes. En général, on cible le génome dans<br />
son entier.<br />
- La mutagénèse au hasard peut aussi se faire in<br />
vitro sur un gène donné (porté par un p<strong>la</strong>smi<strong>de</strong>). Le<br />
but est alors d’i<strong>de</strong>ntifier les domaines fonctionnels<br />
d’une protéine.<br />
- dans <strong>la</strong> mutagénèse ciblée, un gène est<br />
spécifiquement inactivé ou altéré par une<br />
combinaison <strong>de</strong> manipu<strong>la</strong>tions in vitro et in vivo.
A. Sélection et crib<strong>la</strong>ge <strong>de</strong>s mutants<br />
– Une mutagénèse au hasard aboutit à une popu<strong>la</strong>tion<br />
hétérogène portant différents type d’allèles mutés. On veut<br />
tester chaque clone pour chercher <strong>la</strong> ou les mutations<br />
d’intérêt.<br />
– Pour ceci, on va établir <strong>de</strong>s conditions dans lesquelles <strong>la</strong><br />
mutation rechercher va donner soit un avantage <strong>de</strong> croissance<br />
(crible positif) ou être délétère (crible négatif)<br />
– premier challenge intellectuel: penser <strong>de</strong>s conditions <strong>de</strong><br />
croissance ou <strong>de</strong> souche , où seul le mutant recherché va<br />
pousser/ou ne pas pousser: un bon exemple est le crib<strong>la</strong>ge basé<br />
sur une résistance à un inhibiteur.<br />
– <strong>de</strong>uxième challenge intellectuel: penser <strong>de</strong>s conditions <strong>de</strong><br />
crib<strong>la</strong>ge qui permettent d’isoler le mutant d’intérêt tout en<br />
éliminant tout ceux qui pourraient donner le même phénotype<br />
par une voie détournée.<br />
Wild type<br />
hog1D<br />
sko1D<br />
aca1D aca2D<br />
hog1D sko1D<br />
hog1D aca1D<br />
aca2D<br />
hog1D sko1D<br />
aca1D aca2D<br />
Wild type<br />
aca2D<br />
hog1D<br />
hog1D aca2D<br />
YPD YPD + 0.4M NaCl<br />
YPD YPD + 0.4M NaCl
• Une fois que le clone portant <strong>la</strong> mutation a été isolé, <strong>la</strong> mutation doit être<br />
caractérisée et le gène portant <strong>la</strong> mutation i<strong>de</strong>ntifié.<br />
• Pour ceci, on réalise:<br />
B. Caractérisation <strong>de</strong>s mutants<br />
- une étu<strong>de</strong> phénotypique détaillée avec d’éventuels cribles secondaires<br />
- on détermine le caractère dominant ou récessif <strong>de</strong> <strong>la</strong> mutation<br />
- on vérifie le nombre <strong>de</strong> mutations liées au phénotype (ségrégation 2/2 <strong>de</strong> <strong>la</strong><br />
mutation après croisement avec <strong>la</strong> souche parentale)<br />
- on catégorise les mutants par groupes <strong>de</strong> complémentation.<br />
- on clone le gène portant <strong>la</strong> mutation
Les mutations dominantes et récessives<br />
La souche mutée est re-croisée avec <strong>la</strong><br />
souche parentale sauvage pour former<br />
un diploï<strong>de</strong> hétérozygote pour <strong>la</strong><br />
mutation concernée<br />
Recessive: wild type phenotype<br />
MUT1<br />
MUT1<br />
mut1<br />
mut1<br />
Dominant: mutant phenotype
• Le caractère dominant peut avoir plusieurs<br />
sources:<br />
– une mutation créant un gain <strong>de</strong><br />
fonction: par expl une protéine<br />
régu<strong>la</strong>trice fonctionnant sans son<br />
stimulus physiologique<br />
– Le produit du gène fonctionne sous<br />
forme oligomérique et l’introduction<br />
d’un monomère muté abolit <strong>la</strong> fonction<br />
<strong>de</strong> l’oligomère<br />
– <strong>la</strong> quantité <strong>de</strong> protéine produite à<br />
partir d’un allèle sauvage n’est pas<br />
suffisante pour assurer <strong>la</strong> fonction<br />
• Le caractère récessif est le plus souvent lié à<br />
une perte <strong>de</strong> fonction du produit. Ce sont les<br />
plus fréquentes.<br />
Recessive: wild type phenotype<br />
MUT1<br />
MUT1<br />
mut1<br />
mut1<br />
Dominant: mutant phenotype
Détermination <strong>de</strong>s groupes <strong>de</strong><br />
complémentation<br />
But: déterminer si les mutations isolées<br />
affectent le même gène.<br />
• Pour les mutations récessives, les clones mutants<br />
sont croisés entre eux dans toutes les<br />
combinaisons possibles.<br />
- Si les <strong>de</strong>ux mutations sont dans le même<br />
gène, <strong>la</strong> souche dipoï<strong>de</strong> aura le même phénotype<br />
mutant que les haploï<strong>de</strong>s<br />
- Si les <strong>de</strong>ux mutations sont dans <strong>de</strong>ux<br />
gènes différents, le diploï<strong>de</strong> <strong>de</strong>vrait avoir un<br />
phénotype sauvage car chaque haploï<strong>de</strong><br />
apporte une copie sauvage <strong>de</strong> l’autre gène.<br />
mut1<br />
mut1<br />
mut1<br />
mut1<br />
MUT1<br />
MUT1<br />
mut1<br />
mut1<br />
No functional gene product<br />
of MUT1<br />
mut2<br />
mut2<br />
MUT2<br />
MUT2<br />
Functional gene products<br />
of MUT1 and MUT2
La complémentation intragènique<br />
w Le croisement <strong>de</strong> <strong>de</strong>ux mutations<br />
récessives donne un phénotype<br />
intermédiaire ou sauvage au<br />
diploï<strong>de</strong> hétérozygote.<br />
w Pourquoi? Les <strong>de</strong>ux mutations<br />
portent sur le même gène mais les<br />
<strong>de</strong>ux produits mutés bien que non<br />
fonctionnels peuvent former un<br />
hétéromère plus ou moins<br />
fonctionnel.<br />
mut1-1<br />
mut1-1<br />
mut1-2<br />
mut1-2<br />
No functional gene product<br />
of MUT1<br />
But a heteromere consisting of<br />
Mut1-1p and Mut1-2p can be functional
I<strong>de</strong>ntifier le gène muté<br />
-dans le cas d’une mutation dominante: il faut construire 1) une banque d’ADN génomique<br />
à partir <strong>de</strong> chaque souche mutante, 2) transformer une souche sauvage et 3) cribler pour<br />
le phénotype attendu. Réisoler le p<strong>la</strong>smi<strong>de</strong> d’intérêt et le séquencer.<br />
-dans le cas d’une mutation récessive: clonage par complémentation qui consiste à<br />
transformer <strong>la</strong> souche mutée avec une banque génomique et sélectionner les clones qui<br />
ont perdu le phénotype mutant. le p<strong>la</strong>smi<strong>de</strong>s est alors ré-isolé puis séquencé.<br />
Attention: le gène isolé par cette approche peut être un suppresseur multicopie.<br />
Il faut donc vérifier que <strong>la</strong> délétion <strong>de</strong> ce gène provoque le même<br />
phénotype que <strong>la</strong> mutation d’origine. La mutation et <strong>la</strong> délétion doivent<br />
aussi appartenir au même groupe <strong>de</strong> complémentation.
III Cloner les gènes chez <strong>la</strong> levure<br />
- Les premières transformations <strong>de</strong> <strong>la</strong> levure par <strong>de</strong> l’ADN étranger datent <strong>de</strong> 1978<br />
- Les levures peuvent maintenir <strong>de</strong>s p<strong>la</strong>smi<strong>de</strong>s extra-chromosomiques<br />
- Les protocoles <strong>de</strong> transformation sont aussi simples mais moins<br />
efficaces que chez E. coli<br />
-Les préparations <strong>de</strong> p<strong>la</strong>smi<strong>de</strong>s à partir <strong>de</strong> <strong>la</strong> levure sont très peu efficaces:<br />
- On utilise donc <strong>de</strong>s vecteurs navettes capables <strong>de</strong> se répliquer et<br />
<strong>de</strong> se maintenir à <strong>la</strong> fois chez E. coli et chez <strong>la</strong> levure<br />
-les p<strong>la</strong>smi<strong>de</strong>s sont construits in vitro<br />
-transformés, sélectionnés et amplifiés chez <strong>la</strong> bactérie.<br />
-transformés dans <strong>la</strong> levure.
Les vecteurs navettes<br />
Ils sont <strong>de</strong> trois type: intégratifs, centromériques ou épisomales<br />
les vecteurs intégratifs (YIp):<br />
Amp-resistance<br />
- Ce sont <strong>de</strong>s vecteurs d’E. coli type pBR322,<br />
contenant un marqueur <strong>de</strong> sélection <strong>de</strong> levure.<br />
- Ils ne contiennent pas d’origine <strong>de</strong><br />
réplication chez <strong>la</strong> levure.<br />
-Ils doivent donc s’intégrer dans le génome<br />
<strong>de</strong> <strong>la</strong> levure pour être propagés.<br />
Pst I (4795)<br />
Apa LI (3971)<br />
Apa LI (5217)<br />
PMB1<br />
Apa LI (3473)<br />
YIp5: pBR322 plus the URA3 gene<br />
EcoR I (2)<br />
C<strong>la</strong> I (28)<br />
YIp5<br />
5541bp<br />
Hind III (33)<br />
BamH I (379)<br />
URA3<br />
Ava I (2541)<br />
Xma I (2541)<br />
Sma I (2543)<br />
Tet-resistance<br />
Pst I (1644)<br />
Nco I (1867)
L’intégration se fait par recombinaison homologue.<br />
Elle est favorisée par <strong>la</strong> linéarisation du vecteur<br />
X<br />
ura3<br />
X<br />
p<strong>la</strong>smid<br />
URA3<br />
ura3<br />
URA3<br />
genome<br />
genome
Replicative episomal p<strong>la</strong>smids (YEp):<br />
-Ce sont <strong>de</strong>s vecteurs d’E. coli type<br />
pBR322, contenant un marqueur <strong>de</strong><br />
sélection <strong>de</strong> levure.<br />
-Ils contiennent l’origine <strong>de</strong><br />
réplication du vecteur 2m <strong>de</strong> levure<br />
-Ils sont propagés <strong>de</strong> façon stable<br />
avec 20 à 50 copies/cellule.<br />
PMB1<br />
Apa LI (5701)<br />
Apa LI (7445)<br />
Amp-resistance<br />
Apa LI (6199)<br />
Pst I (7023)<br />
Ava I (4835)<br />
Tet-resistance<br />
YEp24: pBR322 plus the URA3 gene, plus 2micron origin<br />
EcoR I (2)<br />
YEp24<br />
7769bp<br />
BamH I (3785)<br />
Hind III (106)<br />
URA3<br />
Xma I (3379)<br />
Ava I (3379)<br />
Sma I (3381)<br />
Hind III (3439)<br />
2micron ORI<br />
Ava I (1391)<br />
Pst I (2001)<br />
EcoR I (2242)<br />
C<strong>la</strong> I (2268)<br />
Hind III (2273)<br />
Pst I (2482)<br />
Nco I (2705)
p<strong>la</strong>smi<strong>de</strong>s centromériques (Ycp):<br />
-Ce sont <strong>de</strong>s vecteurs d’E. coli type<br />
pBR322, contenant un marqueur <strong>de</strong><br />
sélection <strong>de</strong> levure.<br />
-Ils contiennent une origine <strong>de</strong><br />
réplication chromosomique<br />
ARS (autonomously<br />
Replicating Sequence)<br />
et le centromère CEN<br />
<strong>de</strong>s chromosomes <strong>de</strong> levure<br />
-Ils sont propagés avec un<br />
faible nombre <strong>de</strong> copies (1).<br />
Amp-resistance<br />
Apa LI (6380)<br />
PMB1<br />
Apa LI (5882)<br />
Apa LI (5457)<br />
Pst I (5451)<br />
Pst I (7204)<br />
ARS1<br />
Ava I (4703)<br />
Apa LI (7626)<br />
CEN4<br />
YCp50: pBR322 plus the URA3 gene, plus CEN4, plus ARS1<br />
EcoR I (2)<br />
C<strong>la</strong> I (28)<br />
YCp50<br />
7950bp<br />
Hind III (33)<br />
BamH I (379)<br />
Tet-resistance<br />
POLY<br />
Pst I (1644)<br />
Nco I (1867)<br />
URA3<br />
Xma I (2541)<br />
Ava I (2541)<br />
Sma I (2543)<br />
POLY
Utilisation <strong>de</strong>s vecteurs<br />
utilisés pour exprimer un gène sauvage ou muté sous le contrôle<br />
<strong>de</strong> son propre promoteur ou d’un promoteur exogène inductible<br />
(GAL1, MET3) ou non (ADH, GAP....)<br />
-Le promoteur GAL1 est réprimé en présence <strong>de</strong> glucose<br />
dans le milieu et induit en présence <strong>de</strong> ga<strong>la</strong>ctose.<br />
-Le promoteur MET3 est réprimé en présence <strong>de</strong> méthionine<br />
et induit en absence <strong>de</strong> méthionine
1. construction du vecteur<br />
in vitro<br />
Déléter un gène<br />
YFG1<br />
URA3<br />
Your favourite gene on a p<strong>la</strong>smid<br />
Your favourite gene on a p<strong>la</strong>smid,<br />
ORF rep<strong>la</strong>ced by marker<br />
2. introduction chez <strong>la</strong> levure et intégration dans le génome<br />
par recombinaison<br />
in vivo<br />
URA3<br />
X X<br />
URA3<br />
Recombination in yeast<br />
Your favourite gene <strong>de</strong>leted<br />
from the genome
<strong>la</strong> même approche peut être utilisée avec un fragment PCR<br />
double recombinaison<br />
vérification par PCR<br />
A<br />
PCR et transformation<br />
URA3<br />
X 5’ URA3<br />
X 3’<br />
L’oligonucléoti<strong>de</strong> A contient les 40 bases en<br />
amont <strong>de</strong> l’ATG du gène X<br />
L’oligonucléoti<strong>de</strong> B contient les 40 bases en<br />
aval du codon stop du gène X<br />
B<br />
X chromosome<br />
X 5’ X 3’<br />
ATG<br />
STOP<br />
X 5’ URA3<br />
X 3’<br />
Caviston et al. MBC 2003
Introduire une étiquette (tag)<br />
A<br />
double recombinaison<br />
tag<br />
PCR et transformation<br />
ATG<br />
ATG<br />
URA3<br />
X 5’<br />
X<br />
tag URA3 X 3’<br />
STOP<br />
X tag URA3<br />
L’oligonucléoti<strong>de</strong> A contient les 40 bases en<br />
amont du codon stop du gène X, en phase<br />
avec <strong>la</strong> séquence du tag<br />
L’oligonucléoti<strong>de</strong> B contient les 40 bases en<br />
Baval<br />
du codon stop du gène X<br />
Gulli et al. Mol Cell 2000
Potentialités et limites <strong>de</strong> <strong>la</strong> modification <strong>de</strong>s gènes<br />
par introduction d’une cassette PCR<br />
Potentialités: - déléter n’importe quelle ORF<br />
- étiqueter n’importe quelle protéine à son<br />
extrémité C-terminale<br />
- créer <strong>de</strong>s formes tronquées en C-ter avec ou<br />
sans étiquette<br />
Limitations: - avoir <strong>la</strong> possibilité <strong>de</strong> vérifier que l’addition d’une<br />
étiquette ne modifie pas <strong>la</strong> fonction <strong>de</strong> <strong>la</strong> protéine<br />
- Risque d’introduire une autre cassette ailleurs dans le<br />
génome
Introduire une mutation au locus d’un gène<br />
Cette technique est basée sur le fait qu’on peut contre-sélectionner le<br />
marqueur URA3 en présence d’aci<strong>de</strong> 5-fluoro-orotique (FOA)<br />
-URA3 co<strong>de</strong> pour l’oritidine5’-phosphate <strong>de</strong>carboxy<strong>la</strong>se, enzyme<br />
impliquée dans <strong>la</strong> synthèse <strong>de</strong> l’uracile<br />
-l’aci<strong>de</strong> 5-fluoroorotic (5-FOA) est converti par Ura3 en 5-fluorouracil,<br />
toxique pour <strong>la</strong> cellule<br />
-les cellules URA3 + sont donc tuées en présence <strong>de</strong> 5-FOA tandis que les<br />
cellules ura3 sont résistantes.
souche ∆x<br />
transformation avec un fragment<br />
d’ADN modifié in vitro<br />
survivants<br />
X 5’ URA3<br />
X 3’<br />
mut<br />
X 5’ X<br />
X 3’<br />
étalement sur boites contenant du FOA<br />
mut<br />
X 5’ X 3’<br />
URA3 X<br />
vérifications à faire: - introduction <strong>de</strong> <strong>la</strong> cassette au locus désiré<br />
- présence <strong>de</strong> <strong>la</strong> mutation
IV Que faire avec les gènes essentiels?<br />
• environ 1/3 <strong>de</strong>s gènes sont essentiels. Leur délétion est létale.<br />
• On détermine si un gène est essentiel en réalisant <strong>la</strong> délétion dans un diploï<strong>de</strong>. Après<br />
dissection, seules <strong>de</strong>ux spores seront viables et ne porteront pas le marqueur <strong>de</strong> <strong>la</strong><br />
délétion.<br />
• Après mutagénèse aléatoire, on contourne le problème en recherchant <strong>de</strong>s mutations<br />
thermo-sensible (ts) pour lesquelles le produit du gène sera fonctionnel à température<br />
permissive (25°C) et inactif à température restrictive (37°C).<br />
• l’autre possibilité consiste à transformer <strong>la</strong> souche avec un p<strong>la</strong>smi<strong>de</strong> exprimant le gène<br />
sauvage <strong>de</strong> façon conditionnelle (sous contrôle d’un promoteur inductible).
ISOLEMENT DE MUTANT THERMOSENSIBLE
Pour analyser l’effet d’une mutation ponctuellesur un gène essentiel, on utilise <strong>la</strong> technique<br />
du ”p<strong>la</strong>smid shuffling”. La souche portant une délétion du gène est transformée par <strong>de</strong>ux<br />
p<strong>la</strong>smi<strong>de</strong>s, l’un porte le gène sauvage et le marqueur URA3, l’autre porte l’allèle muté à<br />
tester. La souche est étalée sur milieu contenant du FOA: seul les clones ayant perdu le<br />
vecteur avec l’allèle sauvage (et URA3) peuvent pousser à condition que l’allèle porté par le<br />
second vecteur soit fonctionnel.
IV génétique inverse<br />
-Basée sur le fait qu’un p<strong>la</strong>smi<strong>de</strong> linéaire ne peut pas être<br />
maintenu chez <strong>la</strong> levure à moins d’être recircu<strong>la</strong>risé:<br />
c’est <strong>la</strong> technique du «Gap repair»<br />
-Un <strong>de</strong>s moyens <strong>de</strong> recircu<strong>la</strong>riser le p<strong>la</strong>smi<strong>de</strong> est <strong>la</strong> recombinaison<br />
homologue avec <strong>de</strong>s séquences portées par un autre p<strong>la</strong>smi<strong>de</strong>,<br />
un fragment d’ADN ou l’ADN chromosomique<br />
X<br />
gapped p<strong>la</strong>smid<br />
X<br />
repair fragment<br />
gapped p<strong>la</strong>smid<br />
X X<br />
genomic copy is used to repair the gap; the temp<strong>la</strong>te is duplicated
IV les analyses génétiques<br />
BUT: déterminer si <strong>de</strong>s gènes (et leurs produits) contrôlent<br />
le même processus cellu<strong>la</strong>ire, par <strong>de</strong>s voies i<strong>de</strong>ntiques ou parallèles<br />
Pour ceci différentes approches peuvent être utilisées:<br />
- <strong>la</strong> recherche <strong>de</strong> suppresseurs<br />
- <strong>la</strong> recherche <strong>de</strong> suppresseurs multicopies<br />
- <strong>la</strong> recherche <strong>de</strong> mutation synthétique-létales
Les suppresseurs<br />
- Un suppresseur est un gène ou une mutation qui supprime au moins<br />
partiellement l’effet d’une première mutation: il permet <strong>de</strong> retrouver<br />
un phénotype plus ou moins sauvage.<br />
-La suppression peut être intragénique (sauf pour <strong>de</strong>s délétions)<br />
-Le suppresseur est le plus souvent extragénique. En général,<br />
il active le processus affecté par <strong>la</strong> première mutation ou active<br />
une voie parallèle redondante avec le première.
Les suppresseurs multicopies<br />
• Elle est basée sur <strong>la</strong> surexpression d’un gène via un p<strong>la</strong>smi<strong>de</strong> multicopies ou un<br />
promoteur fort: <strong>la</strong> surexpression du suppresseur supprime les effets <strong>de</strong> <strong>la</strong> première<br />
mutation.<br />
• En général, les suppresseurs multicopies sont <strong>de</strong>s gènes fonctionnant en aval<br />
<strong>de</strong> <strong>la</strong> mutation sur <strong>la</strong> même voie ou dans une voie parallèle.<br />
Cdc24<br />
Cdc42<br />
émergence du bourgeon<br />
XCdc24<br />
Cdc42<br />
X<br />
émergence du bourgeon<br />
X<br />
Cdc24<br />
Cdc42<br />
émergence du bourgeon
Les mutations synthétiques létales<br />
But: déterminer si les produits <strong>de</strong> <strong>de</strong>ux gènes fonctionnent dans <strong>de</strong>s voies<br />
parallèles.<br />
- Pratiquement, une souche portant une mutation x est transformée par un<br />
p<strong>la</strong>smi<strong>de</strong> portant une copie du gène sauvage exprimée <strong>de</strong> façon conditionnelle.<br />
Après mutagénèse <strong>de</strong> cette souche, on recherche les mutations qui ne<br />
permettent pas une croissance en absence d’induction du gène sauvage.<br />
- Cette approche a été robotisée et réalisée à l’échelle génomique (soit 4,200 x<br />
4,200 croisements, sporu<strong>la</strong>tions et analyse <strong>de</strong> tétra<strong>de</strong>s.)
Analyse <strong>de</strong>s re<strong>la</strong>tions épistatiques<br />
BUT: déterminer le nombre <strong>de</strong> gènes (protéines) impliqués dans un même<br />
processus et l’ordre dans lequel ils fonctionnent.<br />
L’approche consiste à combiner <strong>de</strong>ux mutations dans une cellule et à analyser le phénotype<br />
du double mutant.<br />
X<br />
X<br />
common target<br />
w soit 4 gènes dont <strong>la</strong> délétion entraine une sensibilité modérée aux fortes<br />
concentrations salines<br />
w Si on combine les délétions ∆hog1 et ∆pbs2, le double mutant présente <strong>la</strong><br />
meme sensibilité aux sels que les <strong>de</strong>ux simples mutants: ils fonctionnent<br />
dans <strong>la</strong> même voie.<br />
w Si on combine les délétions ∆pbs2 et ∆cba1, le double mutant présente<br />
une sensibilité accrue aux sels par rapport à chaque simple mutant: ils<br />
fonctionnent donc dans <strong>de</strong>ux voies parallèles pour controler le même<br />
processus.
X<br />
XSko1<br />
XSko1<br />
X<br />
Ordonner les protéines dans une voie<br />
w <strong>la</strong> délétion <strong>de</strong> PBS2 entraine une sensibilité accrue aux fortes<br />
concentrations salines tandis que <strong>la</strong> délétion <strong>de</strong> SKO1 rend les cellules<br />
plus tolérantes.<br />
w quel sera le phénotype du double mutant ∆pbs2,∆sko1?<br />
- si Sko1 agit en aval <strong>de</strong> Pbs2, on attend que le double mutant ait le même<br />
phenotype que <strong>la</strong> simple délétion ∆sko1: que les cellules soit plus<br />
tolérantes aux sels. La délétion sko1 est alors dite épistatic (dominante) <strong>de</strong><br />
<strong>la</strong> délétion ∆pbs2<br />
- Si Sko1p agit en amont <strong>de</strong> Hog1p, on attend que le double mutant ∆pbs2<br />
∆sko1 soit sensible au sels.
X<br />
Ordonner les protéines dans une voie<br />
w On peut aussi utiliser <strong>de</strong>s suppressions multicopies ou <strong>de</strong>s<br />
mutations activatrices: <strong>la</strong> suppression n’est possible que si <strong>la</strong><br />
protéines agit en aval <strong>de</strong> <strong>la</strong> mutation: <strong>la</strong> surexpression <strong>de</strong><br />
PBS2 ne peut pas supprimer le phénotype ∆hog1D<br />
w Une mutation activatrice <strong>de</strong> Hog1 peut supprimer <strong>la</strong><br />
sensibiliter aux sels d’un mutant ∆pbs2 mutant, mais l’inverse<br />
ne marche pas.<br />
w Le concept d’epistasie est très <strong>la</strong>rgement utilisé: si le<br />
phénotype d’un double mutant ressemble à celui du simple<br />
mutant, alors le produit du gène correspondant fonctionne le<br />
plus en aval dans le systèmes.
Les levures comme modèles?<br />
Les levures sont considérées comme <strong>de</strong>s organismes modèles c’est à dire que<br />
l’on anticipe qu’une partie au moins <strong>de</strong>s systèmes cellu<strong>la</strong>ires fonctionne <strong>de</strong><br />
façon simi<strong>la</strong>ire chez <strong>la</strong> levure et chez l’homme et par extension chez tous les<br />
eucaryotes.<br />
ceci est vrai dans une certaine mesure et <strong>de</strong> nombreux processus mis en évi<strong>de</strong>nce<br />
ou étudiés chez <strong>la</strong> levure se sont révélés en partie conservés chez les<br />
mammifères bien qu’avec <strong>de</strong>s niveaux <strong>de</strong> complexité plus élevés<br />
- <strong>la</strong> régu<strong>la</strong>tion du cycle cellu<strong>la</strong>ire<br />
- <strong>la</strong> transmission <strong>de</strong>s signaux extracellu<strong>la</strong>ires<br />
- le protéasome<br />
- certains aspects <strong>de</strong> <strong>la</strong> po<strong>la</strong>risation <strong>de</strong> <strong>la</strong> croissance<br />
- les régu<strong>la</strong>tions <strong>de</strong> l’expression <strong>de</strong>s gènes<br />
- le trafic intracellu<strong>la</strong>ire...
Les levures comme modèles<br />
Les levures sont considérées comme <strong>de</strong>s organismes modèles c’est à dire que<br />
l’on anticipe qu’une partie au moins <strong>de</strong>s systèmes cellu<strong>la</strong>ires fonctionne <strong>de</strong><br />
façon simi<strong>la</strong>ire chez <strong>la</strong> levure et chez l’homme et par extension chez tous les<br />
eucaryotes.<br />
ceci est vrai dans une certaine mesure et <strong>de</strong> nombreux processus mis en évi<strong>de</strong>nce<br />
ou étudier chez <strong>la</strong> levure se sont révélés en partie conservés chez les<br />
mammifères bien qu’avec <strong>de</strong>s niveaux <strong>de</strong> compléxité plus élevés<br />
- <strong>la</strong> régu<strong>la</strong>tion du cycle cellu<strong>la</strong>ire<br />
- <strong>la</strong> transmission <strong>de</strong>s signaux extracellu<strong>la</strong>ires<br />
- le protéasome<br />
- certains aspects <strong>de</strong> <strong>la</strong> po<strong>la</strong>risation <strong>de</strong> <strong>la</strong> croissance<br />
- les régu<strong>la</strong>tions <strong>de</strong> l’expression <strong>de</strong>s gènes<br />
- le trafic intracellu<strong>la</strong>ire
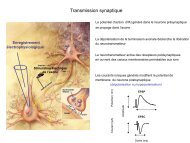
• Le principe du controle <strong>de</strong> <strong>la</strong><br />
transcription est bien conservé<br />
ainsi que les principaux facteurs<br />
<strong>de</strong> transcription.<br />
• La plupart <strong>de</strong>s constituants <strong>de</strong> <strong>la</strong><br />
machinerie d’initiation <strong>de</strong> <strong>la</strong><br />
transcription sont conservés <strong>de</strong> <strong>la</strong><br />
levure à l’homme<br />
• Beaucoup d’activateurs <strong>de</strong> <strong>la</strong><br />
transcription sont aussi<br />
conservés bien que certaine<br />
catégories n’existe pas chez <strong>la</strong><br />
levure<br />
• L’organisation <strong>de</strong> <strong>la</strong> chromatine<br />
semble plus simple chez <strong>la</strong><br />
levure mais son rôle dans <strong>la</strong><br />
régu<strong>la</strong>tion <strong>de</strong> <strong>la</strong> transcription est<br />
conservé<br />
• les mécanismes <strong>de</strong> transfert <strong>de</strong>s<br />
signaux à travers <strong>la</strong> membrane<br />
nucléaire sont aussi <strong>la</strong>rgement<br />
conservés.<br />
La régu<strong>la</strong>tion <strong>de</strong> <strong>la</strong> transcription
• Le transport <strong>de</strong>s vésicules, c’est à<br />
dire les mécanismes qui contrôle<br />
<strong>la</strong> trafic <strong>de</strong>s protéines et <strong>de</strong>s<br />
membranes, est aussi très<br />
conservé chez les eucaryotes<br />
• Des mutants thermo-sensible sec<br />
ont été c<strong>la</strong>ssés selon le sta<strong>de</strong><br />
auquel le trafic est bloqué (en<br />
utilisant <strong>la</strong> microscopie<br />
électronique). Cette c<strong>la</strong>ssification<br />
a constitué <strong>la</strong> base <strong>de</strong> l’analyse<br />
génétique.<br />
• le transport vers les vacuoles et<br />
l’endocytose sont eux étudier par<br />
<strong>la</strong> combinaison d’analyses<br />
génétiques, <strong>de</strong> biochimie et <strong>de</strong><br />
biologie cellu<strong>la</strong>ire.<br />
Le trafic cellu<strong>la</strong>ire
• Prions<br />
les systèmes non attendus<br />
– La levure possè<strong>de</strong> <strong>de</strong>ux systèmes possédant toutes les caractéristiques<br />
<strong>de</strong>s prions. Ce sont <strong>de</strong>s éléments génétiques, allèles <strong>de</strong> gènes connus qui<br />
se comporte comme <strong>de</strong>s éléments non-men<strong>de</strong>lien: PSI+ (Sup35p), une<br />
protéine impliquée dans <strong>la</strong> terminaison <strong>de</strong> <strong>la</strong> traduction et URE3<br />
(Ure2p), un régu<strong>la</strong>teur du métabolisme <strong>de</strong> l’azote.<br />
Ma<strong>la</strong>die <strong>de</strong> Creutzfeldt Jakob<br />
•longue longue phase d’incubation<br />
d incubation,<br />
• accumu<strong>la</strong>tion <strong>de</strong> structures amyloi<strong>de</strong>s<br />
--> mort neuronale<br />
• diagnostique complexe (no easy ante-mortem test),<br />
• sans traitement
PrP c<br />
apparition et propagation <strong>de</strong>s prions<br />
[prion-] [prion+]<br />
hélice lice a feuillet b<br />
monomères<br />
monom res<br />
solubles<br />
activité activit<br />
enzymatique<br />
aggregats<br />
insolubles<br />
activité activit<br />
enzymatique<br />
formation et propagation<br />
<strong>de</strong>s agrégats agr gats amyloi<strong>de</strong>s<br />
(snow snow ball mechanism)<br />
mechanism
Chez Saccharomyces cerevisiae<br />
PrP sc<br />
Formation <strong>de</strong> fibres amyloi<strong>de</strong>s<br />
Ure2 Sup35<br />
Rnq1, etc.<br />
Caughey B. (2000). TSE, amyloidoses and yeast prions: Common threads ? Nature me<strong>de</strong>cine 6, 751-754.
• Sup35 :<br />
- facteur <strong>de</strong> terminaison <strong>de</strong> <strong>la</strong> traduction (actif sous forme <strong>de</strong> complexe<br />
avec Sup45)<br />
Phenotype [psi<br />
Sup35 est fonctionnel<br />
- Génotype a<strong>de</strong> 1-14<br />
? ]<br />
red<br />
colonies<br />
><br />
‡ traduction stoppée (stop codon) : <strong>la</strong> souche est a<strong>de</strong>-.<br />
Phenotype [PSI + ]<br />
Sup35 forme <strong>de</strong>s agrégats<br />
‡ <strong>la</strong> traduction ne s'arrête pas au codon stop: <strong>la</strong><br />
souche est A<strong>de</strong>++<br />
white<br />
colonies
crib<strong>la</strong>ge <strong>de</strong> molécules «anti-prion»<br />
secondary screen<br />
based on another<br />
yeast prion<br />
test against<br />
mammalian prion
•Veillissement<br />
–Les levures ont une durée <strong>de</strong> vie prédéterminée, i.e. <strong>la</strong> cellule mère meure<br />
après 40 à 50 générations<br />
–Le veillissement semble avoir <strong>de</strong>s point commun entre <strong>la</strong> levure et les<br />
eucaryotes supérieurs (accumu<strong>la</strong>tion <strong>de</strong> rDNA circles, <strong>de</strong> protéines oxydées...<br />
–les mutations du gène, WRN (Werner’s syndrom) chez l’homme<br />
et <strong>de</strong> son homologue SGS1 chez <strong>la</strong> levure provoquent <strong>de</strong>s sénescences précoces.
Les levures comme outils<br />
-Biotechnologies:<br />
- concerne toute l’industrie du vin, <strong>de</strong> <strong>la</strong> bière et du pain.<br />
Les souches utilisées sont difficilement manipu<strong>la</strong>bles mais il y a<br />
beaucoup d’étu<strong>de</strong>s réalisées pour augmenter leur capacité<br />
<strong>de</strong> fermentation, <strong>de</strong> tolérance à l’alcool, aux sucres et aux fortes<br />
pressions osmotiques<br />
- <strong>la</strong> production <strong>de</strong> protéines: <strong>la</strong> capacité <strong>de</strong> production chez <strong>la</strong> levure<br />
sont bien inférieures à celle d’E. coli mais <strong>la</strong> possibilité existe <strong>de</strong><br />
produire <strong>de</strong>s protéines modifiées comme chez les eucaryotes supérieurs.<br />
La levure <strong>la</strong> plus utilisée dans ce cadre est Pichia pastoris qui fermente<br />
le méthanol.
-Clonage <strong>de</strong> gènes hétérologues:<br />
- <strong>de</strong> nombreux gènes <strong>de</strong> mammifères ou <strong>de</strong> p<strong>la</strong>ntes ont été clonés<br />
par complémentation <strong>de</strong> mutants <strong>de</strong> levure<br />
Pour ceci <strong>de</strong>s banques <strong>de</strong> cDNA sont construites dans <strong>de</strong>s vecteurs<br />
d’expression <strong>de</strong> levure sous contrôle d’un promoteur <strong>de</strong> levure.<br />
- crib<strong>la</strong>ge <strong>de</strong> médicaments:<br />
-lié à <strong>la</strong> possibilité <strong>de</strong> faire croître les levures<br />
rapi<strong>de</strong>ment y compris sur boites microtitres.<br />
- nécessite l’utilisation <strong>de</strong> mutants <strong>de</strong> <strong>la</strong> paroi pour augmenter<br />
<strong>la</strong> perméabilité <strong>de</strong>s cellules.