O Ciclo da Água evaporada e pode retornar - UFTM
O Ciclo da Água evaporada e pode retornar - UFTM
O Ciclo da Água evaporada e pode retornar - UFTM
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
CO2 + H2O ⇔ H2CO3 ⇔ H + + HCO3 - ⇔<br />
2H + + CO3 2- Ca 2+ + CO3 2- ⇔ CaCO3<br />
O carbonato de cálcio tem baixa<br />
solubili<strong>da</strong>de e precipita na coluna d’água.<br />
Sob condições áci<strong>da</strong>s, contudo, a formação<br />
de ácido carbônico remove os íons<br />
carbonato do sistema. Essa remoção reduz a<br />
quanti<strong>da</strong>de de carbonato de cálcio dissolvido<br />
na água, aumentando a dissolução de rochas<br />
de carbonato de cálcio e dos sedimentos por<br />
onde a água passa; assim águas áci<strong>da</strong>s<br />
dissolvem sedimentos calcários. Quando<br />
águas carrega<strong>da</strong>s de cálcio entram nos<br />
oceanos e se misturam com a água de pH<br />
praticamente neutro, o carbonato de cálcio<br />
torna-se menos solúvel e precipita-se<br />
formando sedimentos.<br />
No sistema marinho, sob condições<br />
aproxima<strong>da</strong>mente neutras, o sistema<br />
carbonato mantém um equilíbrio. CaCO3<br />
(insolúvel) + H2O + CO2 ⇔ Ca (HCO3)2<br />
(solúvel)<br />
A remoção de CO2 pela fotossíntese<br />
desloca a reação para a esquer<strong>da</strong>, resultando<br />
na formação e precipitação de carbonato de<br />
cálcio. Muitas algas excretam este carbonato<br />
de cálcio na água circulante, mas algas de<br />
recife e de coral incorporam a substância<br />
como estrutura rígi<strong>da</strong>.<br />
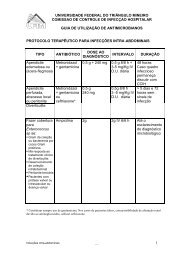
Quando a fotossíntese excede a<br />
respiração, o cálcio tende a precipitar-se.<br />
O <strong>Ciclo</strong> do Fósforo<br />
Devido ao requerimento nutricional<br />
<strong>da</strong>s plantas e animais o fósforo foi, e é, um<br />
elemento amplamente estu<strong>da</strong>do. Os<br />
organismos requerem cerca de um décimo<br />
<strong>da</strong> quanti<strong>da</strong>de requeri<strong>da</strong> de nitrogênio.<br />
O fósforo é constituinte dos ácidos<br />
nucléicos, membranas celulares, sistema de<br />
transferência de energia (ATP), ossos e<br />
dentes. Sendo o fósforo um fator limitante<br />
Página 2 de 28<br />
<strong>da</strong> produção de matéria orgânica, a sua<br />
abundância <strong>pode</strong> promover o crescimento<br />
exagerado de plantas e consequentemente de<br />
animais.<br />
Este nutriente é assimilado na forma<br />
do íon fosfato (PO4 3- ) diretamente do solo ou<br />
<strong>da</strong> água, sendo incorporado em vários<br />
compostos orgânicos. Os animais eliminam<br />
o excesso de fósforo orgânico excretando<br />
sais de fósforo na urina. O fósforo não entra<br />
na atmosfera, assim o ciclo envolve somente<br />
os compartimentos do solo e aquáticos do<br />
ecossistema.<br />
O <strong>Ciclo</strong> do Enxofre<br />
O enxofre ocorre nos aminoácidos<br />
cistina e metionina e assim é requerido pelas<br />
plantas e animais. Assim como o ciclo do<br />
nitrogênio, o ciclo do enxofre também segue<br />
vários caminhos e afeta o ciclo de outros<br />
elementos.<br />
Em condições aeróbicas, a redução<br />
assimilativa de enxofre (SO4 2- → S<br />
orgânico) equilibra a oxi<strong>da</strong>ção do enxofre<br />
orgânico de volta ao sulfato (SO4 2- , a forma<br />
mais oxi<strong>da</strong><strong>da</strong> do enxofre), ou diretamente ou<br />
passando pelo sulfito (SO3 2- ) como um passo<br />
intermediário. Esta oxi<strong>da</strong>ção ocorre quando<br />
os animais excretam o enxofre orgânico<br />
excessivo <strong>da</strong> dieta e quando os<br />
microorganismos decompõem detritos<br />
vegetais e animais.<br />
Sob condições anaeróbicas, o sulfato<br />
<strong>pode</strong> funcionar como um oxi<strong>da</strong>nte. As<br />
bactérias Desulfovibrio e Desulfomonas<br />
acoplam redução desassimilativa de sulfato<br />
(SO4 2- → S 2- ) com a oxi<strong>da</strong>ção de carbono<br />
orgânico para fornecer energia disponível .<br />
O reduzido S 2- <strong>pode</strong> então ser usado como<br />
um agente redutor (S 2 → S 0 + 2e - ) por<br />
bactéria fotoautotrófica, a qual assimila o<br />
carbono por caminhos análogos aos <strong>da</strong><br />
fotossíntese <strong>da</strong>s plantas verdes. O enxofre<br />
toma o lugar do átomo de oxigênio na água<br />
como um doador de elétrons. O enxofre<br />
elementar acumula-se a menos que os<br />
sedimentos fiquem expostos ao oxigênio, e<br />
em sendo assim o enxofre <strong>pode</strong> ser oxi<strong>da</strong>do<br />
ain<strong>da</strong> mais em sulfeto (SO3 2- ) e sulfato<br />
(SO4 2- ).