GIÁO ÁN ÔN TẬP HÓA HỌC 10
LINK BOX: https://app.box.com/s/ygxm0pcdfqlw6e5wow2zrywipszn87c8 LINK DOCS.GOOGLE: https://drive.google.com/file/d/1W_Sgls2lsz0Y1CyZLXa9hXfGHYF4MrQe/view?usp=sharing
LINK BOX:
https://app.box.com/s/ygxm0pcdfqlw6e5wow2zrywipszn87c8
LINK DOCS.GOOGLE:
https://drive.google.com/file/d/1W_Sgls2lsz0Y1CyZLXa9hXfGHYF4MrQe/view?usp=sharing
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
https://twitter.com/daykemquynhon<br />
https://plus.google.com/+DạyKèmQuyNhơn<br />
www.facebook.com/daykem.quynhon<br />
http://daykemquynhon.blogspot.com<br />
http://daykemquynhon.ucoz.com<br />
Nơi bồi dưỡng kiến thức Toán - Lý - Hóa cho học sinh cấp 2+3 /<br />
Diễn Đàn Toán - Lý - Hóa <strong>10</strong>00B Trần Hưng Đạo Tp.Quy Nhơn Tỉnh Bình Định<br />
NỘI DUNG<br />
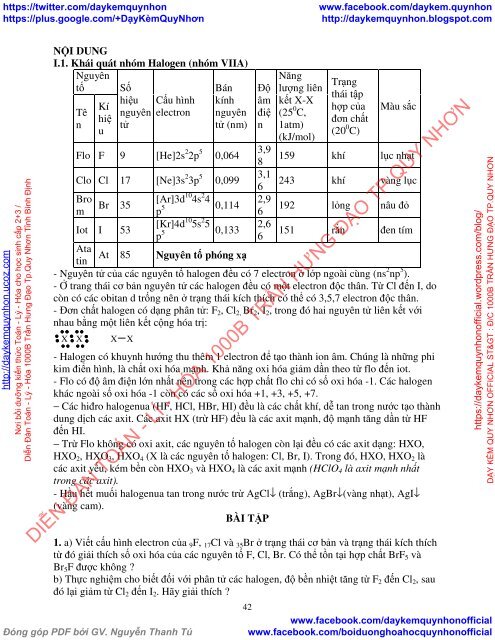
I.1. Khái quát nhóm Halogen (nhóm VIIA)<br />
Nguyên<br />
tố<br />
Tê<br />
n<br />
Kí<br />
hiệ<br />
u<br />
Số<br />
hiệu<br />
nguyên<br />
tử<br />
Cấu hình<br />
electron<br />
Bán<br />
kính<br />
nguyên<br />
tử (nm)<br />
Độ<br />
âm<br />
điệ<br />
n<br />
Năng<br />
lượng liên<br />
kết X-X<br />
(25 0 C,<br />
1atm)<br />
(kJ/mol)<br />
Trạng<br />
thái tập<br />
hợp của<br />
đơn chất<br />
(20 0 C)<br />
Màu sắc<br />
Flo F 9 [He]2s 2 2p 5 0,064<br />
3,9<br />
8<br />
159 khí lục nhạt<br />
Clo Cl 17 [Ne]3s 2 3p 5 0,099<br />
3,1<br />
6<br />
243 khí vàng lục<br />
Bro<br />
[Ar]3d <strong>10</strong> 4s 2 4 2,9<br />
Br 35<br />
m<br />
p 5 0,114<br />
6<br />
192 lỏng nâu đỏ<br />
Iot I 53<br />
[Kr]4d <strong>10</strong> 5s 2 5 2,6<br />
p 5 0,133<br />
6<br />
151 rắn đen tím<br />
Ata<br />
tin<br />
At 85 Nguyên tố phóng xạ<br />
- Nguyên tử của các nguyên tố halogen đều có 7 electron ở lớp ngoài cùng (ns 2 np 5 ).<br />
- Ở trang thái cơ bản nguyên tử các halogen đều có một electron độc thân. Từ Cl đến I, do<br />
còn có các obitan d trống nên ở trạng thái kích thích có thể có 3,5,7 electron độc thân.<br />
- Đơn chất halogen có dạng phân tử: F 2 , Cl 2, Br 2 , I 2 , trong đó hai nguyên tử liên kết với<br />
nhau bằng một liên kết cộng hóa trị:<br />
X X X X<br />
- Halogen có khuynh hướng thu thêm 1 electron để tạo thành ion âm. Chúng là những phi<br />
kim điển hình, là chất oxi hóa mạnh. Khả năng oxi hóa giảm dần theo từ flo đến iot.<br />
- Flo có độ âm điện lớn nhất nên trong các hợp chất flo chỉ có số oxi hóa -1. Các halogen<br />
khác ngoài số oxi hóa -1 còn có các số oxi hóa +1, +3, +5, +7.<br />
− Các hiđro halogenua (HF, HCl, HBr, HI) đều là các chất khí, dễ tan trong nước tạo thành<br />
dung dịch các axit. Các axit HX (trừ HF) đều là các axit mạnh, độ mạnh tăng dần từ HF<br />
đến HI.<br />
− Trừ Flo không có oxi axit, các nguyên tố halogen còn lại đều có các axit dạng: HXO,<br />
HXO 2 , HXO 3 , HXO 4 (X là các nguyên tố halogen: Cl, Br, I). Trong đó, HXO, HXO 2 là<br />
các axit yếu, kém bền còn HXO 3 và HXO 4 là các axit mạnh (HClO 4 là axit mạnh nhất<br />
trong các axit).<br />
- Hầu hết muối halogenua tan trong nước trừ AgCl↓ (trắng), AgBr↓(vàng nhạt), AgI↓<br />
(vàng cam).<br />
BÀI <strong>TẬP</strong><br />
DIỄN ĐÀN TO<strong>ÁN</strong> - LÍ - <strong>HÓA</strong> <strong>10</strong>00B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
1. a) Viết cấu hình electron của 9 F, 17 Cl và 35 Br ở trạng thái cơ bản và trạng thái kích thích<br />
từ đó giải thích số oxi hóa của các nguyên tố F, Cl, Br. Có thể tồn tại hợp chất BrF 5 và<br />
Br 5 F được không ?<br />
b) Thực nghiệm cho biết đối với phân tử các halogen, độ bền nhiệt tăng từ F 2 đến Cl 2 , sau<br />
đó lại giảm từ Cl 2 đến I 2 . Hãy giải thích ?<br />
Đóng góp PDF bởi GV. Nguyễn Thanh Tú<br />
https://daykemquynhonofficial.wordpress.com/blog/<br />
DẠY KÈM QUY NHƠN OFFICIAL ST> : Đ/C <strong>10</strong>00B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
42<br />
www.facebook.com/daykemquynhonofficial<br />
www.facebook.com/boiduonghoahocquynhonofficial