MC-Handout 4xx - ChemistforChrist
MC-Handout 4xx - ChemistforChrist
MC-Handout 4xx - ChemistforChrist
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
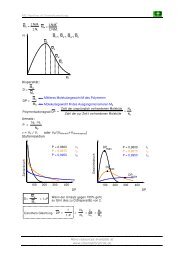
<strong>MC</strong> <strong>Handout</strong> 4: Anionische Polymerisation<br />
BuLi<br />
PS<br />
PS-b-BR<br />
"tapered" = Spitz zu laufen<br />
7 Kationische Polymerisation<br />
Kationische Polymerisationen sind Kettenreaktionen. Die Polymerisation erfolgt in den<br />
drei Schritten Initiierung, Wachstum und Abbruch. Die Reaktion kann als kationische<br />
Vinylpolymerisation oder kationische ringöffnende Polymerisation erfolgen.<br />
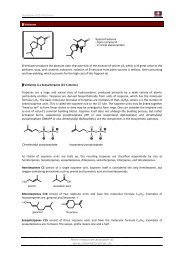
Carbenium Ion Oxonium Ion<br />
Kinetik der kationischen Polymerisation<br />
Initiatoren:<br />
O<br />
Starke Protonensäuren: HClO4, CF3SO3H,....<br />
Lewis Säuren: AlCl3, SnCl4, BF3, FeCl3, SnBr4 (AlCl3 → AlCl4 - AlCl2 + )<br />
Alkylhalogenide + LS: R-Cl + BF3 → R + [ClBF3] -<br />
Alkohole (H2O) + LS: R-OH + BF3 → R + [ROBF3] -<br />
Carbenium Ionen Ph3C + BF4 - , R3S + X - , ArN2 + X -<br />
Fotoinitiatoren: Ph3S + BF4 - → Ph . + Ph2S + HF +..<br />
Fe PF 6<br />
O<br />
hν<br />
O<br />
Fe<br />
O O<br />
PF 6<br />
Initiation<br />
Reaktionsgeschwindigkeit und Mechanismus hängen von der Polarität des LM und der<br />
Natur des Gegenions ab. In polaren L.M. liegt der Initiator in der dissoziierten Form als<br />
freie Ionen, in unpolaren LM undissoziiert, d.h. kovalent vor. Mit der Polarität des LM<br />
nimmt auch die Reaktionsgeschwindigkeit zu.<br />
M A M A M + A<br />
kovalente<br />
Bindung<br />
LM separiertes<br />
Ionenpaar<br />
Polarität des LM nimmt zu<br />
Wachstum<br />
freie Ionen<br />
More resources available at<br />
www.chemistforchrist.de<br />
.......<br />
Mechanismus ist abhängig vom Gegenion, LM, T und Art des Monomeren.<br />
Wachstumsrate: - d[M]<br />
dt<br />
=<br />
k i k p<br />
k t<br />
[HX] [M] 2