Ergebnisse: 3,4-trans-CHDSelektivität [mol/mol]0,300,250,200,150,100,05Selektivität:differentiellintegral0,000 10 20 30 40Prozesszeit [h]Produktivität und Raum-Zeit-Ausbeute[mmol/(l*h)]10864200 10 20 30 40Prozesszeit [h]QpRZAAbb. 6.4:Verlauf der differentiellen und integralen Selektivität (links) und grafische Darstellung derdifferentiellen Produktivität und der integralen Raum-Zeit-Ausbeute (rechts) (7,5 Liter; E.coli F82pC22).Bei Fermentationen mit dem Produktionsstamm F82pC22 wurde eine Vielzahl vonNebenprodukten akkumuliert. In der Abbildung 6.5 sind die Verläufe der spezifischendifferentiellen Produkt- und Nebenproduktbildungsraten dargestellt. Nach der IPTG-Induktionstieg die Produktbildungsrate auf einen maximalen Wert von 0,52 mmol/(g*h). Gleichzeitigwurde Shikimat-3-Phosphat, ein Intermediat der Aromaten-Biosynthese, gebildet. Diemaximale spezifische Shikimat-Bildungsrate betrug 0,09 mmol/(g*h). Chorismat, ein weiteresIntermediat der Aromaten-Biosynthese, wurde während der Wachstumsphase akkumuliert.Die maximale Chorismat-Bildungsrate wurde nach 10,2 Stunden mit 0,05 mmol/(g*h)gemessen. Im Laufe der Produktionsphase wurden die Nebenprodukte Shikimat und4-Hydroxy-Benzosäure akkumuliert.spez. Bildungsrate [mmol/(g*h)]0,50,40,30,20,1spez. Bildungsrate:3,4-CHDChorismatS-3-P und Shikimat4-Hydroxy-Benzoat0,00 10 20 30 40Prozesszeit [h]spez. Bildungs- und Verbrauchsraten[mmol/(g*h)]1001010,1Glucoseverbrauchsrate3,4-CHD-BildungsrateCO 2 -Bildungsrate0,010 10 20 30 40Prozesszeit [h]1001010,10,01Abb. 6.5: Links: Verlauf der differentiellen biomassespezifischen Bildungsraten des Produkts 3,4-trans-CHD, des Nebenproduktes 4-Hydroxy-Benzoat und der Intermediate der Aromaten-Biosynthese Chorismat, Shikimat-3-Phosphat und Shikimat. Rechts: LogarithmischeDarstellung der differentiellen Glukoseverbrauchsrate, der 3,4-trans-CHD- undKohlendioxidbildungsrate (7,5 Liter; E. coli F82pC22).85
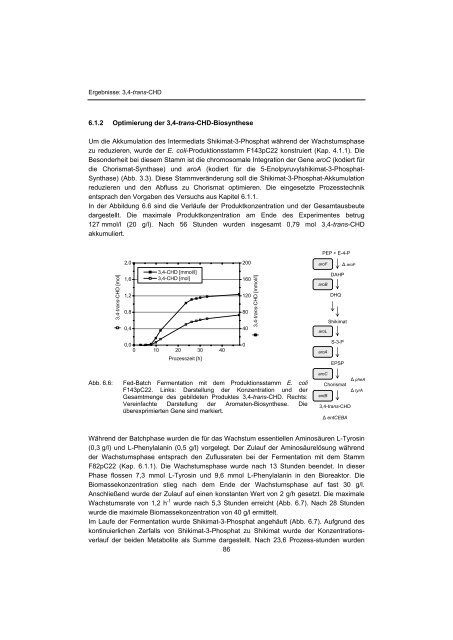
Ergebnisse: 3,4-trans-CHD6.1.2 Optimierung der 3,4-trans-CHD-BiosyntheseUm die Akkumulation des Intermediats Shikimat-3-Phosphat während der Wachstumsphasezu reduzieren, wurde der E. coli-Produktionsstamm F143pC22 konstruiert (Kap. 4.1.1). DieBesonderheit bei diesem Stamm ist die chromosomale Integration der Gene aroC (kodiert fürdie Chorismat-Synthase) und aroA (kodiert für die 5-Enolpyruvylshikimat-3-Phosphat-Synthase) (Abb. 3.3). Diese Stammveränderung soll die Shikimat-3-Phosphat-Akkumulationreduzieren und den Abfluss zu Chorismat optimieren. Die eingesetzte Prozesstechnikentsprach den Vorgaben des Versuchs aus Kapitel 6.1.1.In der Abbildung 6.6 sind die Verläufe der Produktkonzentration und der Gesamtausbeutedargestellt. Die maximale Produktkonzentration am Ende des Experimentes betrug127 mmol/l (20 g/l). Nach 56 Stunden wurden insgesamt 0,79 mol 3,4-trans-CHDakkumuliert.PEP + E-4-P3,4-trans-CHD [mol]2,01,61,20,80,43,4-CHD [mmol/l]3,4-CHD [mol]20016012080403,4-trans-CHD [mmol/l]aroF aroFDAHParoBDHQShikimataroL0,00 10 20 30 40Prozesszeit [h]0aroAS-3-PEPSPAbb. 6.6:Fed-Batch Fermentation mit dem Produktionsstamm E. coliF143pC22. Links: Darstellung der Konzentration und derGesamtmenge des gebildeten Produktes 3,4-trans-CHD. Rechts:Vereinfachte Darstellung der Aromaten-Biosynthese. Dieüberexprimierten Gene sind markiert.aroC pheAChorismat tyrAentB3,4-trans-CHD entCEBAWährend der Batchphase wurden die für das Wachstum essentiellen Aminosäuren L-Tyrosin(0,3 g/l) und L-Phenylalanin (0,5 g/l) vorgelegt. Der Zulauf der Aminosäurelösung währendder Wachstumsphase entsprach den Zuflussraten bei der Fermentation mit dem StammF82pC22 (Kap. 6.1.1). Die Wachstumsphase wurde nach 13 Stunden beendet. In dieserPhase flossen 7,3 mmol L-Tyrosin und 9,6 mmol L-Phenylalanin in den Bioreaktor. DieBiomassekonzentration stieg nach dem Ende der Wachstumsphase auf fast 30 g/l.Anschließend wurde der Zulauf auf einen konstanten Wert von 2 g/h gesetzt. Die maximaleWachstumsrate von 1,2 h -1 wurde nach 5,3 Stunden erreicht (Abb. 6.7). Nach 28 Stundenwurde die maximale Biomassekonzentration von 40 g/l ermittelt.Im Laufe der Fermentation wurde Shikimat-3-Phosphat angehäuft (Abb. 6.7). Aufgrund deskontinuierlichen Zerfalls von Shikimat-3-Phosphat zu Shikimat wurde der Konzentrationsverlaufder beiden Metabolite als Summe dargestellt. Nach 23,6 Prozess-stunden wurden86
- Seite 8:
DanksagungDanksagungHerrn Prof. Dr.
- Seite 11 und 12:
Inhaltsverzeichnis4.3 Apparativer A
- Seite 13 und 14:
AbkürzungenAbkürzungsverzeichnis:
- Seite 15 und 16:
AbkürzungenF Kraft Ng Erdbeschleun
- Seite 17 und 18:
EinleitungUmweltschutz und der Land
- Seite 20 und 21:
Zielsetzung2 Zielsetzung der Arbeit
- Seite 22 und 23:
Stand des Wissens3 Stand des Wissen
- Seite 24 und 25:
Stand des WissensD-GlukoseptsPyruva
- Seite 26 und 27:
Stand des Wissensisofunktionelle Me
- Seite 28 und 29:
Stand des Wissensmit einer annäher
- Seite 30 und 31:
Stand des WissensDas Produkt 2,3-tr
- Seite 32 und 33:
Stand des Wissens3.3 Verfahrenstech
- Seite 34 und 35:
Stand des Wissens3.3.2.1 Reaktivext
- Seite 36 und 37:
Stand des Wissens-Cl+NTOMAC: CH 3 (
- Seite 38 und 39:
Stand des WissensDie Gleichgewichtk
- Seite 40 und 41:
Stand des Wissensorganische Phasew
- Seite 42 und 43:
Stand des WissensDer Stofftransport
- Seite 44 und 45:
Stand des Wissenswd( 2t w org 2 r
- Seite 46 und 47:
Stand des WissensDie im Rahmen dies
- Seite 48 und 49:
Stand des WissenscP cend P0RZA (3-
- Seite 50: Stand des WissensAnreicherung [%]in
- Seite 53 und 54: Material und MethodenFür die Produ
- Seite 55 und 56: Material und Methoden4.2.2 Bestimmu
- Seite 57 und 58: Material und MethodenAbb. 4.1:Links
- Seite 59 und 60: Material und MethodenDie Kalibrieru
- Seite 61 und 62: Material und Methoden4.3.2 Fermenta
- Seite 63 und 64: Material und MethodenGlucoseL-TyrL-
- Seite 65 und 66: Material und Methoden42 Liter Maste
- Seite 67 und 68: Material und Methoden40 cm10 cmAbb.
- Seite 69 und 70: Material und Methoden4.3.7 Prozessk
- Seite 72 und 73: Ergebnisse: 2,3-trans-CHD5 Ergebnis
- Seite 74 und 75: Ergebnisse: 2,3-trans-CHDder Aminos
- Seite 76 und 77: Ergebnisse: 2,3-trans-CHDZwischen d
- Seite 78 und 79: Ergebnisse: 2,3-trans-CHDGlukonsäu
- Seite 80 und 81: Ergebnisse: 2,3-trans-CHD3 mmol/(l*
- Seite 82 und 83: Ergebnisse: 2,3-trans-CHDWachstumsp
- Seite 84 und 85: Ergebnisse: 2,3-trans-CHD251501002,
- Seite 86 und 87: Diskussion: 2,3-trans-CHD5.2 Diskus
- Seite 88 und 89: Diskussion: 2,3-trans-CHD1,02,0Bild
- Seite 90 und 91: Diskussion: 2,3-trans-CHD2,3-CHD Ac
- Seite 92 und 93: Diskussion: 2,3-trans-CHDCOOHNHCOOH
- Seite 94 und 95: Diskussion: 2,3-trans-CHDDifferenz:
- Seite 96 und 97: Diskussion: 2,3-trans-CHDAbnahme de
- Seite 98 und 99: Ergebnisse: 3,4-trans-CHD6 Ergebnis
- Seite 102 und 103: Ergebnisse: 3,4-trans-CHD3 mmol/l g
- Seite 104 und 105: Ergebnisse: 3,4-trans-CHD3,4-trans-
- Seite 106 und 107: Ergebnisse: 3,4-trans-CHDtrans-CHD
- Seite 108 und 109: Ergebnisse: 3,4-trans-CHDwährend d
- Seite 110 und 111: Diskussion: 3,4-trans-CHD6.2 Diskus
- Seite 112 und 113: Diskussion: 3,4-trans-CHDChorismat
- Seite 114 und 115: Diskussion: 3,4-trans-CHDführen, d
- Seite 116 und 117: Diskussion: 3,4-trans-CHDNur unter
- Seite 118 und 119: Ergebnisse: 2,3-trans-CHA7 Fermenta
- Seite 120 und 121: Diskussion: 2,3-trans-CHA7.2 Diskus
- Seite 122 und 123: Ergebnisse: Reaktivextraktion8 Erge
- Seite 124 und 125: Ergebnisse: Reaktivextraktiongrades
- Seite 126 und 127: Ergebnisse: Reaktivextraktion3,4-tr
- Seite 128 und 129: Ergebnisse: Reaktivextraktion2,3-tr
- Seite 130 und 131: Ergebnisse: Reaktivextraktion250in
- Seite 132 und 133: Ergebnisse: ReaktivextraktionRaum-Z
- Seite 134 und 135: Ergebnisse: ReaktivextraktionDurch
- Seite 136 und 137: Diskussion: Reaktivextraktion8.4 Di
- Seite 138 und 139: Diskussion: ReaktivextraktionDie Ur
- Seite 140 und 141: Diskussion: ReaktivextraktionVergle
- Seite 142 und 143: Diskussion: ReaktivextraktionDas Pr
- Seite 144 und 145: Zusammenfassung9 ZusammenfassungIm
- Seite 146 und 147: Ausblick10 AusblickDie drei Produkt
- Seite 148 und 149: AusblickOptimierung der Reaktivextr
- Seite 150 und 151:
Literaturverzeichnis11 Literaturver
- Seite 152 und 153:
LiteraturverzeichnisGibson DT, Koch
- Seite 154 und 155:
LiteraturverzeichnisMüller R, Breu
- Seite 156 und 157:
LiteraturverzeichnisWieczorek S, Br
- Seite 158 und 159:
Anhang12 Anhang12.1 Zusammensetzung
- Seite 160 und 161:
Anhang12.1.6 Zulaufmedien: Glukose
- Seite 162 und 163:
Anhang12.2.1 Datenblatt der chemisc
- Seite 164 und 165:
AnhangGeräteparameter:stationäre
- Seite 166 und 167:
Anhang2,3-trans-CHD3,4-trans-CHDAbb
- Seite 168 und 169:
AnhangAbb. 12.3:1 H-NMR-Spektrum de
- Seite 170 und 171:
AnhangSauerstoffelektrode 12 mm Oxy
- Seite 172 und 173:
Anhang Bei dem Einsatz des accutren
- Seite 174 und 175:
AnhangAbb. 5.6:Abb. 5.7:Abb. 5.8:Ab
- Seite 176 und 177:
AnhangAbb. 6.15: Gegenüberstellung
- Seite 178:
Anhang12.8 TabellenverzeichnisTab.
- Seite 181 und 182:
Schriften des Forschungszentrums J
- Seite 183:
Schriften des Forschungszentrums J