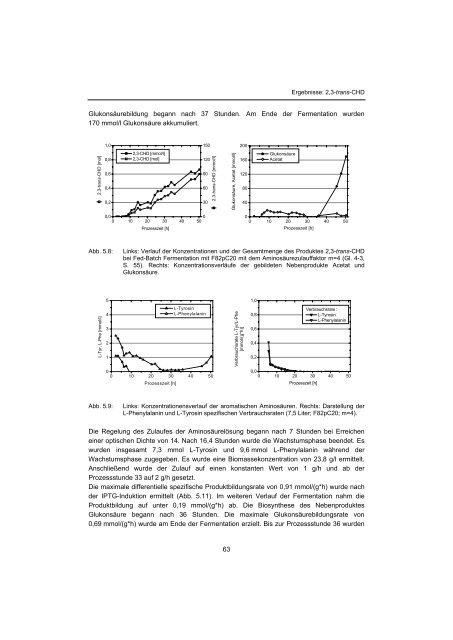
Ergebnisse: 2,3-trans-CHDGlukonsäurebildung begann nach 37 Stunden. Am Ende der Fermentation wurden170 mmol/l Glukonsäure akkumuliert.1,01502002,3-trans-CHD [mol]0,80,60,40,22,3-CHD [mmol/l]2,3-CHD [mol]1209060302,3-trans-CHD [mmol/l]Glukonsäure, Acetat [mmol/l]1601208040GlukonsäureAcetat0,00 10 20 30 40 50Prozesszeit [h]000 10 20 30 40 50Prozesszeit [h]Abb. 5.8:Links: Verlauf der Konzentrationen und der Gesamtmenge des Produktes 2,3-trans-CHDbei Fed-Batch Fermentation mit F82pC20 mit dem Aminosäurezulauffaktor m=4 (Gl. 4-3,S. 55). Rechts: Konzentrationsverläufe der gebildeten Nebenprodukte Acetat undGlukonsäure.L-Tyr, L-Phe [mmol/l]54321L-TyrosinL-Phenylalanin00 10 20 30 40 50Prozesszeit [h]Verbrauchsrate L-Tyr/L-Phe[mmol/(g*h)]1,00,80,60,40,2Verbrauchsrate :L-TyrosinL-Phenylalanin0,00 10 20 30 40 50Prozesszeit [h]Abb. 5.9:Links: Konzentrationensverlauf der aromatischen Aminosäuren. Rechts: Darstellung derL-Phenylalanin und L-Tyrosin spezifischen Verbrauchsraten (7,5 Liter; F82pC20; m=4).Die Regelung des Zulaufes der Aminosäurelösung begann nach 7 Stunden bei Erreicheneiner optischen Dichte von 14. Nach 16,4 Stunden wurde die Wachstumsphase beendet. Eswurden insgesamt 7,3 mmol L-Tyrosin und 9,6 mmol L-Phenylalanin während derWachstumsphase zugegeben. Es wurde eine Biomassekonzentration von 23,8 g/l ermittelt.Anschließend wurde der Zulauf auf einen konstanten Wert von 1 g/h und ab derProzessstunde 33 auf 2 g/h gesetzt.Die maximale differentielle spezifische Produktbildungsrate von 0,91 mmol/(g*h) wurde nachder IPTG-Induktion ermittelt (Abb. 5.11). Im weiteren Verlauf der Fermentation nahm dieProduktbildung auf unter 0,19 mmol/(g*h) ab. Die Biosynthese des NebenproduktesGlukonsäure begann nach 36 Stunden. Die maximale Glukonsäurebildungsrate von0,69 mmol/(g*h) wurde am Ende der Fermentation erzielt. Bis zur Prozessstunde 36 wurden63
Ergebnisse: 2,3-trans-CHD3,8 mmol/(g*h) CO 2 gebildet. Während der Glukonsäurebildung nahm dieKohlendioxidbildung um 32% auf 2,6 mmol/(g*h) ab. In dem gleichen Zeitraum stieg dieGlukoseverbrauchsrate um 41% von 0,78 auf 1,33 mmol/(g*h).502,020Biomasse [g/l]40302010BiomasseWachstumsrate1,61,20,80,4Wachstumsrate [1/h]Aminosäurenzulaufrate [g/h]161284Zulauffaktor:m=2m=400 10 20 30 40 50Prozesszeit [h]0,000 10 20 30 40 50Prozesszeit [h]Abb. 5.10: Links: Verlauf der Biomassekonzentration und der Wachstumsrate (7,5 Liter; E. coliF82pC20; m=4). Rechts: Vergleich der Verläufe der Aminosäurenzulaufraten beiExperimenten mit einem Zulauffaktor von m=2 und m=4 (Gl. 4-3, S. 55).Bildungs- und Verbrauchsraten[mmol/(g*h)]1001010,1Glukonsäure Glucose2,3-trans-CHD CO 20,010 10 20 30 40 50Prozesszeit [h]1001010,10,01Abb. 5.11: Logarithmische Darstellung des Verlaufes der differentiellen spezifischenGlukoseverbrauchsrate und der spezifischen 2,3-trans-CHD-, Glukonsäure- und CO 2 -Bildungsraten (7,5 Liter; E. coli F82pC20; m=4).Es wurde eine maximale differentielle substratbezogene Ausbeute von 13,6 %mol/molerreicht (Abb. 5.12). Nach der Induktion der Glukonsäurebiosynthese stagnierte der Wert aufeinem Niveau von 6 bis 8 %mol/mol. Die integrale Selektivität ergab ein Maximum von8,3 %mol/mol. Nach dem Ende des Wachstums wurde die maximale Produktivität von4,2 mmol/(l*h) erreicht. Im weiteren Verlauf der Fermentation sank der Wert auf 2 bis64
- Seite 8:
DanksagungDanksagungHerrn Prof. Dr.
- Seite 11 und 12:
Inhaltsverzeichnis4.3 Apparativer A
- Seite 13 und 14:
AbkürzungenAbkürzungsverzeichnis:
- Seite 15 und 16:
AbkürzungenF Kraft Ng Erdbeschleun
- Seite 17 und 18:
EinleitungUmweltschutz und der Land
- Seite 20 und 21:
Zielsetzung2 Zielsetzung der Arbeit
- Seite 22 und 23:
Stand des Wissens3 Stand des Wissen
- Seite 24 und 25:
Stand des WissensD-GlukoseptsPyruva
- Seite 26 und 27:
Stand des Wissensisofunktionelle Me
- Seite 28 und 29: Stand des Wissensmit einer annäher
- Seite 30 und 31: Stand des WissensDas Produkt 2,3-tr
- Seite 32 und 33: Stand des Wissens3.3 Verfahrenstech
- Seite 34 und 35: Stand des Wissens3.3.2.1 Reaktivext
- Seite 36 und 37: Stand des Wissens-Cl+NTOMAC: CH 3 (
- Seite 38 und 39: Stand des WissensDie Gleichgewichtk
- Seite 40 und 41: Stand des Wissensorganische Phasew
- Seite 42 und 43: Stand des WissensDer Stofftransport
- Seite 44 und 45: Stand des Wissenswd( 2t w org 2 r
- Seite 46 und 47: Stand des WissensDie im Rahmen dies
- Seite 48 und 49: Stand des WissenscP cend P0RZA (3-
- Seite 50: Stand des WissensAnreicherung [%]in
- Seite 53 und 54: Material und MethodenFür die Produ
- Seite 55 und 56: Material und Methoden4.2.2 Bestimmu
- Seite 57 und 58: Material und MethodenAbb. 4.1:Links
- Seite 59 und 60: Material und MethodenDie Kalibrieru
- Seite 61 und 62: Material und Methoden4.3.2 Fermenta
- Seite 63 und 64: Material und MethodenGlucoseL-TyrL-
- Seite 65 und 66: Material und Methoden42 Liter Maste
- Seite 67 und 68: Material und Methoden40 cm10 cmAbb.
- Seite 69 und 70: Material und Methoden4.3.7 Prozessk
- Seite 72 und 73: Ergebnisse: 2,3-trans-CHD5 Ergebnis
- Seite 74 und 75: Ergebnisse: 2,3-trans-CHDder Aminos
- Seite 76 und 77: Ergebnisse: 2,3-trans-CHDZwischen d
- Seite 80 und 81: Ergebnisse: 2,3-trans-CHD3 mmol/(l*
- Seite 82 und 83: Ergebnisse: 2,3-trans-CHDWachstumsp
- Seite 84 und 85: Ergebnisse: 2,3-trans-CHD251501002,
- Seite 86 und 87: Diskussion: 2,3-trans-CHD5.2 Diskus
- Seite 88 und 89: Diskussion: 2,3-trans-CHD1,02,0Bild
- Seite 90 und 91: Diskussion: 2,3-trans-CHD2,3-CHD Ac
- Seite 92 und 93: Diskussion: 2,3-trans-CHDCOOHNHCOOH
- Seite 94 und 95: Diskussion: 2,3-trans-CHDDifferenz:
- Seite 96 und 97: Diskussion: 2,3-trans-CHDAbnahme de
- Seite 98 und 99: Ergebnisse: 3,4-trans-CHD6 Ergebnis
- Seite 100 und 101: Ergebnisse: 3,4-trans-CHDSelektivit
- Seite 102 und 103: Ergebnisse: 3,4-trans-CHD3 mmol/l g
- Seite 104 und 105: Ergebnisse: 3,4-trans-CHD3,4-trans-
- Seite 106 und 107: Ergebnisse: 3,4-trans-CHDtrans-CHD
- Seite 108 und 109: Ergebnisse: 3,4-trans-CHDwährend d
- Seite 110 und 111: Diskussion: 3,4-trans-CHD6.2 Diskus
- Seite 112 und 113: Diskussion: 3,4-trans-CHDChorismat
- Seite 114 und 115: Diskussion: 3,4-trans-CHDführen, d
- Seite 116 und 117: Diskussion: 3,4-trans-CHDNur unter
- Seite 118 und 119: Ergebnisse: 2,3-trans-CHA7 Fermenta
- Seite 120 und 121: Diskussion: 2,3-trans-CHA7.2 Diskus
- Seite 122 und 123: Ergebnisse: Reaktivextraktion8 Erge
- Seite 124 und 125: Ergebnisse: Reaktivextraktiongrades
- Seite 126 und 127: Ergebnisse: Reaktivextraktion3,4-tr
- Seite 128 und 129:
Ergebnisse: Reaktivextraktion2,3-tr
- Seite 130 und 131:
Ergebnisse: Reaktivextraktion250in
- Seite 132 und 133:
Ergebnisse: ReaktivextraktionRaum-Z
- Seite 134 und 135:
Ergebnisse: ReaktivextraktionDurch
- Seite 136 und 137:
Diskussion: Reaktivextraktion8.4 Di
- Seite 138 und 139:
Diskussion: ReaktivextraktionDie Ur
- Seite 140 und 141:
Diskussion: ReaktivextraktionVergle
- Seite 142 und 143:
Diskussion: ReaktivextraktionDas Pr
- Seite 144 und 145:
Zusammenfassung9 ZusammenfassungIm
- Seite 146 und 147:
Ausblick10 AusblickDie drei Produkt
- Seite 148 und 149:
AusblickOptimierung der Reaktivextr
- Seite 150 und 151:
Literaturverzeichnis11 Literaturver
- Seite 152 und 153:
LiteraturverzeichnisGibson DT, Koch
- Seite 154 und 155:
LiteraturverzeichnisMüller R, Breu
- Seite 156 und 157:
LiteraturverzeichnisWieczorek S, Br
- Seite 158 und 159:
Anhang12 Anhang12.1 Zusammensetzung
- Seite 160 und 161:
Anhang12.1.6 Zulaufmedien: Glukose
- Seite 162 und 163:
Anhang12.2.1 Datenblatt der chemisc
- Seite 164 und 165:
AnhangGeräteparameter:stationäre
- Seite 166 und 167:
Anhang2,3-trans-CHD3,4-trans-CHDAbb
- Seite 168 und 169:
AnhangAbb. 12.3:1 H-NMR-Spektrum de
- Seite 170 und 171:
AnhangSauerstoffelektrode 12 mm Oxy
- Seite 172 und 173:
Anhang Bei dem Einsatz des accutren
- Seite 174 und 175:
AnhangAbb. 5.6:Abb. 5.7:Abb. 5.8:Ab
- Seite 176 und 177:
AnhangAbb. 6.15: Gegenüberstellung
- Seite 178:
Anhang12.8 TabellenverzeichnisTab.
- Seite 181 und 182:
Schriften des Forschungszentrums J
- Seite 183:
Schriften des Forschungszentrums J