JuSER - Forschungszentrum Jülich
JuSER - Forschungszentrum Jülich
JuSER - Forschungszentrum Jülich
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
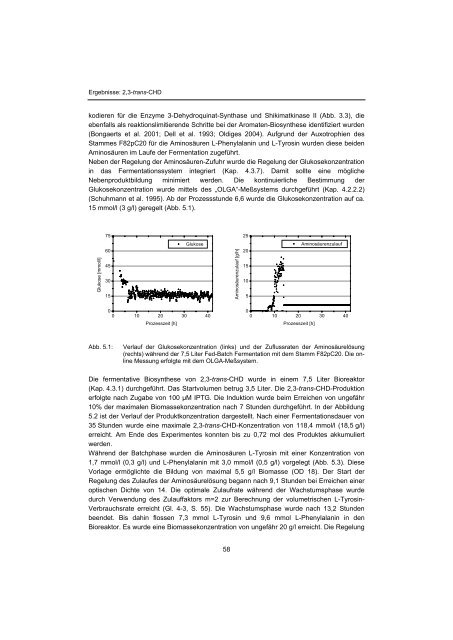
Ergebnisse: 2,3-trans-CHDkodieren für die Enzyme 3-Dehydroquinat-Synthase und Shikimatkinase II (Abb. 3.3), dieebenfalls als reaktionslimitierende Schritte bei der Aromaten-Biosynthese identifiziert wurden(Bongaerts et al. 2001; Dell et al. 1993; Oldiges 2004). Aufgrund der Auxotrophien desStammes F82pC20 für die Aminosäuren L-Phenylalanin und L-Tyrosin wurden diese beidenAminosäuren im Laufe der Fermentation zugeführt.Neben der Regelung der Aminosäuren-Zufuhr wurde die Regelung der Glukosekonzentrationin das Fermentationssystem integriert (Kap. 4.3.7). Damit sollte eine möglicheNebenproduktbildung minimiert werden. Die kontinuierliche Bestimmung derGlukosekonzentration wurde mittels des „OLGA“-Meßsystems durchgeführt (Kap. 4.2.2.2)(Schuhmann et al. 1995). Ab der Prozessstunde 6,6 wurde die Glukosekonzentration auf ca.15 mmol/l (3 g/l) geregelt (Abb. 5.1).7525Glukose [mmol/l]60453015GlukoseAminosäurenzulauf [g/h]2015105Aminosäurenzulauf00 10 20 30 40Prozesszeit [h]00 10 20 30 40Prozesszeit [h]Abb. 5.1:Verlauf der Glukosekonzentration (links) und der Zuflussraten der Aminosäurelösung(rechts) während der 7,5 Liter Fed-Batch Fermentation mit dem Stamm F82pC20. Die onlineMessung erfolgte mit dem OLGA-Meßsystem.Die fermentative Biosynthese von 2,3-trans-CHD wurde in einem 7,5 Liter Bioreaktor(Kap. 4.3.1) durchgeführt. Das Startvolumen betrug 3,5 Liter. Die 2,3-trans-CHD-Produktionerfolgte nach Zugabe von 100 µM IPTG. Die Induktion wurde beim Erreichen von ungefähr10% der maximalen Biomassekonzentration nach 7 Stunden durchgeführt. In der Abbildung5.2 ist der Verlauf der Produktkonzentration dargestellt. Nach einer Fermentationsdauer von35 Stunden wurde eine maximale 2,3-trans-CHD-Konzentration von 118,4 mmol/l (18,5 g/l)erreicht. Am Ende des Experimentes konnten bis zu 0,72 mol des Produktes akkumuliertwerden.Während der Batchphase wurden die Aminosäuren L-Tyrosin mit einer Konzentration von1,7 mmol/l (0,3 g/l) und L-Phenylalanin mit 3,0 mmol/l (0,5 g/l) vorgelegt (Abb. 5.3). DieseVorlage ermöglichte die Bildung von maximal 5,5 g/l Biomasse (OD 18). Der Start derRegelung des Zulaufes der Aminosäurelösung begann nach 9,1 Stunden bei Erreichen eineroptischen Dichte von 14. Die optimale Zulaufrate während der Wachstumsphase wurdedurch Verwendung des Zulauffaktors m=2 zur Berechnung der volumetrischen L-Tyrosin-Verbrauchsrate erreicht (Gl. 4-3, S. 55). Die Wachstumsphase wurde nach 13,2 Stundenbeendet. Bis dahin flossen 7,3 mmol L-Tyrosin und 9,6 mmol L-Phenylalanin in denBioreaktor. Es wurde eine Biomassekonzentration von ungefähr 20 g/l erreicht. Die Regelung58