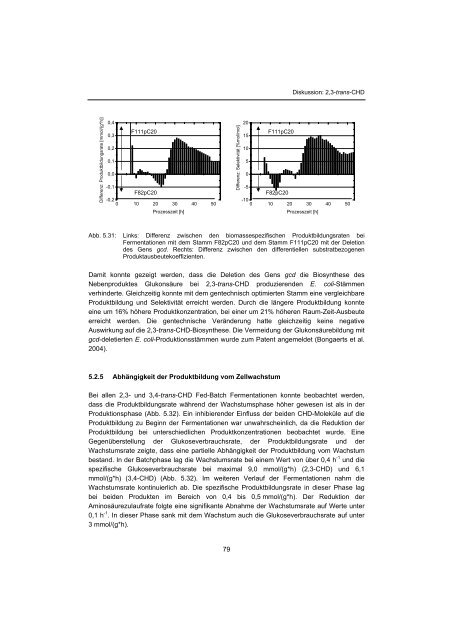
Diskussion: 2,3-trans-CHDDifferenz: Produktbildungsrate [mmol/(g*h)]0,4F111pC200,30,20,10,0-0,1F82pC20-0,20 10 20 30 40 50Prozesszeit [h]Differenz: Selektivität [%mol/mol]20F111pC20151050-5F82pC20-100 10 20 30 40 50Prozesszeit [h]Abb. 5.31: Links: Differenz zwischen den biomassespezifischen Produktbildungsraten beiFermentationen mit dem Stamm F82pC20 und dem Stamm F111pC20 mit der Deletiondes Gens gcd. Rechts: Differenz zwischen den differentiellen substratbezogenenProduktausbeutekoeffizienten.Damit konnte gezeigt werden, dass die Deletion des Gens gcd die Biosynthese desNebenproduktes Glukonsäure bei 2,3-trans-CHD produzierenden E. coli-Stämmenverhinderte. Gleichzeitig konnte mit dem gentechnisch optimierten Stamm eine vergleichbareProduktbildung und Selektivität erreicht werden. Durch die längere Produktbildung konnteeine um 16% höhere Produktkonzentration, bei einer um 21% höheren Raum-Zeit-Ausbeuteerreicht werden. Die gentechnische Veränderung hatte gleichzeitig keine negativeAuswirkung auf die 2,3-trans-CHD-Biosynthese. Die Vermeidung der Glukonsäurebildung mitgcd-deletierten E. coli-Produktionsstämmen wurde zum Patent angemeldet (Bongaerts et al.2004).5.2.5 Abhängigkeit der Produktbildung vom ZellwachstumBei allen 2,3- und 3,4-trans-CHD Fed-Batch Fermentationen konnte beobachtet werden,dass die Produktbildungsrate während der Wachstumsphase höher gewesen ist als in derProduktionsphase (Abb. 5.32). Ein inhibierender Einfluss der beiden CHD-Moleküle auf dieProduktbildung zu Beginn der Fermentationen war unwahrscheinlich, da die Reduktion derProduktbildung bei unterschiedlichen Produktkonzentrationen beobachtet wurde. EineGegenüberstellung der Glukoseverbrauchsrate, der Produktbildungsrate und derWachstumsrate zeigte, dass eine partielle Abhängigkeit der Produktbildung vom Wachstumbestand. In der Batchphase lag die Wachstumsrate bei einem Wert von über 0,4 h -1 und diespezifische Glukoseverbrauchsrate bei maximal 9,0 mmol/(g*h) (2,3-CHD) und 6,1mmol/(g*h) (3,4-CHD) (Abb. 5.32). Im weiteren Verlauf der Fermentationen nahm dieWachstumsrate kontinuierlich ab. Die spezifische Produktbildungsrate in dieser Phase lagbei beiden Produkten im Bereich von 0,4 bis 0,5 mmol/(g*h). Der Reduktion derAminosäurezulaufrate folgte eine signifikante Abnahme der Wachstumsrate auf Werte unter0,1 h -1 . In dieser Phase sank mit dem Wachstum auch die Glukoseverbrauchsrate auf unter3 mmol/(g*h).79
Diskussion: 2,3-trans-CHD86654 Glucose[mmol/(g*h)] Glucose[mmol/(g*h)]4322100,1 0,20,30,40,5 2,3-CHD[mmol/(g*h)]0,00,10,3 0,40,2 [1/h]00,1 0,20,30,40,5 3,4-CHD[mmol/(g*h)]0,00,10,3 0,40,2 [1/h]Abb. 5.32: Gegenüberstellung der Wachstumsrate ( ), der Substratverbrauchsrate ( ) und derProduktbildungsrate ( ) bei der Fermentation mit dem 2,3-trans-CHD-ProduktionsstammF111pC20 (links) und dem 3,4-trans-CHD-Produktionsstamm F82pC22 (rechts).Eine Optimierung des Prozesses könnte durch drei Ansätze bewerkstelligt werden: eineVerlängerung der Wachstumsphase, eine kontinuierliche oder semikontinuierlicheProzessführung und eine Stammverbesserung. Eine Verlängerung der Wachstumsphasegegenüber der Produktionsphase könnte durch die Erhöhung der Biomassekonzentrationerreicht werden. Das kann durch das Aufkonzentrieren des Batch-Mediums erreicht werden.Dadurch könnten die integrale spezifische Produktbildungsrate und die Raum-Zeit-Ausbeuteerhöht werden. Durch die höhere Biomassekonzentration steigt jedoch der Sauerstoffbedarfsignifikant und der substratbezogene Ausbeutekoeffizient der Fermentation nimmt ab. EineÜbertragung dieser Prozessführung in den großtechnischen Ansatz könnte an dem nichtausreichenden Sauerstoffeintrag der Produktionsreaktoren scheitern. Außerdem entstehenKosten bei der Entsorgung der Biomasse.Der Einsatz einer kontinuierlichen oder semikontinuierlichen Prozessführung würde durch diekonstante Zufütterung der Medienbestandteile eine höhere Wachstumsrate über dieFermentationsdauer ermöglichen. Dadurch könnte die spezifische Produktbildungsrate aufeinem höheren Niveau gehalten werden. Aufgrund der hohen Plasmidinstabilität bei denStämmen F82pC20 (Kap. 5.1.1), F111pC20 (Kap. 5.1.3) und F82pC22 (Kap. 6.1) war esnicht möglich, diese Stämme für kontinuierliche Fermentationen einzusetzen. DieKonstruktion neuer Produktionsstämme mit der chromosomalen Integration der Gene entBCund aroBFL oder die Verwendung von Plasmiden mit einer höheren Stabilität würde dieEntwicklung des kontinuierlichen Verfahrens sinnvoll machen.Die Reduktion der Aminosäurenzulaufrate am Ende der Wachstumsphase führte zurAbnahme der Biomassebildung und verursachte eine Veränderung der Stoffwechselflüsse.Aufgrund dessen könnte es zu einer Anhäufung der Metabolite des Pentose-Phosphat-Weges, des TCA-Zyklus und der Glykolyse kommen. Die Akkumulation dieser Metabolitekönnte eine inhibierende Wirkung auf die Produktbildung haben. Zum Beispiel könnte derMetabolit Pyruvat eine Beeinflussung der Produktbildung bewirken. Pyruvat entstehtwährend der Aufnahme von Glukose in die Zelle während der enzymatischen Umwandlungvon Isochorismat zu 2,3-trans-CHD und in der Glykolyse (Abb. 3.2 und 3.5). Pyruvat fließtunter aeroben Bedingungen hauptsächlich über Acetyl-CoA in den TCA-Zyklus ein. Die80
- Seite 8:
DanksagungDanksagungHerrn Prof. Dr.
- Seite 11 und 12:
Inhaltsverzeichnis4.3 Apparativer A
- Seite 13 und 14:
AbkürzungenAbkürzungsverzeichnis:
- Seite 15 und 16:
AbkürzungenF Kraft Ng Erdbeschleun
- Seite 17 und 18:
EinleitungUmweltschutz und der Land
- Seite 20 und 21:
Zielsetzung2 Zielsetzung der Arbeit
- Seite 22 und 23:
Stand des Wissens3 Stand des Wissen
- Seite 24 und 25:
Stand des WissensD-GlukoseptsPyruva
- Seite 26 und 27:
Stand des Wissensisofunktionelle Me
- Seite 28 und 29:
Stand des Wissensmit einer annäher
- Seite 30 und 31:
Stand des WissensDas Produkt 2,3-tr
- Seite 32 und 33:
Stand des Wissens3.3 Verfahrenstech
- Seite 34 und 35:
Stand des Wissens3.3.2.1 Reaktivext
- Seite 36 und 37:
Stand des Wissens-Cl+NTOMAC: CH 3 (
- Seite 38 und 39:
Stand des WissensDie Gleichgewichtk
- Seite 40 und 41:
Stand des Wissensorganische Phasew
- Seite 42 und 43:
Stand des WissensDer Stofftransport
- Seite 44 und 45: Stand des Wissenswd( 2t w org 2 r
- Seite 46 und 47: Stand des WissensDie im Rahmen dies
- Seite 48 und 49: Stand des WissenscP cend P0RZA (3-
- Seite 50: Stand des WissensAnreicherung [%]in
- Seite 53 und 54: Material und MethodenFür die Produ
- Seite 55 und 56: Material und Methoden4.2.2 Bestimmu
- Seite 57 und 58: Material und MethodenAbb. 4.1:Links
- Seite 59 und 60: Material und MethodenDie Kalibrieru
- Seite 61 und 62: Material und Methoden4.3.2 Fermenta
- Seite 63 und 64: Material und MethodenGlucoseL-TyrL-
- Seite 65 und 66: Material und Methoden42 Liter Maste
- Seite 67 und 68: Material und Methoden40 cm10 cmAbb.
- Seite 69 und 70: Material und Methoden4.3.7 Prozessk
- Seite 72 und 73: Ergebnisse: 2,3-trans-CHD5 Ergebnis
- Seite 74 und 75: Ergebnisse: 2,3-trans-CHDder Aminos
- Seite 76 und 77: Ergebnisse: 2,3-trans-CHDZwischen d
- Seite 78 und 79: Ergebnisse: 2,3-trans-CHDGlukonsäu
- Seite 80 und 81: Ergebnisse: 2,3-trans-CHD3 mmol/(l*
- Seite 82 und 83: Ergebnisse: 2,3-trans-CHDWachstumsp
- Seite 84 und 85: Ergebnisse: 2,3-trans-CHD251501002,
- Seite 86 und 87: Diskussion: 2,3-trans-CHD5.2 Diskus
- Seite 88 und 89: Diskussion: 2,3-trans-CHD1,02,0Bild
- Seite 90 und 91: Diskussion: 2,3-trans-CHD2,3-CHD Ac
- Seite 92 und 93: Diskussion: 2,3-trans-CHDCOOHNHCOOH
- Seite 96 und 97: Diskussion: 2,3-trans-CHDAbnahme de
- Seite 98 und 99: Ergebnisse: 3,4-trans-CHD6 Ergebnis
- Seite 100 und 101: Ergebnisse: 3,4-trans-CHDSelektivit
- Seite 102 und 103: Ergebnisse: 3,4-trans-CHD3 mmol/l g
- Seite 104 und 105: Ergebnisse: 3,4-trans-CHD3,4-trans-
- Seite 106 und 107: Ergebnisse: 3,4-trans-CHDtrans-CHD
- Seite 108 und 109: Ergebnisse: 3,4-trans-CHDwährend d
- Seite 110 und 111: Diskussion: 3,4-trans-CHD6.2 Diskus
- Seite 112 und 113: Diskussion: 3,4-trans-CHDChorismat
- Seite 114 und 115: Diskussion: 3,4-trans-CHDführen, d
- Seite 116 und 117: Diskussion: 3,4-trans-CHDNur unter
- Seite 118 und 119: Ergebnisse: 2,3-trans-CHA7 Fermenta
- Seite 120 und 121: Diskussion: 2,3-trans-CHA7.2 Diskus
- Seite 122 und 123: Ergebnisse: Reaktivextraktion8 Erge
- Seite 124 und 125: Ergebnisse: Reaktivextraktiongrades
- Seite 126 und 127: Ergebnisse: Reaktivextraktion3,4-tr
- Seite 128 und 129: Ergebnisse: Reaktivextraktion2,3-tr
- Seite 130 und 131: Ergebnisse: Reaktivextraktion250in
- Seite 132 und 133: Ergebnisse: ReaktivextraktionRaum-Z
- Seite 134 und 135: Ergebnisse: ReaktivextraktionDurch
- Seite 136 und 137: Diskussion: Reaktivextraktion8.4 Di
- Seite 138 und 139: Diskussion: ReaktivextraktionDie Ur
- Seite 140 und 141: Diskussion: ReaktivextraktionVergle
- Seite 142 und 143: Diskussion: ReaktivextraktionDas Pr
- Seite 144 und 145:
Zusammenfassung9 ZusammenfassungIm
- Seite 146 und 147:
Ausblick10 AusblickDie drei Produkt
- Seite 148 und 149:
AusblickOptimierung der Reaktivextr
- Seite 150 und 151:
Literaturverzeichnis11 Literaturver
- Seite 152 und 153:
LiteraturverzeichnisGibson DT, Koch
- Seite 154 und 155:
LiteraturverzeichnisMüller R, Breu
- Seite 156 und 157:
LiteraturverzeichnisWieczorek S, Br
- Seite 158 und 159:
Anhang12 Anhang12.1 Zusammensetzung
- Seite 160 und 161:
Anhang12.1.6 Zulaufmedien: Glukose
- Seite 162 und 163:
Anhang12.2.1 Datenblatt der chemisc
- Seite 164 und 165:
AnhangGeräteparameter:stationäre
- Seite 166 und 167:
Anhang2,3-trans-CHD3,4-trans-CHDAbb
- Seite 168 und 169:
AnhangAbb. 12.3:1 H-NMR-Spektrum de
- Seite 170 und 171:
AnhangSauerstoffelektrode 12 mm Oxy
- Seite 172 und 173:
Anhang Bei dem Einsatz des accutren
- Seite 174 und 175:
AnhangAbb. 5.6:Abb. 5.7:Abb. 5.8:Ab
- Seite 176 und 177:
AnhangAbb. 6.15: Gegenüberstellung
- Seite 178:
Anhang12.8 TabellenverzeichnisTab.
- Seite 181 und 182:
Schriften des Forschungszentrums J
- Seite 183:
Schriften des Forschungszentrums J