JuSER - Forschungszentrum Jülich
JuSER - Forschungszentrum Jülich
JuSER - Forschungszentrum Jülich
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
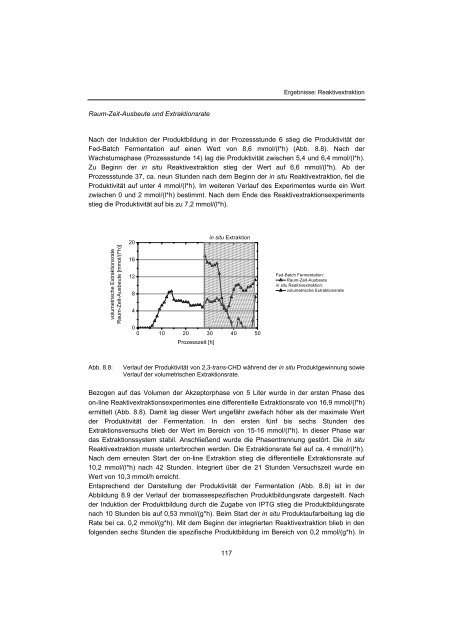
Ergebnisse: ReaktivextraktionRaum-Zeit-Ausbeute und ExtraktionsrateNach der Induktion der Produktbildung in der Prozessstunde 6 stieg die Produktivität derFed-Batch Fermentation auf einen Wert von 8,6 mmol/(l*h) (Abb. 8.8). Nach derWachstumsphase (Prozessstunde 14) lag die Produktivität zwischen 5,4 und 6,4 mmol/(l*h).Zu Beginn der in situ Reaktivextraktion stieg der Wert auf 6,6 mmol/(l*h). Ab derProzessstunde 37, ca. neun Stunden nach dem Beginn der in situ Reaktivextraktion, fiel dieProduktivität auf unter 4 mmol/(l*h). Im weiteren Verlauf des Experimentes wurde ein Wertzwischen 0 und 2 mmol/(l*h) bestimmt. Nach dem Ende des Reaktivextraktionsexperimentsstieg die Produktivität auf bis zu 7,2 mmol/(l*h).volumetrische ExtraktionsrateRaum-Zeit-Ausbeute [mmol/(l*h)]20161284in situ Extraktion00 10 20 30 40 50Prozesszeit [h]Fed-Batch Fermentation:Raum-Zeit-Ausbeutein situ Reaktivextraktion:volumetrische ExtraktionsrateAbb. 8.8:Verlauf der Produktivität von 2,3-trans-CHD während der in situ Produktgewinnung sowieVerlauf der volumetrischen Extraktionsrate.Bezogen auf das Volumen der Akzeptorphase von 5 Liter wurde in der ersten Phase deson-line Reaktivextraktionsexperimentes eine differentielle Extraktionsrate von 16,9 mmol/(l*h)ermittelt (Abb. 8.8). Damit lag dieser Wert ungefähr zweifach höher als der maximale Wertder Produktivität der Fermentation. In den ersten fünf bis sechs Stunden desExtraktionsversuchs blieb der Wert im Bereich von 15-16 mmol/(l*h). In dieser Phase wardas Extraktionssystem stabil. Anschließend wurde die Phasentrennung gestört. Die in situReaktivextraktion musste unterbrochen werden. Die Extraktionsrate fiel auf ca. 4 mmol/(l*h).Nach dem erneuten Start der on-line Extraktion stieg die differentielle Extraktionsrate auf10,2 mmol/(l*h) nach 42 Stunden. Integriert über die 21 Stunden Versuchszeit wurde einWert von 10,3 mmol/h erreicht.Entsprechend der Darstellung der Produktivität der Fermentation (Abb. 8.8) ist in derAbbildung 8.9 der Verlauf der biomassespezifischen Produktbildungsrate dargestellt. Nachder Induktion der Produktbildung durch die Zugabe von IPTG stieg die Produktbildungsratenach 10 Stunden bis auf 0,53 mmol/(g*h). Beim Start der in situ Produktaufarbeitung lag dieRate bei ca. 0,2 mmol/(g*h). Mit dem Beginn der integrierten Reaktivextraktion blieb in denfolgenden sechs Stunden die spezifische Produktbildung im Bereich von 0,2 mmol/(g*h). In117