LUH_LeibnizCampus 19 2017
Ehemaligenmagazin der Leibniz Universität
Ehemaligenmagazin der Leibniz Universität
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Forschungsschwerpunkt | Optische Technologien<br />
Abbildung 3<br />
Das Aptamer wird auf dem Sensor<br />
immobilisiert und ein komplementäres<br />
Oligonukleotid wird<br />
an das Aptamer hybridisiert.<br />
Die ses Oligonukleotid wird durch<br />
das Target des Aptamers verdrängt,<br />
wodurch die optische<br />
Dichte über dem Sensor verringert<br />
wird (a). Dies kann als<br />
Verschiebung der Resonanz ausgelesen<br />
werden (b–d).<br />
unterschiede ist ein direktes<br />
Maß dafür, in welchen geringen<br />
Mengen zu detektierende<br />
Stoffe noch erkannt werden<br />
können. Damit der Sensor jedoch<br />
bestimmte Stoffe selektiv<br />
über den Brechungsindex<br />
nachweisen kann, muss seine<br />
Ober fläche zusätzlich noch<br />
mit einer Funktionalisierungsschicht<br />
versehen werden, an<br />
die die zu detektierenden<br />
Stoffe andocken können und<br />
so den Brechungsindex verändern.<br />
Simples Prägen<br />
für komplexe Sensoren<br />
Für die Herstellung der Sensoren<br />
sind zwei Faktoren entscheidend:<br />
Erstens muss der<br />
Herstellungsprozess für die<br />
Massenproduktion tauglich<br />
und, zweitens, müssen kleinste<br />
Strukturen im Sub-Mikromaßstab<br />
herstellbar sein, die<br />
mehr als hundertmal kleiner<br />
als das menschliche Haar<br />
sind. Aufgrund dieser Randbedingungen<br />
setzten wir thermische<br />
Imprintverfahren ein,<br />
Kraft gepresst, anschließend<br />
gekühlt und vom Polymer<br />
entformt. Als Plastikmaterial<br />
können handelsübliche Materialien<br />
wie beispielsweise Plexiglas<br />
® verwendet werden.<br />
Für die Herstellung des planaroptischen<br />
Plasmonensensors<br />
werden kleine Kanäle mit<br />
einem rechteckigen Querschnitt<br />
von 25 x 25 µm 2 in dünne<br />
Kunststofffolien geprägt<br />
und anschließend mit Epoxidharzkleber<br />
gefüllt. Nach dem<br />
Aushärten dient das Epoxidharz<br />
als Lichtwellenleiter, in<br />
dem Licht geführt werden<br />
kann. Um plasmonische Sensoren<br />
herzustellen, wird zudem<br />
eine 40 nm (0.00004 mm)<br />
dicke Goldschicht auf den<br />
Sensor abgeschieden.<br />
DNA Strukturen sorgen für<br />
Spezifität und Flexibilität<br />
Um das Sensorsystem in eine<br />
diagnostische Plattform zu<br />
überführen, ist eine Funktionalisierung<br />
der SPR-Sensoroberfläche<br />
notwendig. Dazu<br />
werden Aptamere verwendet.<br />
Dr. Kort Bremer<br />
Jahrgang <strong>19</strong>82, studierte Elektronik<br />
an der Hochschule Wismar<br />
und promovierte an der<br />
University of Limerick, Irland.<br />
Nach einem Postdoc an der<br />
City University London, England,<br />
arbeitet Kort Bremer als<br />
Nachwuchsgruppenleiter am<br />
Hannoverschen Zentrum für<br />
Optische Technologien. Kontakt:<br />
kort.bremer@hot.unihannover.de<br />
Aptamere ist dabei wesentlich<br />
für die Spezifität des Sensorsystems:<br />
Die Struktur des Aptamers<br />
ist komplementär zu<br />
3 4<br />
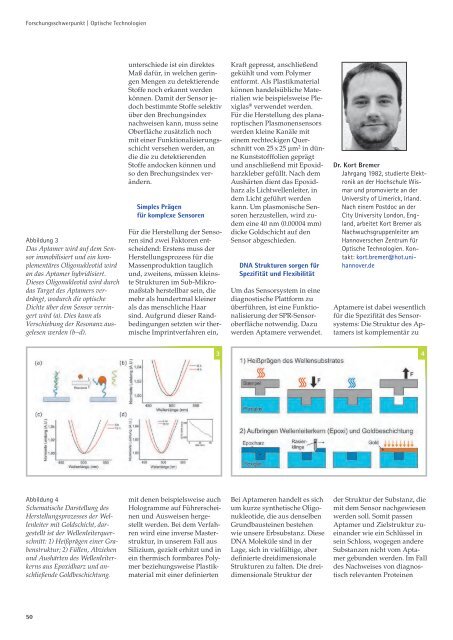
Abbildung 4<br />
Schematische Darstellung des<br />
Herstellungsprozesses der Wellenleiter<br />
mit Goldschicht, dargestellt<br />
ist der Wellenleiterquerschnitt:<br />
1) Heißprägen einer Grabenstruktur;<br />
2) Füllen, Abziehen<br />
und Aushärten des Wellenleiterkerns<br />
aus Epoxidharz und anschließende<br />
Goldbeschichtung.<br />
mit denen beispielsweise auch<br />
Hologramme auf Führerscheinen<br />
und Ausweisen hergestellt<br />
werden. Bei dem Verfahren<br />
wird eine inverse Masterstruktur,<br />
in unserem Fall aus<br />
Silizium, gezielt erhitzt und in<br />
ein thermisch formbares Polymer<br />
beziehungsweise Plastikmaterial<br />
mit einer definierten<br />
Bei Aptameren handelt es sich<br />
um kurze synthetische Oligonukleotide,<br />
die aus denselben<br />
Grundbausteinen bestehen<br />
wie unsere Erbsubstanz. Diese<br />
DNA Moleküle sind in der<br />
Lage, sich in vielfältige, aber<br />
definierte dreidimensionale<br />
Strukturen zu falten. Die dreidimensionale<br />
Struktur der<br />
der Struktur der Substanz, die<br />
mit dem Sensor nachgewiesen<br />
werden soll. Somit passen<br />
Aptamer und Zielstruktur zueinander<br />
wie ein Schlüssel in<br />
sein Schloss, wogegen andere<br />
Substanzen nicht vom Aptamer<br />
gebunden werden. Im Fall<br />
des Nachweises von diagnostisch<br />
relevanten Proteinen<br />
50