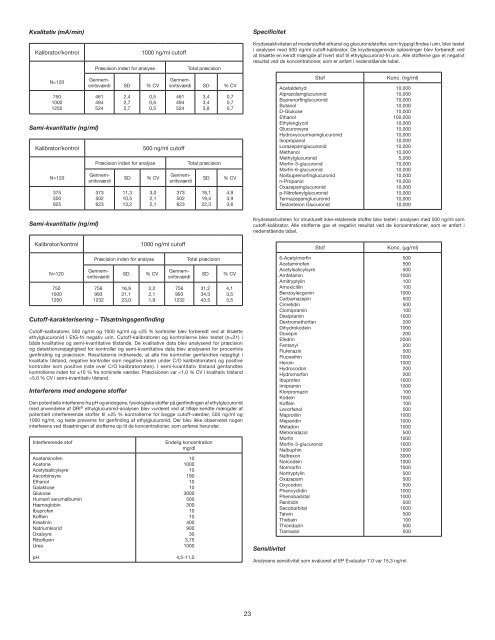
DRI ® ethylglucuronid-analyse Katalognr.: 10011723 (18 ml kit) 10011297 (68 ml kit) 10011226 (500 ml kit) Tilsigtet anvendelse DRI ® ethylglucuronid-enzymimmunanalyse er beregnet til kvalitativ og semi-kvantitativ bestemmelse af ethylglucuronid i human urin ved cutoff-værdier på 500 og 1000 ng/ml. Denne analyse giver kun et præliminært analytisk testresultat. Der skal anvendes en mere specifik, alternativ metode for at opnå et dokumenteret, analytisk resultat. De foretrukne konfirmatoriske metoder er gaskromatografi/flydende kromatografi-massespektometri (GC/MS) og flydende kromatografi/tandem- massespektrometri (LC/MS/MS). Der skal udvises klinisk omtanke og professionel vurdering ved ethvert testresultat til påvisning af misbrug af stoffet, især når der anvendes præliminære positive resultater. Opsummering og forklaring af testen <strong>Ethyl</strong>glucoronid (EtG) er en direkte metabolit af ethanol, som dannes ved den enzymatiske konjugation af ethanol med glucuronsyre. 1,2 Alkohol i urin kan normalt kun påvises i et par timer, hvorimod EtG kan påvises i op til flere dage, selv efter fuldstændig eliminering af alkohol fra kroppen. 3 EtG kan derfor være nyttig som en diagnostisk biomarkør til bestemmelse af nylig alkoholindtagelse og til monitorering af abstinens hos alkoholikere, der deltager i alkoholbehandlingsprogrammer. 4-7 Ethanol kan produceres in vitro pga. fermentation af urinprøver, der indeholder sukker (diabetes), bakterier eller gær, når prøverne eksponeres for varme temperaturer. 8 I sådanne tilfælde kan EtG-testen anvendes som en konfirmatorisk test til at bestemme, om alkoholen i prøven skyldes indtagelse af alkohol, eller den dannes in vitro som et resultat af fermentation. EtG monitoreres på det nuværende tidspunkt af GC/MS og LC/MS/MS. 9-10 DRI ® ethylglucoronid-analysen leveres som en flydende, homogen, brugsklar enzymanalyse. Analysen bruger specifikke antistoffer, som kan påvise ethylglucuronid uden nogen signifikant krydsreaktivitet med andre glucuronidstoffer. Analysen er baseret på konkurrence mellem et medikament mærket med glucose-6-fosfatdehydrogenase (G6PDH) og frit medikament fra urinprøven for en fast mængde af specifikke antistofbindingssteder. Ved fraværet af frit medikament fra prøven binder det specifikke antistof medikamentet mærket med G6PDH og forårsager et fald i enzymaktiviteten. Dette fænomen skaber et direkte forhold mellem medikamentkoncentrationen i urin og enzymaktiviteten. Aktivt enzym omdanner NAD til NADH, hvilket resulterer i en absorbansændring, som kan måles med spektrofotometer ved 340 nm. Reagenser Antistof-/Substratreagens: Indeholder monoklonalt anti-ethylglucuronid-antistof fra mus, glucose-6-fosfat (G6P) og nicotinamid-adenindinukleotid (NAD) i Tris-buffer med natriumazid som konserveringsmiddel. Enzymkonjugatreagens: Indeholder ethylglucuronid-derivat mærket med glucose-6fosfatdehydrogenase (G6PDH) i Tris-buffer med natriumazid som konserveringsmiddel. Nødvendige ekstra materialer (sælges separat): 10011207, DRI ® ethylglucuronid-negativ kalibrator, 25 ml 10011208, DRI ® ethylglucuronid-kalibrator 100 ng/ml, 10 ml 10011210, DRI ® ethylglucuronid-kalibrator 500 ng/ml, 10 ml 10011212, DRI ® ethylglucuronid-kalibrator 1000 ng/ml, 10 ml 10011213, DRI ® ethylglucuronid-kalibrator 2000 ng/ml, 10 ml 10012135, DRI ® ethylglucuronid 375 ng/ml kontrol, 25 ml 10012136, DRI ® ethylglucuronid 625 ng/ml kontrol, 25 ml 10012137, DRI ® ethylglucuronid 750 ng/ml kontrol, 25 ml 10012138, DRI ® ethylglucuronid 1250 ng/ml kontrol, 25 ml Forholdsregler og advarsler 1. Denne test er kun til in vitro diagnostisk anvendelse. Reagenserne er skadelige ved indtagelse. 2. Reagenserne anvendt i analysekomponenterne indeholder natriumazid, som kan reagere med bly- og kobberrør og danne potentielt eksplosive metalazider. Ved bortskaffelse af sådanne reagenser skylles med rigelige mængder vand for at undgå aflejring af azider. 3. Reagenser må ikke anvendes efter udløbsdatoerne er overskredet. Reagensforberedelse og opbevaring Reagenserne er klar til brug. Ingen yderligere forberedelse er nødvendig. Reagenserne bør opbevares i køleskab ved 2-8 °C. Alle analysekomponenter, i åben eller uåben stand, er holdbare indtil udløbsdatoen, som er angivet på deres respektive etiketter. Reagenserne må ikke anvendes efter deres udløbsdatoer er overskredet. Prøvetagning og -håndtering Indsaml urinprøver i plast- eller glasbeholdere. Det foreslås at anvende friske urinprøver. Mandatory Guidelines for Federal Workplace Drug Testing Programs (Obligatoriske retningslinjer for stoftest på offentlige arbejdspladser) anbefaler, at prøver, der ikke testes inden for 7 dage efter modtagelse på laboratoriet, bør placeres i sikrede køleskabe. Urinprøver skal altid opbevares i køleskabet. Prøver, hvor pH-værdien er inden for 4,5 og 11, er egnede til testning med denne analyse. 22 Til in vitro diagnostisk anvendelse Der skal tages tiltag til at holde de pipetterede prøver fri for groft snavs. Centrifuger stærkt uklare prøver før analysen. Forfalskning af urinprøverne kan give fejlagtige resultater. Hvis der er mistanke om forfalskning, skal der opnås en anden prøve, og begge prøver skal fremsendes til laboratoriet mhp. testning. Håndter alle urinprøver, som om de var smitsomme. Analyseprocedure Til denne immunanalyse kan der anvendes kliniske kemianalysatorer, der er i stand til at bibeholde en konstant temperatur, pipettere prøver, blande reagenser, måle hastigheden af enzymatiske reaktioner ved 340 nm og indstille reaktionerne præcist. Se de specifikke anvendelsesinstruktioner for hver analysator vedrørende kemiparametrene, inden analysen foretages. Kvalitetskontrol og kalibrering God laboratoriepraksis foreslår brug af kontrolprøver til at sikre korrekt analysepræstation. Sørg for, at kontrolresultaterne er inden for det fastlagte værdiområde, som fastlagt af laboratorieprocedurer og retningslinjer. Hvis resultaterne falder uden for de fastlagte værdiområder, er analyseresultaterne ugyldige. Brug 500 ng/ml eller 1000 ng/ml kalibrator som cutoff-niveau ved kvalitativ analyse. Brug alle kalibratorer ved semi-kvantitativ analyse. Alle kvalitetskontrolkrav bør udføres i overensstemmelse med lokale og/eller nationale regler eller akkrediteringskrav. Resultater og forventede værdier Kvalitative analyser Der kan anvendes enten 500 ng/ml eller 1000 ng/ml kalibratorer som en cutoff-reference til at skelne “positive” prøver fra “negative” prøver. En prøve, som viser en ændring i absorbansværdi (∆A), der er lig med eller større end den værdi, der blev opnået med cutoff-kalibratoren, anses som positiv. En prøve, som viser en ændring i absorbansværdi (∆A), der er lavere end den værdi, der blev opnået med cutoff-kalibratoren, anses som negativ. Semi-kvantitative analyser Der kan opnås en grov vurdering af ethylglucuronid-koncentrationen i prøverne ved at køre en standardkurve med alle kalibratorer og ved at mængdebestemme prøverne fra standardkurven. Når koncentrationen af EtG i prøven er større end den højeste kalibrator, kan prøven fortyndes med den negative kalibrator og testes igen. Rapporterbart område DRI ® ethyl glucuronid-analysen er beregnet til semi-kvantitativ anvendelse i området mellem 100 ng/ml, den laveste kalibrator, og 2000 ng/ml, værdien af den højeste kalibrator. Begrænsninger 1. Et positivt resultat med anvendelse af DRI ® ethylglucuronid-analysen angiver kun tilstedeværelsen af ethylglucuronid, og korrelerer ikke nødvendigvis med omfanget af fysiologiske og psykologiske virkninger. 2. Præstationskarakteristika for DRI ® ethylglucuronid-analysen er ikke fastlagt med andre legemsvæsker end human urin. 3. Denne DRI ® ethylglucuronid-analyse blev valideret på analysatorer, der anvender en integreret celleskylning. Hvis din analysator ikke har en integreret celleskylning, skal du kontakte den lokale repræsentant for Thermo Fischer <strong>Scientific</strong>. 4. Der skal udvises forsigtighed ved rapportering af resultater, da der er mange faktorer, fx væskeindtagelse og andre biologiske faktorer, som kan påvirke resultatet af en urinprøve. 5. Det er muligt, at andre stoffer end dem, der undersøges i den specifikke undersøgelse, kan påvirke testen og give falske resultater. Typiske præstationskarakteristika Typiske præstationsresultater opnået på Hitachi 917-analysatoren er angivet nedenfor. De resultater, der opnås på de enkelte laboratorier, kan afvige fra disse data. Der henvises til det analysatorspecifikke anvendelsesskema for yderligere præstatationsdata specifikke for analysatoren. Præcision DRI ® ethylglucuronid-kontrollerne (375, 625, 750 og 1250 ng/ml) og cutoff-kalibratorerne (500 og 1000 ng/ml) blev testet i kvalitativ (mA/min) og semi-kvantitativ (ng/ml) tilstand vha. en modificeret NCCLS-protokol. Resultaterne, der præsenteres herunder, blev genereret ved testning af alle prøver i replikater på 6, to gange dagligt i 10 dage. Kvalitativ (mA/min) Kalibrator/kontrol 500 ng/ml cutoff N=120 375 500 625 Præcision inden for analyse Total præcision Gennemsnitsværdi 392 417 439 SD % CV 2,1 2,1 2,0 0,5 0,5 0,5 Gennemsnitsværdi 392 417 439 SD % CV 2,9 3,1 2,7 0,7 0,7 0,6
Kvalitativ (mA/min) Kalibrator/kontrol 1000 ng/ml cutoff N=120 750 1000 1250 Semi-kvantitativ (ng/ml) Præcision inden for analyse Total præcision Gennemsnitsværdi SD % CV 461 494 524 2,4 2,7 2,7 0,5 0,6 0,5 Gennemsnitsværdi SD % CV 461 494 524 Kalibrator/kontrol 500 ng/ml cutoff N=120 375 500 625 Semi-kvantitativ (ng/ml) 3,4 3,4 3,8 Præcision inden for analyse Total præcision Gennemsnitsværdi 373 502 623 SD % CV 11,3 10,5 13,2 3,0 2,1 2,1 Gennemsnitsværdi 373 502 623 Kalibrator/kontrol 1000 ng/ml cutoff N=120 750 1000 1250 0,7 0,7 0,7 SD % CV 18,1 19,4 22,3 Præcision inden for analyse Total præcision Gennemsnitsværdi 756 993 1232 SD % CV 16,9 21,1 23,0 2,2 2,1 1,9 Cutoff-karakterisering – Tilsætningsgenfinding Gennemsnitsværdi 756 993 1232 4,9 3,9 3,6 SD % CV 31,2 34,3 43,5 Cutoff-kalibratorer, 500 ng/ml og 1000 ng/ml og ±25 % kontroller blev forberedt ved at tilsætte ethylglucuronid i EtG-fri negativ urin. Cutoff-kalibratoren og kontrollerne blev testet (n=21) i både kvalitative og semi-kvantitative tilstande. De kvalitative data blev analyseret for præcision og detektionsnøjagtighed for kontroller og semi-kvantitative data blev analyseret for procentvis genfinding og præcision. Resultaterne indikerede, at alle fire kontroller genfandtes nøjagtigt i kvalitativ tilstand, negative kontroller som negative (raten under C/O kalibratorraten) og positive kontroller som positive (rate over C/O kalibratorraten). I semi-kvantitativ tilstand genfandtes kontrollerne inden for ±10 % fra nominelle værdier. Præcisionen var