Lire l'Article - retinavisionetretinaaudition.fr
Lire l'Article - retinavisionetretinaaudition.fr
Lire l'Article - retinavisionetretinaaudition.fr
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Livre.book Page 387 Jeudi, 26. février 2009 3:40 15<br />
NEUROPATHIES OPTIQUES<br />
ET NEURO- OPHTALMOLOGIE<br />
En dehors des neuropathies optiques qui ont été évoquées<br />
dans les chapitres précédents, de nombreuses affections<br />
neuro-ophtalmologiques, au premier rang desquelles les<br />
pathologies oculomotrices, peuvent avoir une origine génétique.<br />
Cette composante génétique est largement suspectée<br />
depuis de nombreuses années en ce qui concerne les strabismes,<br />
bien qu’aucun gène n’ait encore été retrouvé. En revanche,<br />
plusieurs gènes responsables de myasthénies, de<br />
myopathies ou de syndromes de restriction ont été localisés<br />
et/ou identifiés, ce qui permet d’envisager un dépistage pré-<br />
CHAPITRE 27<br />
STRABISME, MYOPATHIES,<br />
NEURO- OPHTALMOLOGIE<br />
C. ORSSAUD<br />
natal ou chez des patients à risque. De plus, le rôle du produit<br />
de certains de ces gènes commence à être connu. Ces<br />
connaissances ont permis de développer un traitement adapté<br />
dans la maladie de Gaucher, souvent responsable de paralysies<br />
supranucléaires. D’autres développements de ces<br />
connaissances devraient suivre, en particulier dans la myopathie<br />
de Duchenne. Il ne faut néanmoins pas oublier le pourcentage<br />
important des formes sporadiques de ces anomalies<br />
oculomotrices le plus <strong>fr</strong>équemment rencontrées, telles que le<br />
syndrome de Stilling-Duane-Türk ou le syndrome de Brown.<br />
I – STRABISMES ET SYNDROMES DE RESTRICTION<br />
Le caractère génétique des strabismes essentiels est suspecté<br />
depuis plus d’un siècle et a donné lieu à de nombreux travaux<br />
[128, 234] . Cependant, aucune des études réalisées n’a permis<br />
d’affirmer de manière définitive le mode selon lequel ces<br />
pathologies ségrègent au sein des différentes <strong>fr</strong>atries [135] .<br />
Certaines études de ségrégations tendent à prouver que la<br />
transmission est de type multifactoriel [83] . En effet, la part de<br />
facteurs tels que la ré<strong>fr</strong>action, elle-même sous la dépendance<br />
de facteurs génétiques, mais aussi de facteurs environnementaux<br />
tels que des troubles gestationnels, influent sur l’apparition<br />
de ces deux pathologies [6, 128, 234] . La notion d’hétérogénéité<br />
génétique des strabismes a été renforcée par une étude de<br />
Parikh [167] . Enfin, on observe des strabismes symptomatiques<br />
au cours de différents syndromes polymalformatifs ou dans le<br />
cadre de pathologies multisystémiques. Le mode de transmission<br />
est alors celui de ces affections. Les syndromes de restriction<br />
ou de fibrose congénitale des muscles oculomoteurs sont<br />
des anomalies non évolutives aboutissant à une limitation des<br />
mouvements actifs et passifs du globe oculaire. La classification<br />
en cinq types établie par Brown a été révisée. Le<br />
syndrome de Stilling-Duane-Türk et celui de Brown sont<br />
considérés comme des entités séparées [135] . Le strabismus fixus,<br />
le syndrome de rétraction verticale et la fibrose congénitale du<br />
muscle droit inférieur sont regroupés au sein du « syndrome de<br />
fibrose congénitale des muscles extraoculaires », désigné par<br />
l’acronyme CFEOM. L’hétérogénéité phénotypique de ces différents<br />
syndromes de restriction est corrélée à une hétérogénéité<br />
génotypique [182] .<br />
GÉNÉTIQUE DES STRABISMES<br />
CONCOMITANTS<br />
De très nombreuses données concernant le caractère génétique<br />
du strabisme ont été publiées depuis que Parinaud, en<br />
1899, a constaté que certaines formes de strabismes essentiels<br />
avaient un caractère héréditaire. Des travaux ultérieurs ont<br />
démontré une plus grande prévalence des strabismes dans les<br />
<strong>fr</strong>atries d’enfants atteints que dans la population générale.<br />
Crone retrouve une incidence du strabisme de 3 % dans la<br />
population générale, mais de 13 % parmi les apparentés<br />
d’enfants strabiques [56] . Le risque pour le <strong>fr</strong>ère ou la sœur<br />
d’un enfant strabique de développer un strabisme est plus faible<br />
lorsque les parents sont eux-mêmes indemnes de strabisme.<br />
Cependant, la <strong>fr</strong>équence du strabisme essentiel, toutes<br />
formes confondues, chez des apparentés d’un patient strabique,<br />
varie de 4 à 65,4 % dans les différentes études portant<br />
sur des ensembles de population d’enfants strabiques avec<br />
analyse de la <strong>fr</strong>atrie [56, 65] . Cette <strong>fr</strong>équence est influencée par<br />
de nombreux facteurs. Elle dépend de l’importance relative de<br />
la forme de strabisme étudiée au sein de la population retenue.<br />
Maumenee retrouve une faible <strong>fr</strong>équence des formes<br />
familiales (15,8 %), mais elle n’a pris en compte que des<br />
enfants porteurs de strabismes congénitaux [130] ; or, l’incidence<br />
des formes familiales serait plus faible dans cette forme<br />
de strabisme que dans les exotropies intermittentes ou les<br />
ésotropies accommodatives [128, 234] . La <strong>fr</strong>équence des formes<br />
familiales dans ces différentes études dépend également des<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 387
Livre.book Page 388 Jeudi, 26. février 2009 3:40 15<br />
apparentés (parents, grands-parents, oncles et tantes, cousins…)<br />
retenus dans l’analyse et des critères pris en compte<br />
pour s’assurer de l’existence ou de l’absence de strabisme au<br />
sein de cette population [183] . Les microstrabismes et certains<br />
strabismes peu importants n’ayant pas nécessité de prise en<br />
charge particulière sont parfois négligés lors des enquêtes<br />
génétiques de ces différentes études, entraînant une sous-estimation<br />
de la <strong>fr</strong>équence des formes familiales.<br />
Une étude portant sur 63 familles fait état d’une concordance<br />
du type de déviation oculaire entre le proposant et les<br />
apparentés au premier degré dans 44,4 % des cas, alors<br />
qu’une discordance n’est retrouvée que dans 11,1 % des cas.<br />
La concordance n’était pas analysable dans les autres <strong>fr</strong>atries<br />
(44,5 %) de cette étude [65] . La <strong>fr</strong>équence élevée des formes<br />
familiales de strabismes, tous types confondus, et des transmissions<br />
directes parent-enfant(s) — retrouvées dans un tiers<br />
des familles —, ainsi que l’existence de patients atteints sur<br />
plusieurs générations, ont fait évoquer une transmission<br />
dominante autosomique à pénétrance incomplète ou codominante<br />
avec un facteur récessif associé [65, 130, 183] . Ce mode de<br />
transmission n’est pas admis par tous les auteurs. Une transmission<br />
de type polygénique et multifactoriel est souvent<br />
évoquée [83, 119] . Le strabisme serait sous la dépendance de facteurs<br />
environnementaux et les facteurs génétiques ne seraient<br />
pas seuls responsables de sa survenue. Les études réalisées<br />
sur des cohortes de jumeaux, triplés ou quadruplés sont<br />
fondamentales. Elles confirment une plus grande concordance<br />
du strabisme chez les jumeaux monozygotes que<br />
chez les jumeaux dizygotes. Ainsi, une méta-analyse portant<br />
sur 206 paires de jumeaux monozygotes et 130 paires<br />
de jumeaux dizygotes retrouve une concordance à 73 % dans<br />
le premier groupe contre seulement 35 % dans le second [169] .<br />
Un tel résultat est en faveur du rôle essentiel du facteur génétique.<br />
Mais elle démontre aussi que des jumeaux monozygotes<br />
peuvent ne pas développer le même type de strabisme, ou<br />
qu’un seul des deux peut être strabique. Cette concordance<br />
incomplète peut s’interpréter de plusieurs manières. Elle constitue<br />
un argument en faveur de l’intervention de facteurs<br />
d’ordre non génétique dans le développement d’un strabisme,<br />
renforçant l’idée d’une transmission multifactorielle. Mais de<br />
telles observations de formes discordantes de strabismes chez<br />
des jumeaux monozygotes peuvent être observées dans le<br />
cadre d’une transmission dominante à pénétrance incomplète.<br />
Elles relèvent uniquement d’une différence de pénétrance<br />
chez des patients ayant un même patrimoine<br />
génétique. Parikh a récemment évoqué la possibilité d’une<br />
hétérogénéité génétique du strabisme lors d’une étude menée<br />
sur sept <strong>fr</strong>atries rassemblant de trois à dix-neuf patients<br />
atteints sur deux à six générations [167] . Lors de cette étude, cet<br />
auteur a retrouvé un locus de susceptibilité génétique pour le<br />
strabisme en 7p22.1 dans une famille avec un lod score très<br />
positif (supérieur à 4,51). Or, aucune liaison génétique n’a pu<br />
être retrouvée au sein des six autres <strong>fr</strong>atries de cette étude.<br />
Les facteurs ethniques constituent des sources de variations<br />
de la prévalence des strabismes ou de la <strong>fr</strong>équence des<br />
différentes formes de strabismes. Ainsi, il est observé une<br />
plus grande prévalence des strabismes chez les patients caucasiens<br />
que chez les patients a<strong>fr</strong>icains ou a<strong>fr</strong>o-américains.<br />
L’ésotropie est plus <strong>fr</strong>équente chez les Caucasiens que chez<br />
les patients d’origine asiatique. Ces derniers développent plus<br />
volontiers une exotropie. Ces variations de prévalence des<br />
strabismes ont vraisemblablement une origine génétique,<br />
mais le facteur génétique peut intervenir de manière indirecte<br />
sur le strabisme. Ainsi, la différence de déviation oculaire<br />
388 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
observée entre les Caucasiens et les Asiatiques peut être<br />
secondaire à la différence de ré<strong>fr</strong>action existant entre ces<br />
populations, elle-même génétiquement déterminée. La myopie,<br />
très souvent corrélée au strabisme divergent, est extrêmement<br />
<strong>fr</strong>équente en Corée. Contrairement à ce qui avait été<br />
évoqué, une plus grande <strong>fr</strong>équence du strabisme chez les<br />
femmes n’a pas été confirmée lors d’études d’autres cohortes<br />
— sex-ratio de 0,49 [65] .<br />
STRABISMES ESSENTIELS<br />
Il est fondamental de pouvoir constituer des groupes homogènes<br />
de patients. Or, les définitions et les critères utilisés<br />
pour regrouper les patients ne sont pas identiques d’une<br />
étude à l’autre, ce qui rend difficile toute comparaison des<br />
résultats. Cependant, tous les travaux s’accordent à reconnaître<br />
qu’il faut séparer les ésotropies des exotropies. S’il existe<br />
des arguments en faveur de l’existence d’un facteur héréditaire<br />
dans l’un et l’autre de ces deux groupes, la <strong>fr</strong>équence des<br />
cas familiaux y est très différente [65, 183, 234] . Les ésotropies<br />
constituent un ensemble de strabismes cliniquement très<br />
variés quant à l’âge de survenue ou le caractère accommodatif.<br />
C’est la raison pour laquelle, dans la plupart des études,<br />
plusieurs sous-groupes d’ésotropies sont constitués et analysés<br />
séparément. Mais il n’existe aucun consensus concernant<br />
les dénominations (strabismes congénitaux, strabismes simples,<br />
strabismes accommodatifs, strabismes avec amblyopie,<br />
strabismes anisométropiques…) et les définitions de ces sousgroupes<br />
[65, 234] . Le diagnostic de strabisme accommodatif est<br />
généralement retenu lorsque le port de la correction optique<br />
permet d’obtenir une disparition complète ou une diminution<br />
notable de l’angle de la déviation oculaire et devant un<br />
rapport AC/A élevé. Mais les critères ré<strong>fr</strong>actifs, avec une<br />
hypermétropie supérieure à + 3 dioptries, ou les critères de<br />
variabilité de l’angle à type d’incomitance loin-près ou<br />
d’intermittence sont parfois également utilisés [6] . En revanche,<br />
les critères retenus pour définir les strabismes congénitaux<br />
sont généralement univoques [130] . Enfin, les patients<br />
porteurs de microtropie ou de strabismes monoculaires sont<br />
généralement exclus des travaux concernant l’hérédité du<br />
strabisme, aussi bien en tant que proposant que dans la<br />
recherche d’apparentés [169] . Les conséquences de ces exclusions<br />
souvent involontaires sur le calcul de la <strong>fr</strong>équence des<br />
strabismes familiaux ont déjà été évoquées.<br />
Ésotropies<br />
Depuis plus d’un siècle, en dehors d’observations isolées, comportant<br />
néanmoins parfois plusieurs <strong>fr</strong>atries, de très nombreuses<br />
études ont été consacrées à la recherche des modes de transmission<br />
et des facteurs génétiques associés aux ésotropies, quelles<br />
que soient leurs caractéristiques cliniques [6, 65, 83, 128, 130, 183, 234] .<br />
L’incidence des formes familiales varie de 13 à 65,4 % lors des<br />
ésotropies, toutes formes confondues, et cette différence peut<br />
s’expliquer par le degré des apparentés pris en compte dans<br />
l’étude. La <strong>fr</strong>équence de l’hérédité diminue en suivant une<br />
courbe de probabilité d’haplotype commun entre les parents ou<br />
la <strong>fr</strong>atrie et les cousins germains (troisième degré) [183] . Cependant,<br />
on connaît des familles au sein desquelles un apparenté<br />
atteint n’est retrouvé qu’au troisième degré, alors que les apparentés<br />
du premier et deuxième degrés sont indemnes. De telles<br />
<strong>fr</strong>atries pourraient en imposer pour une forme non familiale si<br />
la recherche était limitée aux parents les plus proches. Lors<br />
d’une étude portant sur 181 familles, dont 114 au sein desquel-
Livre.book Page 389 Jeudi, 26. février 2009 3:40 15<br />
les on retrouvait plus de deux patients strabiques, 44,7 % des<br />
apparentés atteints se situaient au-delà du deuxième degré [65] .<br />
En revanche, aucune différence significative n’a pu être mise en<br />
évidence entre les différents types de strabismes convergents<br />
[65] . Cependant, la <strong>fr</strong>équence des formes familiales est généralement<br />
variable en fonction du type d’ésotropie considéré [65, 234] .<br />
Ziakas a observé un pourcentage significativement plus élevé<br />
d’apparentés du premier degré strabiques en présence d’une<br />
ésotropie accommodative chez le proposant (26,1 %) que d’une<br />
ésotropie congénitale (14,9 %) ou d’une ésotropie anisométropique<br />
(12,1 %) [234] . Mais la différence n’atteint plus le seuil de la<br />
significativité lorsque l’étude porte sur les apparentés des<br />
deuxième ou troisième degrés. Des résultats identiques sont<br />
signalés à plusieurs reprises [128] .<br />
Il n’y a, à ce jour, aucun consensus quant au mode de<br />
transmission des ésotropies simples ou accommodatives [119] .<br />
Les caractéristiques des transmissions retrouvées sur différents<br />
arbres généalogiques sont volontiers en faveur d’un<br />
mode dominant autosomique. On en veut pour preuve le<br />
nombre important de transmissions entre apparentés du premier<br />
degré, avec des transmissions père-fils et un pourcentage<br />
égal d’hommes et de femmes atteints. Cependant, une transmission<br />
de type polygénique, pouvant relever de deux gènes<br />
ou plus, et/ou multifactorielle ne peut pas être écartée [119] .<br />
Enfin, un locus de susceptibilité pour le strabisme a été<br />
retrouvé dans une famille atteinte d’ésotropie sur le chromosome<br />
7, en 7p22.1 [167] . Quoique les caractéristiques de la<br />
transmission soient en faveur d’une dominance à pénétrance<br />
incomplète, l’analyse des haplotypes au sein de cette famille<br />
ne peut éliminer ni une transmission récessive autosomique<br />
ni une semi-dominance. Enfin, parmi les facteurs environnementaux,<br />
interviennent les troubles de la réfaction. Leur rôle,<br />
plus particulièrement celui de l’hypermétropie moyenne<br />
(jusqu’à + 3,75 dioptries) ou forte (au-delà de + 3,75 dioptries),<br />
est diversement apprécié. Une hypermétropie moyenne<br />
est physiologiquement observée chez les jeunes enfants. Les<br />
patients dont l’hypermétropie est supérieure à + 3,5 dioptries<br />
à l’âge d’un an ont un risque particulièrement important de<br />
développer un strabisme convergent [5] . De plus, l’existence<br />
d’une hypermétropie associée à un antécédent familial de<br />
strabisme augmente le risque de développer une ésotropie<br />
avec un odd ratio à 6,7 [6] . Le risque d’ésotropie est également<br />
important lorsque la ré<strong>fr</strong>action n’évolue pas vers l’emmétropisation<br />
avant l’âge de 4 ans [207] . Les enfants génétiquement<br />
prédisposés à développer un strabisme ne répondraient pas<br />
au stimulus que constitue une vision floue et, de ce fait,<br />
n’auraient pas une accommodation normale. La transmission<br />
de l’hypermétropie est génétiquement déterminée, soit dominante<br />
autosomique soit polygénique. Il serait donc intéressant<br />
de prendre en compte la valeur du rapport AC/A<br />
également impliqué dans le développement des strabismes<br />
partiellement accommodatifs. Ce rapport semble également<br />
transmis selon les lois de l’hérédité, en raison de la grande<br />
concordance de sa valeur chez des jumeaux monozygotes.<br />
Les ésotropies congénitales doivent être considérées à part.<br />
Les facteurs génétiques jouent un rôle certain, comme la <strong>fr</strong>équence<br />
des formes familiales déjà évoquée tend à le prouver.<br />
Mais le rôle de facteurs environnementaux a été également<br />
bien documenté. La prématurité est un facteur <strong>fr</strong>équemment<br />
associé aux ésotropies congénitales, alors que la notion<br />
d’antécédents familiaux favorise les ésotropies accommodatives<br />
[128] . Le pourcentage de prématurité dans les ésotropies<br />
congénitales varie de 2 à 17 %.<br />
Exotropies<br />
Le mode de transmission de l’exotropie pourrait être dominant<br />
autosomique. Toutefois, le rôle de la réfaction dans le développement<br />
d’un strabisme divergent et le mode de transmission de<br />
ce trouble ré<strong>fr</strong>actif sont des paramètres essentiels. On observe<br />
volontiers une myopie ou une évolution vers la myopie chez un<br />
enfant porteur d’une exotropie [5] . De plus, l’exotropie est volontiers<br />
associée à la présence d’une myopie au sein de la famille,<br />
que le proposant soit lui-même myope ou non [127] . Or, la myopie<br />
est généralement transmise selon un mode dominant autosomique<br />
ou polygénique (cf. chapitre 8).<br />
STRABISMES ASSOCIÉS<br />
À DES ANOMALIES GÉNÉRALES<br />
Un strabisme est <strong>fr</strong>équemment observé au cours de nombreux<br />
syndromes polymalformatifs ou de pathologies dégénératives<br />
ou métaboliques. La présence du strabisme est alors<br />
la conséquence d’un trouble du développement craniofacial<br />
ou neurologique. Ces strabismes symptomatiques peuvent<br />
également être secondaires à des désordres neurologiques<br />
évolutifs, quelle qu’en soit l’origine. S’ils n’ont parfois aucune<br />
caractéristique clinique qui les différencie des strabismes<br />
essentiels, ils s’accompagnent volontiers de paralysie ou de<br />
parésie oculomotrice d’origine nucléaire ou supranucléaire. Le<br />
mode de transmission de ces strabismes symptomatiques est<br />
celui des affections auxquels ils sont associés, en sachant que<br />
la plupart des affections métaboliques sont généralement<br />
transmises selon un mode récessif autosomique. Les différentes<br />
étiologies de ces strabismes symptomatiques sont résumées<br />
dans le tableau 27-I.<br />
Les craniosténoses constituent une cause habituelle des<br />
strabismes orbitaires en raison des malpositions musculaires<br />
qu’elles entraînent. La classification clinique des craniosténoses<br />
repose sur la fermeture prématurée d’une ou de plusieurs<br />
sutures. À côté des formes simples, plusieurs syndromes<br />
complexes ont été décrits (tableau 27-II). Le retentissement<br />
cérébral est d’autant plus important que la fermeture de la<br />
suture limite les possibilités d’expansion de la boîte crânienne<br />
comme dans l’oxycéphalie et dans l’acrocéphalosyndactilie<br />
d’Apert. Lorsque la craniosténose s’accompagne d’hypertension<br />
intracrânienne, celle-ci peut se compliquer d’atrophie<br />
optique. La déformation crânienne retentit sur la forme et<br />
l’orientation des orbites ainsi que sur leur écartement, expliquant<br />
l’hypertélorisme et la <strong>fr</strong>équence des strabismes. Outre<br />
leur hétérogénéité phénotypique, les craniosténoses se caractérisent<br />
également par une hétérogénéité génétique. Des anomalies<br />
génétiques ont été retrouvées dans cinq gènes<br />
différents : le gène MSX2, le gène TWIST et les gènes des<br />
récepteurs du FGF de type 1, 2 et 3 [106] (tableau 27-III). Ces<br />
quatre derniers gènes sont impliqués dans la réponse des cellules<br />
au Fibroblast Growth Factor. Des mutations différentes<br />
survenant dans un même gène peuvent être responsables de<br />
plusieurs tableaux cliniques différents, comme dans la maladie<br />
de Crouzon ou l’acrocéphalosyndactilie d’Apert. Le rôle<br />
d’un âge paternel élevé a été évoqué dans la survenue de<br />
mutations de novo responsables de ces craniosténoses, ellesmêmes<br />
corrélées à des perturbations des mécanismes de<br />
réparation de l’ADN des spermatozoïdes [79] .<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 389
Livre.book Page 390 Jeudi, 26. février 2009 3:40 15<br />
TABLEAU 27-I<br />
Localisation génétique et mode de transmission des principales causes de strabisme symptomatique.<br />
Syndrome Localisation chromosomique Gène Mode de transmission<br />
CFEOM1 12p11.2-q12 KIF21A DA ; (RA ?)<br />
CFEOM2 11q13 ARIX RA<br />
CFEOM3 16q24.2-q24.3 DA<br />
Stilling-Duane-Türk 8q13 ; 2q31 ; 22q DA<br />
Brown ?<br />
Mœbius 13q12.2-q13 ; 3q21-q22 ; 10q21.3-q22.1 ; 1p22 DA ; RA ; RLX<br />
Ophtalmoplégie externe progressive del ADNmt Mitochondrial<br />
Kearns-Sayre del ADNmt Mitochondrial<br />
Leigh 9q34.3 SURF-1 RA<br />
AMBLYOPIE<br />
Les bases génétiques de l’amblyopie fonctionnelle sont<br />
encore mal connues. Celle-ci est bien souvent secondaire à un<br />
trouble rétractif, à un nystagmus congénital ou à un strabisme.<br />
Or, le caractère génétique de ces différents facteurs<br />
amblyogènes est clairement établi. Cependant, dans certaines<br />
<strong>fr</strong>atries, l’amblyopie apparaît isolée et une composante héréditaire<br />
semble pouvoir être affirmée.<br />
Les facteurs neurobiologiques jouent un rôle certain dans<br />
le développement du cortex et dans les mécanismes de plasticité<br />
cérébrale. Ainsi, des neurotrophines, le NGF (nerve growth<br />
factor) présent dans le cortex visuel des mammifères, ou le<br />
BDNF (brain-derived neurotrophic factor), pourraient avoir un<br />
390 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
Xp22.2-p22.1 CPDH, E 1α RLX<br />
Sous-unité unité 5<br />
du complexe I<br />
NDUFS7<br />
NDUFV1<br />
NDUFS4<br />
5p15 flavoprotéine<br />
Waardenburg 2q37.3 DA<br />
Joubert 9q34.3 JTS1 RA<br />
11p12-q13.3 CORS2<br />
11p11.2<br />
X <strong>fr</strong>agile Xq27.3 RLX<br />
Cornelia de Lange 3q26.3 DA<br />
Cri du chat 5p DA<br />
Franceschetti 5q32-q33.2 DA<br />
Cat eye Tétrasomie 22 partielle DA<br />
Down Trisomie 21<br />
Patau Trisomie 13-15<br />
DA : dominant autosomique ; RA : récessif autosomique ; RLX : récessif lié au chromosome X.<br />
Mitochondrial<br />
effet protecteur vis-à-vis d’une amblyopie par déprivation [76] .<br />
Ces données suggèrent que ces molécules puissent avoir également<br />
un rôle de remodelage du système visuel en développement,<br />
dépendant de l’activité neuronale [107] . Or, les cellules<br />
rétiniennes présentent une activité électrique spontanée bien<br />
avant la naissance objectivée par des trains d’ondes dont<br />
l’organisation est précise. De même, il a été démontré que<br />
l’inactivation du récepteur aux neurotrophines p75NTR chez<br />
la souris diminue de façon plus ou moins marquée les projections<br />
géniculo-striées [133] . Les récepteurs au glutamate de type<br />
NMDA, impliqués dans la potentialisation à long terme (longterm<br />
potentialisation), ou des facteurs de transcription de type<br />
cAMP/Ca 2+ response element-binding protein participent également<br />
aux mécanismes de plasticité cérébrale [107, 143] . Mais ces<br />
RA
Livre.book Page 391 Jeudi, 26. février 2009 3:40 15<br />
TABLEAU 27-II<br />
Caractéristiques cliniques et mode de transmission des craniosténoses.<br />
Syndrome<br />
de Crouzon<br />
Sutures<br />
Bicoronale<br />
et sagittale<br />
Parfois<br />
lambdoïde<br />
Complications<br />
neurologiques<br />
HTIC<br />
Hydrocéphalie<br />
Syndrome de Pfeiffer Diffuse HTIC<br />
Hydrocéphalie<br />
Syndrome<br />
de Crouzon<br />
et acanthosis nigricans<br />
Acrocéphalosyndactilie<br />
d’Apert (type 1)<br />
Syndrome<br />
de Saethre-Chotzen, ou<br />
acrocéphalosyndactilie<br />
de type III<br />
Coronale<br />
et sagittale<br />
Parfois<br />
lambdoïde<br />
HTIC<br />
Arnold Chiari<br />
Sténose de<br />
l’orifice jugulaire<br />
Diffus HTIC possible<br />
Hydrocéphalie<br />
Retard mental<br />
Unicoronale<br />
Rarement<br />
bicoronale<br />
Métopique<br />
différentes molécules semblent être aussi impliquées dans<br />
l’embryogenèse cérébrale. Ainsi, l’absence de récepteur NR1<br />
au NMDA stimule le développement de projections callosales<br />
vers les aires visuelles chez la souris. De nombreuses substances<br />
participent à la mise en place de la voie rétino-géniculostriée<br />
ou à l’embryogenèse du cortex visuel et commencent à<br />
être bien connues : la netrine-1 impliquée dans le guidage des<br />
cônes de croissance des axones, les sémaphorines, en particulier<br />
Sema3A et Sema5A, ou les éphrines, facteurs diffusibles<br />
présentant également un rôle inhibiteur dans la guidance axonale<br />
[163] . Il faut également souligner le rôle de ZIF268, dont<br />
l’activité est modulée par l’activité rétinienne. La multiplicité<br />
Autres<br />
anomalies<br />
Complication<br />
ophtalmologique<br />
Hypoplasie maxillaire AO par HTIC<br />
Exorbitisme et<br />
luxation du globe<br />
Hypertélorisme<br />
Anomalies auditives<br />
Sténose trachéale<br />
Ptosis<br />
Exorbitisme<br />
Hypertélorisme<br />
Acanthosis nigricans AO par HTIC<br />
Exorbitisme et<br />
luxation du globe<br />
Hypertélorisme<br />
Syndactilie totale<br />
ou partielle<br />
Anomalies des<br />
vertèbres cervicales<br />
Syndactylie<br />
(4 e -5 e doigts)<br />
Anomalies auditives<br />
Anomalies des<br />
vertèbres cervicales<br />
Hypertélorisme<br />
Exorbitisme<br />
AO par HTIC<br />
Hypertélorisme<br />
Obliquité<br />
antimongoloïde<br />
Blépharophimosis<br />
de ces différents facteurs, qui constituent autant de candidats<br />
au développement d’une amblyopie, et la difficulté de leur<br />
analyse in vivo chez l’homme, ne permettent pas pour l’instant<br />
de préciser les mécanismes physiopathogéniques et<br />
génétiques de l’amblyopie.<br />
HYPERTHERMIE MALIGNE<br />
Fréquence<br />
du strabisme<br />
36 %<br />
Xt > Et<br />
Présent<br />
Fréquence<br />
inconnue<br />
36 %<br />
Xt > Et<br />
Transmission<br />
DA<br />
Sporadique<br />
(âge paternel<br />
élevé)<br />
DA<br />
Sporadique<br />
(âge paternel<br />
élevé)<br />
DA<br />
Sporadique<br />
52 % DA<br />
Sporadique<br />
(âge paternel<br />
élevé)<br />
Présent<br />
Fréquence<br />
inconnue<br />
Scaphocéphalie Sagittale Rares 22 %<br />
Xt > Et<br />
Plagiocéphalie Unicoronale Orbite agrandie<br />
Ascension du globe<br />
oculaire<br />
Brachycéphalie Bicoronale HTIC Exophtalmie<br />
Hypertélorisme<br />
Obliquité<br />
antimongoloïde<br />
Oxycéphalie Multiples<br />
Crâne en « pain<br />
de sucre »<br />
53 %<br />
Hypertropie<br />
et hyperaction<br />
de l’OS<br />
DA<br />
Sporadique<br />
DA RA (?)<br />
Sporadique<br />
DA<br />
Sporadique<br />
38 % DA<br />
Sporadique<br />
HTIC AO par HTIC 28 % DA RA (?)<br />
Sporadique<br />
Trigonocéphalie Métopique Hypertélorisme<br />
Paroi orbitaire<br />
interne verticalisée<br />
18 %<br />
Xt > Et<br />
HTIC : Hypertension intracrânienne ; AO : Atrophie optique ; DA : Dominant autosomique ; RA : Récessif autosomique.<br />
AD<br />
Sporadique<br />
Si la prise en charge thérapeutique du strabisme et les différentes<br />
techniques chirurgicales n’ont pas à apparaître dans ce<br />
chapitre, en revanche, l’hyperthermie maligne, génétique-<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 391
Livre.book Page 392 Jeudi, 26. février 2009 3:40 15<br />
TABLEAU 27-III<br />
Gènes impliqués dans les craniosténoses.<br />
Localisation Craniosténose Type d’anomalie génétique<br />
MSX2 5q34-q35 Turbrachycéphalie (type Boston) Mutation (Pro148His)<br />
TWIST 7p21 Syndrome de Saethre-Chotzen Mutations responsables de perte de fonction<br />
RFGF 1 8p11.2-p11.1 Syndrome de Pfeiffer Une mutation (gain de fonction)<br />
RFGF 2 10q26 Maladie de Crouzon<br />
Syndrome de Pfeiffer<br />
ment déterminée, doit y être traitée car elle constitue la complication<br />
peropératoire gravissime d’une intervention de<br />
strabisme sous une anesthésie générale utilisant des produits<br />
halogénés.<br />
Rien ne permet de laisser présager un tel accident. C’est la<br />
raison pour laquelle des enfants d’une même <strong>fr</strong>atrie ne doivent<br />
jamais être anesthésiés le même jour, ou à tout le moins<br />
avant que le précédent n’ait été totalement réveillé sans incident.<br />
Sa <strong>fr</strong>équence est d’un pour 10 000 à un pour 8 500 [66] .<br />
Cet accident nécessite dans un premier temps d’injecter du<br />
Dentrolène avant une prise en charge en réanimation. Celui-ci,<br />
qui a été préconisé par voie orale en prévention, agit en interférant<br />
avec le relargage de calcium à partir du réticulum sarcoplasmique.<br />
Il permet ainsi de diminuer le couplage entre<br />
l’excitation nerveuse à la surface de la fibre musculaire et la<br />
contraction de celle-ci qui intervient par relargage de calcium<br />
dans le cytoplasme.<br />
L’hyperthermie maligne est due à un désordre du contrôle<br />
du relargage du calcium au niveau des fibres musculaires qui<br />
aboutit à ce niveau à une hyperexcitabilité et à une augmentation<br />
du métabolisme. Cette affection est transmise selon un<br />
mode dominant autosomique à pénétrance variable. Plusieurs<br />
gènes ou loci ont été identifiés comme étant génétiquement<br />
liés à cette affection. Robinson estime que le risque de présenter<br />
une poussée d’hyperthermie maligne serait sous la<br />
dépendance et l’interaction de plusieurs de ces gènes [187] ,<br />
mais le gène le plus important et le plus <strong>fr</strong>équemment altéré<br />
en Europe est celui du canal calcique du réticulum sarcoplasmique,<br />
encore dénommé récepteur de la ryanodine, localisé<br />
en 19q13.1. Plus de trente mutations et une délétion dans ce<br />
gène ont été rapportées, responsables d’une diminution du<br />
seuil de contractibilité musculaire et de la sensibilité à la<br />
caféine et aux halogènes volatils [66] . Ce canal calcique situé<br />
au niveau de la membrane du réticulum sarcoplasmique intervient<br />
dans les phénomènes d’amplification du signal calcique.<br />
Le calcium, pénétrant dans la cellule par les canaux calciques<br />
de type L voltage-dépendants, interagit avec quatre à six<br />
récepteurs/canaux du réticulum sarcoplasmique pour produire<br />
un influx. Une liaison génétique a été retrouvée avec<br />
cinq autres loci ou gènes codant des protéines impliquées<br />
dans le contrôle du calcium dans les fibres musculaires ou<br />
392 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
Plusieurs mutations communes entre Crouzon<br />
et Pfeiffer, délétions et insertions<br />
Syndrome d’Apert Mutation Ser252Trp, Ser252Phe et Pro253Arg<br />
Syndrome de Saethre-Chotzen Insertion<br />
Délétion (codons 269 et 270)<br />
Craniosténose unicoronale Délétions<br />
RFGF 3 4p16.3 Maladie de Crouzon avec anomalie cutanée Mutation (Ala391Glu)<br />
dans le couplage excitation-contraction [40] . Citons le gène de<br />
la sous-unité 1α du canal calcique de type L voltage-dépendant<br />
(1q32) et celui de la sous-unité δ/α2 du canal calcique<br />
voltage-dépendant (7q21-q22) et les loci 3q13.1, 5p et<br />
17q11.2-q24. En ce sens, l’hyperthermie maligne apparaît<br />
comme une affection entrant dans le vaste cadre des canalopathies.<br />
Le test permettant un diagnostic des sujets à risque dans<br />
une <strong>fr</strong>atrie nécessite de disposer de <strong>fr</strong>agments de tissus musculaires<br />
du patient, qui sont soumis à un test de contraction<br />
in vitro à l’aide de caféine ou d’halothane. Des discordances<br />
dans les résultats de ce test permettent de penser qu’il dépend<br />
des mutations causales. C’est la raison pour laquelle il est<br />
proposé d’utiliser également la ryanodine, alcaloïde végétal,<br />
et de pratiquer une recherche de mutation dans le gène du<br />
récepteur de la ryanodine [185] . Le risque de cette pathologie<br />
grave impose de ne pas anesthésier en même temps deux<br />
enfants de la même <strong>fr</strong>atrie, a fortiori des jumeaux.<br />
GÉNÉTIQUE DES SYNDROMES<br />
DE RESTRICTION<br />
Les trois formes de syndromes de restriction seront successivement<br />
envisagées : les syndromes de fibrose congénitale des<br />
muscles oculomoteurs, le syndrome de Stilling-Duane-Türk<br />
et le syndrome de Brown.<br />
SYNDROMES DE FIBROSE CONGÉNITALE<br />
DES MUSCLES OCULOMOTEURS<br />
L’apport de la génétique a permis d’individualiser trois formes<br />
de fibrose congénitale des muscles oculomoteurs<br />
(CFEOM, Congenital Fibrosis of the ExtraOcular Muscles), dont<br />
les gènes sont localisés sur des chromosomes différents. Le<br />
gène du CFEOM de type 1 (CFEOM1), transmis le plus souvent<br />
selon le mode dominant autosomique, est localisé au<br />
niveau de la région centromérique du chromosome 12 alors<br />
que le gène du CFEOM de type 3 (CFEOM3), transmis selon<br />
le même mode, est localisé sur le bras long du chromo-
Livre.book Page 393 Jeudi, 26. février 2009 3:40 15<br />
some 16, en 16q24.2-q24.3 [63, 70] . Le CFEOM de type 2<br />
(CFEOM2) résulte de mutations au sein du gène ARIX, localisé<br />
sur le bras long du chromosome 11, en 11q13. Sa transmission<br />
est récessive autosomique [148] .<br />
CFEOM1<br />
Symptomatologie<br />
La symptomatologie de la forme classique du CFEOM<br />
(CFEOM1) est très stéréotypée. Un ptosis congénital, dont<br />
l’importance varie d’un sujet à l’autre au sein d’une même <strong>fr</strong>atrie<br />
et qui peut être asymétrique, et une limitation des mouvements<br />
oculaires verticaux sont retrouvés chez tous les patients<br />
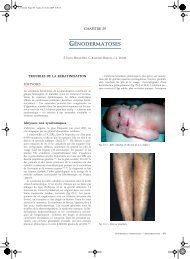
(fig. 27-1) [123] . Au repos, les yeux sont déviés en hypotropie<br />
[194] . Ils ne peuvent pas dépasser la ligne horizontale tant<br />
lors des mouvements volontaires qu’au cours du test de duction<br />
forcée [70, 123] . Les mouvements horizontaux peuvent être<br />
totalement bloqués ou, à l’inverse, d’amplitude normale mais<br />
uniquement réalisés dans l’hémichamp inférieur [70] . Les strabismes<br />
horizontaux à type d’ésotropie ou d’exotropie sont <strong>fr</strong>équents<br />
et peuvent se majorer ou diminuer lors des efforts de<br />
verticalisation des globes [70, 194] . Le ptosis et la limitation des<br />
mouvements oculomoteurs verticaux obligent le patient à<br />
adopter une position compensatrice de la tête, menton relevé<br />
et éventuellement tête tournée dans le sens de la déviation<br />
horizontale [123] . Cette atteinte oculomotrice congénitale est<br />
isolée et non évolutive. La motilité intrinsèque est normale.<br />
Des troubles de la ré<strong>fr</strong>action à type d’astigmatisme sont souvent<br />
rapportés. En raison de la présence de ces différentes<br />
anomalies, le risque d’amblyopie est élevé, nécessitant une<br />
rééducation adaptée précoce [123] . Un traitement chirurgical<br />
peut être proposé pour réduire la position vicieuse de la tête,<br />
le ptosis et améliorer l’alignement des yeux [123] .<br />
Il était généralement admis que la symptomatologie du<br />
CFEOM1 était uniforme, mais la localisation du gène dans la<br />
région centromérique du chromosome 12 a permis de<br />
démontrer l’existence d’une hétérogénéité phénotypique au<br />
sein de certaines <strong>fr</strong>atries. Ainsi, dans une même famille certains<br />
patients sont porteurs d’anomalies oculomotrices évoquant<br />
un CFEOM de type 3 (CFEOM3).<br />
Physiopathogénie<br />
L’origine de ce syndrome semble être neurogène et non myogène<br />
[69] . L’examen anatomopathologique d’un patient atteint<br />
Fig. 27-1 – Patient porteur d’une ophtalmoplégie associée à un ptosis<br />
dans le cadre d’un syndrome de fibrose congénitale des muscles<br />
oculomoteurs (CFEOM). Les yeux sont en exotropie modérée et ne<br />
peuvent pas dépasser la ligne horizontale. (Collection de J.-L. Dufier.)<br />
de CFEOM1 a révélé une anomalie de différenciation de la<br />
portion supérieure des noyaux des nerfs moteurs oculaires<br />
communs, destinée aux muscles releveur de la paupière supérieure<br />
et droit supérieur [153] . Les anomalies musculaires observées<br />
seraient secondaires à une absence d’innervation.<br />
Plusieurs observations de syncinésie d’innervation ou d’innervation<br />
aberrante au cours du CFEOM1 sont également en<br />
faveur de l’hypothèse d’une anomalie du développement des<br />
nerfs crâniens. Ainsi, chez une enfant de neuf mois atteinte<br />
de CFEOM, la stimulation des dents ou de la gencive supérieure<br />
droite entraînait une élévation de l’œil droit, évoquant<br />
une innervation anormale du muscle droit supérieur par un<br />
rameau issu du nerf trijumeau [80] . Un syndrome de Marcus<br />
Gunn unilatéral a été rapporté chez une enfant dont le ptosis<br />
était bilatéral dans le cadre d’une CFEOM [72] . Une cocontraction<br />
anormale des muscles horizontaux ou des mouvements<br />
de convergence ont été rapportés lors des efforts d’élévation<br />
ou d’abaissement des globes [72, 194] . Une anomalie de développement<br />
de certains nerfs crâniens est également retrouvée au<br />
cours d’autres anomalies oculomotrices congénitales, dont<br />
le syndrome de Stilling-Duane-Türk ou le syndrome de<br />
Mœbius, dont les mécanismes physiopathogéniques se rapprochent<br />
ainsi de ceux du CFEOM1. Rappelons le rôle joué<br />
par les crêtes neurales et les rhombomères dans le développement<br />
du rhombencéphale et des nerfs crâniens.<br />
Génétique<br />
La prévalence du syndrome de fibrose des muscles extraoculaires,<br />
quelle que soit sa forme, est estimée à un pour 230 000<br />
dans le Wessex. Le CFEOM1 est observé dans toutes les<br />
régions du globe [70, 194] . Le mode de transmission dominant<br />
autosomique est habituel puisque le sex-ratio est égal à 1, la<br />
consanguinité est toujours absente au sein des familles et des<br />
transmissions père-fils ont été observées sur plus de trois<br />
générations [123, 194] . La pénétrance est dite complète, bien que<br />
de rares observations de pénétrance incomplète aient été<br />
rapportées [24, 70, 194] . Cependant, le mode de transmission du<br />
CFEOM1 pourrait être hétérogène [194, 211] . En effet, un<br />
CFEOM est transmis selon un mode récessif autosomique au<br />
sein d’une famille consanguine présentant une probable<br />
liaison génétique avec la région incluant le gène du<br />
CFEOM1 [211] . Toutefois, la structure de cette famille, ne comportant<br />
qu’un petit nombre de membres, ne permet pas d’éliminer<br />
la présence d’un second gène du CFEOM2, de<br />
transmission récessive autosomique, sur le chromosome 12.<br />
Le CFEOM1 est dû à l’existence de mutations dans le gène<br />
KIF21A, localisé au niveau du bras long du chromosome 12 à<br />
proximité du centromère. Ce grand gène de 38 exons qui<br />
code une kinésine, s’exprime dans l’embryon murin au<br />
jour 10,5, ce qui correspond à la cinquième semaine chez<br />
l’embryon humain. Cette période correspond à celle où le<br />
système oculomoteur se met en place. Les kinésines sont,<br />
avec les dynéines, des protéines responsables du transport<br />
intracellulaire associé aux microtubules. Dans les neurones,<br />
les kinésines sont impliquées dans le transport antérograde. À<br />
ce jour, six mutations faux-sens différentes ont été retrouvées,<br />
dont quatre dans plusieurs <strong>fr</strong>atries. Ces mutations aboutissent<br />
à des modifications d’acides aminés hautement<br />
conservés et situés pour la plupart au niveau d’un repliement<br />
en hélice α de la protéine. Il est probable que ces mutations<br />
aient un effet négatif sur les interactions que la protéine établit<br />
avec d’autres facteurs non identifiés. Ainsi, ces mutations<br />
pourraient altérer le transport d’éléments essentiels au développement<br />
des axones ou de leur terminaison synaptique.<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 393
Livre.book Page 394 Jeudi, 26. février 2009 3:40 15<br />
CFEOM3<br />
Symptomatologie<br />
La variabilité phénotypique au sein d’une même <strong>fr</strong>atrie est un<br />
élément diagnostique du CFEOM3 [63] . Les manifestations<br />
oculomotrices retrouvées chez certains patients sont identiques<br />
à celles rapportées lors du CFEOM1. Le ptosis est<br />
minime ou absent chez d’autres patients pour lesquels on<br />
n’observe ni déviation oculaire ni position anormale de la<br />
tête. Mais l’étude de la motilité oculaire confirme une limitation<br />
portant principalement sur l’élévation, parfois in<strong>fr</strong>aclinique<br />
et nécessitant une exploration au coordimètre. Il est<br />
admis que pour évoquer un CFEOM3, il est nécessaire qu’au<br />
moins un patient atteint de la <strong>fr</strong>atrie ne présente pas un<br />
tableau évocateur de CFEOM1, soit du fait de l’absence de<br />
ptosis soit du fait de l’absence de déviation inférieure des globes<br />
oculaires en position de repos. Cependant, en étudiant<br />
onze familles dont les caractéristiques cliniques et la transmission<br />
génétique sont parfaitement concordantes avec un<br />
CFEOM1, Engle a montré que la présentation clinique et le<br />
mode de pénétrance ne sont pas suffisants pour différencier<br />
les CFEOM de type 1 de ceux de type 3 [70] . En effet, une<br />
liaison génétique avec le gène du CFEOM1 n’a été retenue<br />
que pour deux familles et a été exclue ou considérée comme<br />
improbable pour deux autres familles. Une liaison génétique<br />
avec le gène du CFEOM3 est simplement possible au sein de<br />
trois familles.<br />
Les examens tomodensitométriques pratiqués chez des<br />
patients atteints de CFEOM3 permettent de penser que ses<br />
mécanismes physiopathogéniques seraient identiques à ceux<br />
évoqués pour le CFEOM1 [63, 122] .<br />
Génétique<br />
Le gène du CFEOM3 a d’abord été localisé au niveau de la<br />
portion terminale du bras long du chromosome 16 (16qter)<br />
par Doherty qui a testé 162 marqueurs répartis sur l’ensemble<br />
du génome humain [63] . À l’aide de 22 marqueurs répartis sur<br />
ce <strong>fr</strong>agment du chromosome 16 et de l’analyse des événements<br />
de recombinaison au sein d’une <strong>fr</strong>atrie, cette localisation<br />
a été affinée. Le gène est situé dans une région de<br />
5,6 cM, ou 3,7 Mb, limitée par les marqueurs D16S486 et<br />
D16S671 et correspondant à la région cytogénétique 16q24.2q24.3.<br />
Aucun des vingt gènes localisés dans ou à proximité de<br />
cette région n’a pu être retenu comme gène candidat compte<br />
tenu de la physiopathogénie probable du CFEOM3. La désignation,<br />
parmi eux, d’un gène candidat pourrait être facilitée<br />
par l’analyse des profils d’expression. En effet, certains transcrits<br />
de cette région ne sont retrouvés que dans des librairies<br />
d’expression (tag sequences) de système nerveux central de<br />
l’enfant ; le ou les gènes correspondants pourraient constituer<br />
le ou les candidats. Mais, avant d’envisager d’entreprendre<br />
une approche de type gène candidat, il serait souhaitable de<br />
réduire encore la taille de cette région [63] .<br />
CFEOM2<br />
Symptomatologie<br />
Le CFEOM2 a été décrit en 1998 à partir de l’étude de trois<br />
familles consanguines d’origine saoudienne puis au sein d’une<br />
<strong>fr</strong>atrie d’origine turque [148, 227] . Ce syndrome de restriction est<br />
caractérisé par un ptosis bilatéral très marqué et une ophtalmoplégie<br />
congénitale non évolutive et totale. Tous les mou-<br />
394 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
vements oculaires sont absents, en dehors de l’abduction qui<br />
demeure très limitée. Les globes oculaires sont bloqués en<br />
exodéviation de plus de 50 dioptries prismatiques, à laquelle<br />
peut s’associer une déviation verticale unilatérale à type<br />
d’hypertropie plus que d’hypotropie. Le test de duction forcée<br />
confirme le syndrome de restriction. Cependant, une<br />
variabilité clinique est possible (fig. 27-2). Les globes oculaires<br />
peuvent être fixés en position orthophorique ou atteints de<br />
façon asymétrique, laissant persister des mouvements de verticalité.<br />
Le ptosis est généralement amblyogène et la vision<br />
binoculaire absente. De plus, des anomalies des muscles<br />
intrinsèques de l’œil ont été observées chez les patients les<br />
plus âgés sous forme d’un trouble du jeu pupillaire. Les<br />
pupilles sont bloquées en myosis ou peu réactives à la<br />
lumière et aux collyres myotiques.<br />
Les mécanismes physiopathogéniques du CFEOM2 sont<br />
peu différents de ceux évoqués pour le CFEOM1 et le syndrome<br />
de Mœbius. Le CFEOM2 serait lié à une anomalie de<br />
développement de l’ensemble des complexes nucléaires formant<br />
les noyaux des nerfs moteurs oculaires communs et trochléaires<br />
[227] . Il existe donc une implication des cellules des<br />
crêtes neurales et des rhombomères. Ainsi, cette anomalie de<br />
développement ne laisserait subsister que l’innervation du<br />
muscle droit latéral, issue du noyau protubérantiel du nerf<br />
abducens (moteur oculaire externe).<br />
Fig. 27-2 – Syndrome de fibrose congénitale des muscles oculomoteurs<br />
(CFEOM) très asymétrique. L’œil gauche de ce patient ne peut dépasser<br />
la ligne horizontale et reste en exotropie. (Collection de J.-L. Dufier.)<br />
Génétique<br />
Le CFEOM2 est transmis selon un mode récessif autosomique.<br />
Ce syndrome est dû à la présence de trois mutations au<br />
niveau du gène ARIX (PHOX2A), localisé en 11q13 [148] . Chacune<br />
de ces mutations est associée à un haplotype différent<br />
retrouvé au sein des trois familles saoudiennes et de la<br />
famille d’origine turque. Deux des mutations ont été retrouvées<br />
respectivement à la jonction intron-exon 1 et exon 3intron<br />
de ce gène. Elles pourraient l’une et l’autre aboutir soit<br />
à la synthèse d’un ARN messager incomplet et/ou instable,<br />
soit à la synthèse d’une protéine tronquée et non fonctionnelle.<br />
La troisième mutation dans l’exon 1 entraîne la substitution<br />
d’un acide aminé hautement conservé entre les<br />
espèces au niveau de l’un des sous-domaines de ce gène<br />
(domaine brachyury-like). Le gène Arix (Phox2a) murin a un<br />
rôle essentiel dans le développement et la survie des neurones<br />
adrénergiques ainsi que dans la détermination du phéno-
Livre.book Page 395 Jeudi, 26. février 2009 3:40 15<br />
type des récepteurs adrénergiques. Il joue également un rôle<br />
dans le développement et la survie de neurones du tronc<br />
cérébral, en particulier dans la mise en place des motoneurones<br />
des noyaux du nerf moteur oculaire commun et du nerf<br />
trochléaire [168] . Le knock-out du gène Arix (Phox2a) chez la<br />
souris ou la mutation du gène Arix du poisson zèbre aboutit<br />
à l’absence de ces deux noyaux oculomoteurs, mais aussi du<br />
locus coeruleus et de plusieurs autres nerfs crâniens [168] . Les<br />
souris Arix –/– sont incapables de se nourrir et meurent à la<br />
naissance. Les anomalies observées au niveau des noyaux<br />
oculomoteurs chez ces souris de génotype Arix –/– sont en<br />
conformité avec les mécanismes physiopathogéniques évoqués<br />
chez l’homme dans le cadre du CFEOM2. Mais les<br />
mutations du gène ARIX ne sont pas responsables chez<br />
l’homme d’un phénotype aussi sévère que celui constaté<br />
chez l’animal. Les raisons de cette différence ne sont pas élucidées.<br />
On évoque l’existence de mécanismes de compensation<br />
à partir de gènes voisins, tels que le gène PMX2B<br />
(PHOX2B) qui possède une grande homologie avec le gène<br />
ARIX, ou une dissociation entre le rôle de ce gène dans la<br />
mise en place des noyaux oculomoteurs et le développement<br />
des autres structures du tronc cérébral [148] .<br />
SYNDROME DE STILLING-DUANE-TÜRK<br />
Le syndrome de Stilling-Duane-Türk (SSDT) est l’un des syndromes<br />
de fibrose congénitale des muscles oculomoteurs les<br />
plus <strong>fr</strong>équents. Ce syndrome est d’origine neurogène, mais<br />
les modifications musculaires induites par l’absence de nerf<br />
abducens (moteur oculaire externe) permettent de comprendre<br />
la survenue les manifestations cliniques [69] . Bien que<br />
généralement sporadique ou non héréditaire, une forme familiale<br />
du SSDT est possible. La transmission de cette dernière<br />
s’effectue selon un mode dominant autosomique. Ce syndrome<br />
est génétiquement hétérogène puisque deux gènes<br />
différents ont été localisés, l’un sur le bras long du chromosome<br />
8, l’autre sur le bras long du chromosome 2. Enfin,<br />
d’autres localisations ont été évoquées, en particulier au<br />
niveau des chromosomes 4 et 22.<br />
Symptomatologie<br />
L’existence du SSDT a été suspectée par Stilling dès 1887 puis<br />
par Türk en 1899 ; il n’a été décrit par Duane qu’en 1905.<br />
Dans la littérature anglo-saxonne, ce syndrome n’est connu<br />
que sous le nom de ce dernier auteur. Ce syndrome, présent<br />
dès la naissance, est généralement unilatéral, mais des cas<br />
bilatéraux ont été rapportés dans 10 à 57 % des observations.<br />
En revanche, le pourcentage de 96 % d’atteinte bilatérale<br />
retrouvé par Chung au sein d’une seule famille correspondrait<br />
à un caractère phénotypique propre à celle-ci [49] . Des formes<br />
unilatérales et bilatérales peuvent coexister au sein d’une<br />
même <strong>fr</strong>atrie lors de SSDT familiaux. Dans les formes unilatérales,<br />
l’œil gauche est plus volontiers atteint avec un ratio<br />
de 4/1.<br />
Dans sa forme classique, ou de type I, le SSDT est caractérisé<br />
par une absence, ou du moins un déficit très sévère,<br />
d’abduction d’un œil. La limitation des mouvements d’adduction<br />
de l’œil ipsilatéral est peu importante et doit être recherchée<br />
avec soin. Enfin, ces mouvements d’adduction<br />
entraînent une rétraction du globe qui présente un mouvement<br />
antéropostérieur, en raison de la brièveté des muscles<br />
horizontaux et de la cocontraction des muscles verticaux. Il<br />
s’y associe un rétrécissement de la fente palpébrale, secondaire<br />
à l’énophtalmie provoquée par la rétraction du globe<br />
(fig. 27-3). À l’inverse, un discret élargissement de la fente<br />
palpébrale peut être noté lors des mouvements d’abduction,<br />
sans doute du fait d’une protrusion du globe par mise en jeu<br />
des muscles obliques, ayant fonction d’abducteur, et s’insérant<br />
en avant de l’équateur. Il existe volontiers une discrète<br />
ésotropie en position primaire dans la forme de type I. En<br />
revanche, l’angle de déviation diminue lorsque les yeux se<br />
portent du côté opposé à l’œil présentant la limitation<br />
d’abduction. C’est la raison pour laquelle on observe volontiers<br />
chez ces patients une minime attitude vicieuse de la tête<br />
qui est tournée du côté pathologique. Un torticolis sévère est<br />
plus rare. Néanmoins, Chung a rapporté d’authentiques strabismes<br />
chez plus de 75 % des patients [49] . Des déviations verticales,<br />
en élévation plus qu’en abaissement, ont également<br />
été décrites lors des efforts d’adduction. Ces déviations verti-<br />
a b<br />
c<br />
Fig. 27-3 – Syndrome de Stilling-Duane-Türk de l’œil gauche.<br />
a. En position primaire, cet enfant est orthophorique. Mais, il existe un<br />
discret rétrécissement de la fente palpébrale gauche. b. Lorsque<br />
le regard est dirigé vers la gauche, l’abduction de l’œil gauche est<br />
impossible. Il ne dépasse pas la ligne médiane. c. Lorsque cet enfant<br />
regarde vers la droite, l’œil gauche peut se porter en adduction,<br />
mais il s’y associe un rétrécissement de la fente palpébrale gauche<br />
et une rétraction du globe oculaire gauche avec énophtalmie.<br />
(Collection de J.-L. Dufier.)<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 395
Livre.book Page 396 Jeudi, 26. février 2009 3:40 15<br />
cales sont secondaires à la brièveté des muscles droit interne<br />
et droit externe, avec un mécanisme de glissement de ces<br />
muscles horizontaux au-dessus ou en dessous du globe. Elles<br />
sont également provoquées par la cocontraction des muscles<br />
verticaux lors des mouvements d’adduction. Une anisométropie<br />
est volontiers observée lors du SSDT. Elle est responsable<br />
de la survenue d’amblyopies dont la <strong>fr</strong>équence est évaluée à<br />
48 % [49] . En l’absence d’anisométropie, l’acuité visuelle de<br />
chaque œil est normale, de même que la vision binoculaire.<br />
Le traitement chirurgical n’est indiqué que lorsque l’attitude<br />
vicieuse de la tête devient gênante ou en cas de déviation<br />
strabique en position primaire.<br />
L’association d’un SSDT avec des pathologies telles que le<br />
syndrome de Rubinstein-Taiby ou le syndrome de De Morsier<br />
est vraisemblablement fortuite [8] . La <strong>fr</strong>équence d’anomalies<br />
générales chez les patients porteurs de SSDT (surdité,<br />
anomalies squelettiques, paralysie de nerfs crâniens) est de<br />
l’ordre de 50 %. Il n’est pas exclu que ces anomalies soient<br />
secondaires à des troubles du développement liés à des mécanismes<br />
génétiques voisins de ceux responsables du SSDT.<br />
Fréquence et physiopathogénie<br />
Épidémiologie<br />
La <strong>fr</strong>équence du SSDT est mal connue. Une étude récente<br />
estime à 0,1 % sa prévalence dans la population générale. Il<br />
représente de 1 à 5 % de tous les cas de strabismes [14] .<br />
La majorité des SSDT correspond à des cas sporadiques ou<br />
à des formes non génétiques. Les formes familiales, transmises<br />
selon un mode dominant autosomique, représentent de 8<br />
à 10 % des observations de SSDT [87] . La <strong>fr</strong>équence des strabismes<br />
chez les apparentés de patients porteurs de SSDT est<br />
comprise entre 17,5 et 22 %. Enfin, celle des anomalies neurologiques<br />
ou squelettiques observée chez les apparentés du<br />
premier degré de patients porteurs de SSDT apparemment<br />
idiopathiques est de 46 %.<br />
Physiopathogénie<br />
L’existence d’une fibrose du muscle droit externe éventuellement<br />
associée à des anomalies d’insertion de ce muscle a été<br />
le premier mécanisme évoqué pour expliquer la survenue du<br />
SSDT. Toutefois, les études électromyographiques ont<br />
démontré, d’une part, le caractère fonctionnel du muscle droit<br />
latéral et, d’autre part, des cocontractions de ce muscle lors<br />
des mouvements d’adduction. De plus, une étude anatomopathologique<br />
réalisée chez deux patients a confirmé que le<br />
muscle droit latéral fibreux présente des zones saines au<br />
point d’arrivée de rameaux nerveux aberrants provenant de la<br />
branche inférieure du nerf moteur oculaire commun. Il est<br />
maintenant admis que le SSDT est d’origine neurogène, par<br />
agénésie ou, plus probablement, par anomalie de développement<br />
du noyau du nerf abducens (moteur oculaire externe).<br />
Le SSDT rejoint ainsi le cadre des fibroses congénitales des<br />
muscles extraoculaires secondaires à une anomalie de développement<br />
des noyaux des autres nerfs oculomoteurs, en particulier<br />
de celui du nerf moteur oculaire commun [70] . Cette<br />
absence du noyau du nerf abducens (moteur oculaire externe)<br />
a été confirmée au cours d’études post mortem [137] . Les études<br />
in vivo réalisées en imagerie par résonance magnétique ont<br />
abouti à des conclusions identiques [165] . L’agénésie du noyau<br />
du nerf abducens entraîne une absence de développement du<br />
tronc du nerf abducens et cette dernière s’avère responsable<br />
des anomalies musculaires constatées. En revanche, le nerf<br />
396 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
moteur oculaire commun peut envoyer des rameaux aberrants<br />
vers le muscle droit latéral, autorisant son développement<br />
très partiel.<br />
Génétique<br />
L’analyse du caryotype de patients porteurs d’un SSDT associé<br />
à d’autres malformations générales ou à des déficits neurologiques<br />
pouvant entrer dans le cadre de syndromes de type<br />
gènes contigus, a permis de mettre en évidence des délétions ou<br />
des duplications au niveau des chromosomes 4, 8 et 22 [165] .<br />
Une délétion de novo a été trouvée dans la région 4q27-31<br />
chez un patient porteur d’un ptosis bilatéral, d’un SSDT de<br />
type I et d’un retard mental modéré [44] . Cependant, cette localisation<br />
n’a pas pu être confirmée au sein d’autres familles<br />
porteuses d’un SSDT familial et aucune autre étude n’a à ce<br />
jour apporté de nouveaux arguments permettant de penser<br />
qu’un gène du SSDT soit localisé au niveau du chromosome<br />
4.<br />
Une trisomie 22 complète ou partielle avec un caryotype<br />
47,XX ou 46,XY/47,XY a été retrouvée chez plusieurs<br />
patients porteurs d’un SSDT. Ces caryotypes traduisent la<br />
présence d’un chromosome 22 surnuméraire dans le premier<br />
cas, ou d’un <strong>fr</strong>agment submétamérique de chromosome 22<br />
dans 12 à 99 % des cellules dans le second cas. Les patients<br />
porteurs d’un SSDT associé à une trisomie 22 manifestent<br />
très souvent d’autres anomalies ophtalmologiques ou générales,<br />
qu’il s’agisse d’un cat eye syndrome, d’une tétralogie de Fallot,<br />
d’une surdité, d’un retard mental, d’une dysmorphie<br />
faciale, d’une agénésie rénale ou d’autres anomalies urogénitales,<br />
ou d’anomalies cutanées péri-auriculaires. Or le syndrome<br />
de Di Georges et le cat eye syndrome caractérisé par la<br />
présence d’un colobome irien et d’une anomalie d’orientation<br />
des fentes palpébrales ainsi que par des anomalies périauriculaires,<br />
anales et éventuellement génito-urinaires, sont<br />
associés à une trisomie 22. Il existe donc un chevauchement<br />
des manifestations cliniques observées lors des différents<br />
syndromes dus à une trisomie 22 complète ou partielle. Un<br />
marqueur surnuméraire bi-satellite provenant plus spécifiquement<br />
des régions 22pter-q11 et une microdélétion en 22q11<br />
ont été retrouvés chez des patients porteurs de SSDT.<br />
Deux patients atteints d’un SSDT associé à syndrome<br />
branchio-oto-rénal et à un retard mental dans le cadre d’un<br />
syndrome de gènes contigus portaient une délétion de la<br />
région 8q12.2-q21.2 pour l’un d’eux et une insertion/délétion,<br />
aboutissant à la délétion de la région 8q13-q21.2, insérée en<br />
6q25 pour l’autre [37, 224] . À l’aide de techniques de PCR et de<br />
l’utilisation de contig de Yac, le chevauchement de ces accidents<br />
chromosomiques a été localisé en 8q13, définissant une<br />
première localisation du gène du SSDT. La localisation de ce<br />
gène, DURS1, a pu être réduite à une taille inférieure à 1 cM<br />
grâce à l’étude de deux enfants porteurs d’une translocation<br />
de type t(6;8)(q26;q13) ou d’une délétion du gène EYA1 du<br />
syndrome branchio-oto-rénal, localisé en 8q13.3 [38, 186] . De<br />
plus, il a pu être montré que la translocation t(6;8)(q26;q13)<br />
aboutit à l’interruption d’un gène carboxy-peptidase entre le<br />
premier et le second exon. Ce gène constitue donc un bon<br />
gène candidat [135, 176] .<br />
Un second gène du SSDT, dénommé DURS2, a été localisé<br />
au niveau de la bande 2q31 au sein d’une grande famille<br />
mexicaine chez laquelle le SSDT of<strong>fr</strong>ait une grande variabilité<br />
phénotypique [14, 49] . L’intervalle contenant ce gène a été réduit<br />
à une distance de 8,8 cM, entre les marqueurs D2S326 et<br />
D2S364, après étude d’une seconde famille américaine très
Livre.book Page 397 Jeudi, 26. février 2009 3:40 15<br />
informative. Plusieurs gènes candidats ont été retrouvés au<br />
sein de cet intervalle, dont les gènes HOXD1, D3 et D4. Ces<br />
derniers font partie de la famille des gènes HOX, contrôleurs<br />
du développement s’exprimant très précocement et régulant<br />
la morphogenèse et la division cellulaire chez l’animal. La<br />
suppression des gènes murins homologues des gènes<br />
humains HOXD1, D3 et D4, a confirmé leur importance dans<br />
le développement de la tête et des régions cérébrales postérieures<br />
[39] . Aucune mutation n’a pu actuellement être mise en<br />
évidence au niveau de l’un ou l’autre de ces gènes [14] .<br />
L’expression de ces gènes HOX est régulée par les rétinoïdes,<br />
en particulier le tout-trans et le 9-cis-acide rétinoïque. Il existe<br />
dans les régions 3’ et/ou 5’ des gènes hox murins, des systèmes<br />
de régulation de l’expression par les rétinoïdes. La suppression<br />
de ces séquences régulatrices aboutit à un tableau<br />
clinique identique à celui obtenu par la suppression du gène<br />
hox lui-même, avec une anomalie de développement des nerfs<br />
crâniens. Il n’est pas impossible que de telles régions existent<br />
également chez l’homme et qu’une anomalie à leur niveau<br />
s’avère responsable d’un SSDT [14] .<br />
Syndrome d’Okihiro<br />
Symptomatologie<br />
Encore dénommé Duane-Radial Ray syndrome, ce syndrome,<br />
décrit en 1975 par Temtamy, doit être étudié à part dans le<br />
cadre du SSDT. En effet, il s’agit d’une entité clinique particulière<br />
qui associe un SSDT à une surdité et à une dysplasie du<br />
radius [205] . D’autres anomalies musculaires et osseuses ont<br />
également été rapportées au cours de ce syndrome, portant<br />
principalement sur les membres supérieurs et leur racine.<br />
L’hypoplasie de l’éminence thénar semble être l’anomalie<br />
associée la plus constante au sein des différentes <strong>fr</strong>atries<br />
décrites dans la littérature [93] . Les autres malformations décrites<br />
sont une absence de pouce ou des anomalies des vertèbres<br />
cervicales.<br />
Génétique<br />
Le syndrome d’Okihiro est transmis selon un mode dominant<br />
autosomique. Au moins un gène responsable de ce syndrome<br />
a été identifié en 2002 [9] . Diverses mutations ont été retrouvées<br />
dans le gène SALL4, localisé sur le chromosome 20 en<br />
20q13.13-q13.2.<br />
Compte tenu du rôle des gènes de la famille Sall dans le<br />
développement des territoires cérébraux postérieurs chez<br />
l’animal, le gène SALL4 jouerait un rôle important dans la<br />
mise en place du noyau du nerf moteur oculaire externe [9] .<br />
SYNDROME DE BROWN<br />
Le syndrome de Brown, rapporté à la fibrose de la gaine du<br />
muscle oblique supérieur, peut être congénital ou apparaître<br />
secondairement, en particulier à la suite d’un traumatisme.<br />
Dans sa forme congénitale, ce syndrome entre dans le cadre<br />
des syndromes de restriction puisque les mouvements d’élévation<br />
ou d’abaissement actifs et passifs du globe en adduction<br />
sont limités. Lorsqu’il est congénital, le syndrome de<br />
Brown est le plus souvent sporadique, ce qui n’implique pas<br />
qu’il ne puisse pas être d’origine génétique. Ainsi, quelques<br />
rares observations font état de formes familiales de ce syndrome<br />
[98] .<br />
Symptomatologie<br />
Le syndrome de Brown peut être permanent ou simplement<br />
intermittent, y compris lorsqu’il est congénital. Son existence<br />
est évoquée devant une paralysie généralement unilatérale<br />
et d’intensité variable du muscle oblique supérieur et<br />
une impotence du muscle oblique inférieur homolatéral. En<br />
revanche, la motilité de l’œil n’est pas limitée dans les<br />
autres directions du regard. Ces anomalies oculomotrices<br />
permettent d’expliquer une éventuelle hypotropie de l’œil<br />
ipsilatéral ainsi qu’un syndrome « V ». L’attitude en torticolis<br />
est caractéristique, tête penchée sur l’épaule homolatérale.<br />
La fente palpébrale peut présenter un rétrécissement<br />
lors des mouvements d’adduction. D’autres anomalies de<br />
développement des nerfs crâniens ont été rapportées en<br />
association avec ce syndrome.<br />
Fréquence et physiopathogénie<br />
Épidémiologie<br />
La <strong>fr</strong>équence du syndrome de Brown est évaluée à 2 % des<br />
strabismes. L’atteinte oculomotrice est unilatérale dans 90 %<br />
des cas en moyenne, et il ne semble pas exister de côté préférentiel<br />
pour celle-ci (fig. 27-4). Dès les premières descriptions<br />
de ce syndrome, Brown avait différencié les formes congénitales<br />
et stables des formes tardives, dont la symptomatologie<br />
est variable. Cette classification ne préjuge pas du<br />
caractère génétique ou acquis de cette anomalie puisqu’un<br />
syndrome de Brown unilatéral apparu à l’âge de 12 ou 13 ans<br />
a été rapporté chez trois des quatre enfants d’une famille non<br />
consanguine [98] . Quoique d’apparition tardive, le syndrome<br />
de Brown observé au sein de cette <strong>fr</strong>atrie correspond vraisemblablement<br />
à une forme héréditaire.<br />
Fig. 27-4 – Jeune fille porteuse d’un syndrome de Brown du côté droit.<br />
Il existe une limitation des mouvements verticaux de l’œil droit lorsque<br />
ce dernier est en adduction avec, en particulier, une nette impotence<br />
de l’élévation. (Collection de J.-L. Dufier.)<br />
Physiopathogénie<br />
Initialement, Brown avait expliqué les formes congénitales<br />
de ce syndrome par la présence d’une fibrose musculaire ou<br />
d’une anomalie de longueur de la gaine du tendon du muscle<br />
oblique supérieur. Ses mécanismes physiopathogéniques<br />
ont été révisés : il serait la conséquence d’une anomalie de<br />
coulissement du tendon du muscle oblique supérieur au<br />
niveau de sa poulie, que la cause de ce blocage soit située au<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 397
Livre.book Page 398 Jeudi, 26. février 2009 3:40 15<br />
niveau de la trochlée ou du tendon lui-même. Néanmoins,<br />
aucune anomalie de la région trochléaire n’a pu être objectivée<br />
à ce jour chez les patients atteints d’un syndrome de<br />
Brown congénital. En revanche, à la différence du syndrome<br />
de Stilling-Duane-Türk et des syndromes de fibrose congénitale<br />
des muscles oculomoteurs (CFEOM), aucune anomalie<br />
du développement des nerfs oculomoteurs n’a été<br />
retrouvée au cours de ce syndrome et il n’est pas encore<br />
possible de trancher entre une origine neurogène, myogène<br />
ou tendineuse [98] .<br />
PTOSIS<br />
398 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
Génétique<br />
Historiquement, le syndrome de Brown était considéré<br />
comme non génétique. Néanmoins, la publication de <strong>fr</strong>atries<br />
au sein desquelles l’existence d’un syndrome de Brown sur<br />
une ou deux générations ou chez des jumeaux monozygotes<br />
conduit à mettre cette notion en doute. Du fait du petit nombre<br />
de familles dans lesquelles le syndrome de Brown est<br />
manifestement héréditaire, il n’est pas possible de préciser un<br />
mode de transmission spécifique et il est probable qu’une<br />
hétérogénéité génétique soit encore une fois retrouvée [98] .<br />
II – GÉNÉTIQUE DES PARALYSIES OCULOMOTRICES<br />
PARALYSIES OCULOMOTRICES<br />
NUCLÉAIRES<br />
Les ptosis peuvent être classés en fonction de leur présentation,<br />
isolée ou symptomatique, et de leur caractère héréditaire<br />
ou non. La <strong>fr</strong>équence des formes héréditaires est difficile<br />
à apprécier. Aberfeld considère qu’elle avoisine 75 %, mais<br />
que 96 % des ptosis seraient « génétiques » [3] . Les ptosis<br />
héréditaires ne s’observent pas uniquement dans le cadre des<br />
formes congénitales isolées. En effet, les ptosis acquis peuvent<br />
également relever d’affections ayant une origine génétique.<br />
C’est le cas du ptosis symptomatique de la myasthénie,<br />
mais aussi lors des cytopathies mitochondriales ou des affections<br />
musculaires dégénératives.<br />
Ptosis congénitaux isolés<br />
Les ptosis congénitaux isolés sont non évolutifs, bilatéraux ou<br />
unilatéraux. Pour sa part, McMullan estime que les formes<br />
dites unilatérales correspondent en fait à des formes très asymétriques<br />
de ptosis bilatéraux [131] .<br />
Symptomatologie<br />
Sans vouloir détailler la symptomatologie du ptosis congénital<br />
isolé, il convient d’en rappeler quelques éléments importants,<br />
en particulier l’effacement du pli palpébral supérieur et la<br />
contraction compensatrice du muscle <strong>fr</strong>ontal. Au repos, il faut<br />
rechercher une asymétrie ou une anomalie de taille des orbites<br />
pouvant orienter vers un blépharophimosis (cf. chapitre 7) et<br />
une éventuelle compensation du ptosis par une contraction du<br />
muscle <strong>fr</strong>ontal. Le risque amblyogène, qui influe sur les indications<br />
thérapeutiques, s’évalue en appréciant l’empiétement de<br />
la paupière supérieure sur l’axe pupillaire. Le tonus du muscle<br />
releveur de la paupière supérieure est bien mesuré par l’amplitude<br />
d’excursion palpébrale. Enfin, il faut insister sur l’importance<br />
de certains signes associés : présence ou absence d’un<br />
signe de Charles Bell, anomalie de la sensibilité cornéenne<br />
dont il faut tenir compte lors d’un éventuel traitement chirurgical,<br />
existence d’un strabisme ou d’une ophtalmoplégie et,<br />
surtout, d’une limitation de l’élévation. Ces associations orientent<br />
soit vers une paralysie congénitale du nerf moteur ocu-<br />
laire commun, soit vers l’un des différents syndromes de<br />
fibrose des muscles oculomoteurs, soit enfin vers une cytopathie<br />
mitochondriale. Enfin, les mouvements de succion ou de<br />
diduction mandibulaire objectivent le phénomène de Marcus<br />
Gunn, syncinésie trigémino-palpébrale, généralement unilatérale<br />
se caractérisant par une élévation plus ou moins marquée<br />
de la paupière et traduisant une innervation aberrante du muscle<br />
releveur de la paupière supérieure par un rameau du<br />
contingent moteur du nerf trijumeau (fig. 27-5).<br />
Physiopathogénie<br />
Les mécanismes physiopathogéniques responsables du ptosis<br />
congénital isolé ne sont pas tous connus. Des anomalies du<br />
muscle releveur de la paupière supérieure ont été observées<br />
depuis de nombreuses années ; mais elles ne correspondent<br />
pas à une dystrophie puisque ce ptosis n’est pas évolutif. Il<br />
existerait une anomalie de migration neuronale lors de<br />
l’embryogenèse ou une anomalie de développement du muscle,<br />
peu différent de ce qui est observé lors des syndromes de<br />
fibrose des muscles oculomoteurs [17] .<br />
Génétique<br />
Le ptosis congénital isolé peut être transmis selon deux<br />
modes : dominant autosomique à pénétrance incomplète ou<br />
dominant lié au chromosome X [131] . L’existence du caractère<br />
héréditaire de certains ptosis congénitaux isolés est connue<br />
depuis le début du XX e siècle. Briggs avait déjà évoqué une<br />
transmission dominante autosomique à pénétrance incomplète<br />
ou à expressivité variable en 1919 après analyse d’une<br />
famille américaine comportant des membres atteints de ptosis<br />
congénital unilatéral isolé sur six générations. Cohen a calculé<br />
la pénétrance au sein d’une grande famille comportant<br />
des patients porteurs d’un ptosis uni- ou bilatéral et a estimé<br />
cette <strong>fr</strong>équence à 60 % [51] . Engle a entrepris d’étudier les événements<br />
de recombinaison au sein de cette même <strong>fr</strong>atrie. Il a<br />
ainsi déterminé l’existence, au niveau du bras court du chromosome<br />
1 en 1p32-p34.1, d’une région de 2,8 cM ségrégeant<br />
avec le ptosis. Cette région est bordée par les marqueurs<br />
D1S447/2733 et D1S1616 et est associée au gène PTOS1.<br />
Aucun gène candidat n’a été retrouvé dans cette région. Le<br />
syndrome muscle-œil-système nerveux est également localisé<br />
dans cette même région 1p32-p34.1 [54] . Ce syndrome est cliniquement<br />
peu différent du syndrome de Walker-Warburg
Livre.book Page 399 Jeudi, 26. février 2009 3:40 15<br />
a b<br />
Fig. 27-5 – Ptosis congénital gauche associé à une syncinésie trigémino-palpébrale réalisant le phénomène de Marcus Gunn. a. Au repos, le ptosis gauche<br />
est très marqué, la paupière supérieure atteint l’axe optique. b. Lors des mouvements de succion, la paupière supérieure gauche se relève et les fentes<br />
palpébrales sont symétriques. (Collection de J.-L. Dufier.)<br />
puisqu’il est défini par l’existence d’un retard mental très<br />
sévère, d’une hydrocéphalie, d’anomalies oculaires à type de<br />
myopie forte, de glaucome congénital, de pâleur papillaire et<br />
d’anomalies rétiniennes et d’une dystrophie musculaire.<br />
Cependant, aucune atteinte du muscle releveur de la paupière<br />
supérieure n’est rapportée dans le cadre de cette dystrophie<br />
musculaire, ni aucun ptosis. Ce syndrome est lié à la présence<br />
de mutations au sein du gène de la protéine O-mannose-β-<br />
1,2-N-acétylglucosaminyltransférase. Cette dernière intervient<br />
dans la seconde étape de la synthèse du O-manosylglycane,<br />
jouant un rôle important dans la migration neuronale.<br />
L’hétérogénéité génétique du ptosis congénital isolé est<br />
suggérée par la connaissance d’un locus différent de la localisation<br />
1p32-p34.1. McMullan a décrit l’existence d’une translocation<br />
équilibrée t(1;8)(p34.3;q21.12) apparue de novo chez<br />
un patient porteur d’un ptosis [132] . La localisation précise des<br />
points de cassure sur les chromosomes 1 et 8 a été obtenue<br />
en utilisant les techniques d’hybridation in situ par fluorescence,<br />
de PCR et d’amplification de sites marqués. Le point<br />
de cassure sur le chromosome 1 est situé à distance du locus<br />
1p32-p34.1 tel qu’il a été défini par Engle. De plus, cette cassure<br />
n’affecte aucune séquence codante sur ce chromosome.<br />
En revanche, le point de cassure localisé sur le chromosome<br />
8, en 8q21.12, altère le gène humain ZFH-4, homologue<br />
du gène murin zfh-4. Celui-ci code une protéine possédant un<br />
homéodomaine à doigt de zinc qui est un facteur de transcription<br />
exprimé dans le muscle et le système nerveux [132] .<br />
McMullan évoque la possibilité qu’un second gène responsable<br />
de ptosis congénital isolé soit situé à ce locus et propose<br />
le gène ZFH-4 comme gène candidat. Toutefois, aucune<br />
mutation n’a été retrouvée dans ce gène chez aucun patient<br />
porteur de ptosis congénitaux [132] .<br />
Le ptosis congénital isolé peut être également transmis selon<br />
un mode dominant lié au chromosome X [131] . Une liaison<br />
génétique a pu être mise en évidence avec le chromosome X<br />
au sein d’une <strong>fr</strong>atrie de 94 membres répartis sur cinq générations<br />
dont 21 patients (6 hommes et 15 femmes) étaient porteurs<br />
d’un ptosis bilatéral. Le caractère dominant de la<br />
transmission liée au chromosome X est confirmé par l’absence<br />
de transmission père-fils et par l’atteinte systématique de toutes<br />
les filles d’hommes atteints. Ce gène PTOS2 est localisé<br />
dans la région Xq24-q27.1 [132] . Il n’existe actuellement aucun<br />
gène candidat dans cette région.<br />
Ptosis associés<br />
Les ptosis peuvent être associés à des anomalies neurologiques<br />
ou orbitaires secondaires à un trouble du développement,<br />
comme dans le blépharophimosis — qui associe des<br />
anomalies de l’orbite et des paupières — ou dans le syndrome<br />
de Saethre-Chotzen. Ce syndrome, secondaire à des<br />
mutations dans le gène TWIST, comporte une craniosténose<br />
de type plagiocéphalie, un blépharophimosis et des syndactylies.<br />
Le ptosis peut en être la manifestation essentielle. Il faut<br />
également citer les ptosis symptomatiques des syndromes de<br />
fibrose congénitale des muscles oculomoteurs, d’une paralysie<br />
congénitale du nerf moteur oculaire commun ou du syndrome<br />
myasthénique. Ces ptosis associés peuvent également<br />
constituer le premier signe d’une pathologie générale, héréditaire<br />
ou non. Tel est le cas des ptosis d’origine myasthénique,<br />
des ptosis révélateurs d’une dysthyroïdie, d’une myopathie<br />
mitochondriale, qu’il s’agisse d’une ophtalmoplégie externe<br />
progressive ou d’un syndrome de Kearns-Sayre. Ces affections<br />
sont l’objet du chapitre 28.<br />
PARALYSIE CONGÉNITALE<br />
DU NERF TROCHLÉAIRE (PATHÉTIQUE)<br />
Les paralysies congénitales du nerf trochléaire (IV) ne sont<br />
pas exceptionnelles. Elles constituent les plus <strong>fr</strong>équentes des<br />
paralysies des nerfs oculomoteurs et représentent plus de la<br />
moitié des paralysies du IV chez l’enfant. Il a été décrit des<br />
paralysies du IV d’origine héréditaire.<br />
Symptomatologie<br />
La symptomatologie de la paralysie congénitale du IV est<br />
relativement standardisée. Cette paralysie n’entraîne aucune<br />
diplopie tant qu’elle est bien compensée. Néanmoins, elle<br />
s’accompagne d’une attitude en torticolis caractéristique, le<br />
menton abaissé et la tête penchée sur l’épaule opposée au<br />
muscle paralysé. Cette position de la tête permet de compenser<br />
la déviation verticale du globe. L’examen retrouve<br />
l’hypoaction du muscle oblique supérieur paralysé, l’hyperaction<br />
du muscle oblique inférieur homolatéral, l’hypoaction du<br />
muscle droit supérieur controlatéral et la possible hyperaction<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 399
Livre.book Page 400 Jeudi, 26. février 2009 3:40 15<br />
du muscle droit inférieur controlatéral (fig. 27-6). L’examen<br />
au coordimètre objective la persistance d’une vision binoculaire<br />
dans une grande partie du champ visuel. Cette particularité<br />
est liée à l’augmentation significative de la fusion<br />
verticale qui peut atteindre 30 dioptries prismatiques. Néanmoins,<br />
une neutralisation intermittente peut apparaître dans<br />
les directions du regard où existe une incomitance. Cette<br />
paralysie du IV est longtemps compensée et souvent méconnue.<br />
L’apparition d’une décompensation, qui peut survenir<br />
tardivement, parfois à l’âge adulte, se traduit par la survenue<br />
d’une diplopie souvent interprétée comme une vision trouble.<br />
Mais, il n’existe pas de cyclotorsion au test de Lancaster.<br />
Fig. 27-6 – Paralysie congénitale du nerf trochléaire droit se traduisant<br />
par une hypoaction du muscle oblique supérieur droit et une hyperaction<br />
du muscle oblique inférieur droit. (Collection de J.-L. Dufier.)<br />
Génétique<br />
Les paralysies du IV représentent de 29 à 67 % des paralysies<br />
congénitales de l’enfant selon les séries [29] . La majorité de ces<br />
paralysies sont sporadiques. Néanmoins, huit familles ont été<br />
rapportées au sein desquelles existent des paralysies familiales<br />
du IV, ce qui évoque une possible transmission génétique<br />
[29, 92] . Dans quatre de ces huit familles, la paralysie unilatérale<br />
du IV n’est retrouvée qu’au niveau d’une seule<br />
génération, affectant alors deux enfants, garçons ou filles.<br />
Dans trois autres familles, la transmission se fait d’une génération<br />
à l’autre, deux fois entre une mère et sa fille et une fois<br />
entre un père et sa fille. Chez ces six patients, l’atteinte est<br />
également unilatérale. Enfin, Botelho a rapporté une famille<br />
dans laquelle une paralysie du IV est retrouvée chez cinq des<br />
dix patients de la <strong>fr</strong>atrie sur trois générations. Quatre hommes<br />
sont atteints d’une forme bilatérale alors que l’on observe une<br />
forme unilatérale chez la seule femme atteinte. Un mode de<br />
transmission dominant autosomique est suggéré par un sexratio<br />
égal à 1, l’absence de consanguinité et des transmissions<br />
père-fils sur plusieurs générations. Il n’existe à ce jour aucune<br />
localisation pour le gène de cette paralysie ni de gène candidat.<br />
Récemment, une mutation a été retrouvée au niveau de<br />
l’exon 1 du gène ARIX chez quatre membres d’une même<br />
famille présentant une paralysie congénitale du IV [100] .<br />
PARALYSIE CONGÉNITALE DU NERF MOTEUR<br />
OCULAIRE COMMUN ET DU NERF ABDUCENS<br />
(MOTEUR OCULAIRE EXTERNE)<br />
Aucune observation ne permet d’affirmer l’existence d’une<br />
paralysie congénitale du nerf moteur oculaire commun (III) ou<br />
400 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
du nerf abducens (nerf moteur oculaire externe ou VI) génétiquement<br />
déterminée. Cependant, des ptosis isolés retrouvés<br />
dès la naissance ont été rapportés comme pouvant correspondre<br />
à des paralysies du III limitées au muscle releveur de la<br />
paupière supérieure. En l’absence d’autres arguments en<br />
faveur de cette origine, il semble qu’il faille classer ces anomalies<br />
du jeu palpébral parmi les ptosis congénitaux isolés.<br />
SYNDROME DE MŒBIUS<br />
Le syndrome de Mœbius est défini par une diplégie faciale<br />
associée à un trouble de l’horizontalité du regard avec paralysie<br />
bilatérale de l’abduction. Des atteintes d’autres nerfs crâniens<br />
et des malformations musculo-squelettiques peuvent<br />
s’observer. Considéré généralement comme sporadique, le<br />
syndrome de Mœbius peut être familial et plusieurs gènes<br />
responsables de ce syndrome ont été localisés.<br />
Symptomatologie<br />
Le syndrome de Mœbius associe une paralysie congénitale et<br />
non évolutive de différents nerfs crâniens. McDermot considère<br />
que le terme de syndrome de Mœbius devrait être<br />
réservé à l’association d’une atteinte des sixième et septième<br />
paires crâniennes et d’anomalies faciales ou squelettiques [121] .<br />
La diplégie faciale est constante et souvent symétrique<br />
(fig. 27-7). Cependant, Kremer a décrit une famille au sein de<br />
laquelle la paralysie faciale est asymétrique chez presque tous<br />
les patients porteurs du syndrome de Mœbius et le déficit<br />
moteur d’intensité variable en fonction des branches du nerf<br />
facial [115] . Malheureusement, les anomalies oculomotrices<br />
retrouvées au sein de cette <strong>fr</strong>atrie ne sont pas clairement précisées,<br />
et le diagnostic de paralysie faciale congénitale pourrait<br />
également être évoqué. Cette diplégie faciale est<br />
responsable de troubles de la succion, d’un défaut d’occlusion<br />
palpébrale plus ou moins sévère, d’une kératite ponctuée<br />
superficielle, d’un épiphora et parfois d’un syndrome des<br />
« larmes de crocodile » par anomalie de réinnervation des<br />
glandes lacrymales. La paralysie complète et bilatérale de<br />
l’abduction est due à l’atteinte des nerfs abducens (oculomo-<br />
Fig. 27-7 – Jeune garçon porteur d’un syndrome de Mœbius avec une<br />
diplégie faciale, se traduisant par un visage atone, une disparition des<br />
sillons naso-géniens et des rides du <strong>fr</strong>ont et un ptosis bilatéral. Les yeux<br />
sont en ésotropie du fait d’une paralysie bilatérale des nerfs moteurs<br />
oculaires communs. (Collection de J.-L. Dufier.)
Livre.book Page 401 Jeudi, 26. février 2009 3:40 15<br />
teurs externes) ou de leurs noyaux, avec préservation partielle<br />
de l’adduction de chaque œil. Un déficit plus ou moins marqué<br />
de l’horizontalité du regard, ne laissant persister que des<br />
mouvements incomplets de convergence des deux yeux, peut<br />
s’associer à la paralysie des nerfs abducens. En revanche, la<br />
verticalité du regard est généralement préservée, et la persistance<br />
d’un signe de Charles Bell limite la kératite à la partie<br />
inférieure des deux cornées. La présence d’une ésotropie,<br />
d’une amblyopie unilatérale et d’une altération de la vision<br />
binoculaire n’est pas exceptionnelle. Certains auteurs, tels<br />
que Kremer, considèrent que les anomalies oculomotrices ne<br />
sont pas indispensables pour parler de syndrome de Mœbius,<br />
ce qui n’est pas sans poser des problèmes nosologiques vis-àvis<br />
de la paralysie faciale congénitale [115] .<br />
D’autres nerfs crâniens peuvent être non fonctionnels,<br />
principalement les nerfs grand hypoglosse, trochléaires<br />
(pathétiques), trijumeaux, auditifs et glossopharyngiens. Des<br />
malformations associées de la région faciale (microglossie,<br />
micrognatisme, anomalies de la mâchoire ou d’implantation<br />
des oreilles, télécanthus ou épicanthus) ou des membres<br />
(syndactilie, brachydactilie, déformation des phalanges, anomalies<br />
costales, contractures musculaires) sont également<br />
décrites lors de ce syndrome [115] . Un retard mental est noté<br />
chez 10 % environ des patients [115] . Une atrophie diffuse du<br />
tronc cérébral ou localisée aux nerfs crâniens paralysés ainsi<br />
que des calcifications dans la portion dorsale de la protubérance<br />
peuvent être retrouvées en IRM [73] .<br />
L’association d’un syndrome de Mœbius à un hypogonadisme<br />
par hyposécrétion d’hormone gonadotrophique est<br />
vraisemblablement fortuite puisqu’une hyposécrétion d’hormone<br />
gonadotrophique par défaut de sécrétion de GnRH<br />
d’origine hypothalamique a été décrite lors de multiples<br />
lésions du système nerveux central [30] . Néanmoins, un gène<br />
dénommé WDR10, codant une protéine produite au niveau<br />
des testicules et dans la région de la tige pituitaire et pouvant<br />
être impliquée dans l’hypogonadisme, a été retrouvé en 3q21,<br />
l’une des localisations primaires du syndrome de Mœbius [84] .<br />
L’association d’une anomalie de Poland (aplasie unilatérale<br />
d’un muscle grand pectoral) ou d’un syndrome de Poland<br />
(aplasie unilatérale d’un muscle grand pectoral et malformations<br />
ipsilatérales de la main) à un syndrome de Mœbius réalise<br />
le syndrome de Poland-Mœbius (fig. 27-8 et 27-9) [112] . La<br />
réalité de ce syndrome reste controversée, quoiqu’une même<br />
localisation génique au niveau du chromosome 1 ait été proposée<br />
par Nishikawa pour ces deux syndromes [152] . Le syndrome<br />
de Carey-Fineman-Ziter serait une variante du<br />
syndrome de Poland-Mœbius, associant à un syndrome de<br />
Mœbius une hypoplasie bilatérale du muscle grand pectoral,<br />
une dysmorphie et une parésie des extrémités [18] .<br />
La prise en charge du syndrome de Mœbius repose tout<br />
d’abord sur la prévention des complications cornéennes dues<br />
à la diplégie faciale. Une intervention chirurgicale portant sur<br />
les muscles horizontaux peut corriger un éventuel strabisme<br />
associé mais rarement réduire les conséquences de la paralysie<br />
bilatérale de l’abduction. La prise en charge maxillo-faciale<br />
nécessite de corriger initialement les malformations de la<br />
mâchoire avant d’envisager d’effectuer des transpositions<br />
musculaires (muscle temporal) ou nerveuses (nerf grand<br />
hypoglosse…).<br />
Physiopathogénie<br />
La physiopathogénie du syndrome de Mœbius reste mal<br />
connue et n’est sans doute pas univoque. Certains aspects<br />
anatomopathologiques permettent d’évoquer une origine<br />
génétique ou vasculaire. Ainsi, Verzijl définit deux catégories<br />
de syndrome de Mœbius [223] . La première catégorie correspond<br />
histologiquement à une agénésie ou hypoplasie des<br />
noyaux des nerfs crâniens en relation avec un trouble de la<br />
Fig. 27-8 – Jeune garçon porteur d’un syndrome de Poland-Mœbius.<br />
a. Il existe une ésotropie ainsi qu’une paralysie faciale bilatérale mais<br />
asymétrique, plus marquée à droite. b. Il est retrouvé chez ce même<br />
patient une anomalie de la main avec une aplasie et malformation<br />
des doigts. (Collection de J.-L. Dufier.)<br />
Fig. 27-9 – Dans le cadre du syndrome de Poland-Mœbius, les<br />
anomalies de la main peuvent être beaucoup plus sévères, comme chez<br />
cet enfant ayant une une aplasie presque complète de tous les doigts.<br />
(Collection de J.-L. Dufier.)<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 401<br />
a<br />
b
Livre.book Page 402 Jeudi, 26. février 2009 3:40 15<br />
migration des cellules de la crête neurale d’origine génétique,<br />
encore que le rôle de facteurs épigénétiques ne puisse être<br />
exclu. Dans la seconde catégorie, les études anatomopathologiques<br />
retrouvent des lésions considérées comme ischémiques,<br />
l’ischémie pouvant être d’origine génétique ou<br />
épigénétique. Le développement du rhombencéphale, plus<br />
particulièrement du tronc cérébral, est sous la dépendance de<br />
la migration de cellules dérivées des crêtes neurales, d’une<br />
part, et provient des rhombomères, d’autre part. Ceux-ci sont<br />
particulièrement impliqués dans la mise en place des noyaux<br />
des nerfs oculomoteurs ainsi que du nerf facial. Un accident<br />
vasculaire précoce, entre la quatrième et la huitième semaine<br />
de vie embryonnaire, par régression ou obstruction du système<br />
vasculaire embryonnaire, peut être responsable d’une<br />
anomalie de développement soit des nerfs crâniens, soit du<br />
membre supérieur, soit encore du muscle pectoral dans le<br />
syndrome de Poland. L’importance respective des facteurs<br />
génétique et épigénétique reste imprécise. L’inadéquation de<br />
la vascularisation embryonnaire pourrait être de nature génétique.<br />
Lipson a retrouvé huit incidents lors de la grossesse<br />
chez quinze patients porteurs d’un syndrome de Mœbius :<br />
intoxication alcoolique, menace d’avortement prématuré,<br />
choc électrique ou rupture prématurée des membranes [118] .<br />
Génétique<br />
Le syndrome de Mœbius est habituellement sporadique, mais<br />
il existe néanmoins d’authentiques formes familiales, plus <strong>fr</strong>équentes<br />
dans les formes associées à une surdité, une ophtalmoplégie<br />
complète ou des troubles neurologiques à type de<br />
contracture [115, 121, 223] . Le syndrome de Mœbius peut être<br />
transmis selon trois modes différents : dominant autosomique,<br />
récessif autosomique ou récessif lié au chromosome X.<br />
Dans la forme dominante autosomique, la pénétrance est<br />
comprise entre 60 % et 95 % [115, 223] . Au moins trois gènes<br />
différents, MBS1, MBS2 et MBS3 ont été rattachés à ce syndrome.<br />
Deux d’entre eux, MSB2 et MSB3, l’ont été à des formes<br />
atypiques de syndromes de Mœbius, les anomalies<br />
oculomotrices étant minimes ou mal définies, ce qui pose un<br />
problème nosologique avec la paralysie faciale congénitale.<br />
Enfin, il n’est pas impossible qu’un quatrième gène puisse<br />
exister [152] .<br />
L’existence d’une translocation entre les chromosomes 1 et<br />
13 t(1;13)(p34;q13) chez tous les patients porteurs d’un syndrome<br />
de Mœbius au sein d’une même famille et la présence<br />
d’une délétion de novo localisée au niveau du bras long du<br />
chromosome 13, del(13)(q12.2), chez une fille atteinte d’un<br />
syndrome de Mœbius avec paralysie faciale unilatérale,<br />
paralysie bilatérale des nerfs moteurs oculaires externes et<br />
paralysie dans le territoire du nerf grand hypoglosse, ont<br />
permis de localiser un premier gène MBS1 dans la région<br />
13q12.2-q13 [199, 235] . Une translocation multiple t(7;8;11;13)<br />
chez un autre patient a confirmé cette localisation [28] .<br />
Cependant, la présence d’un gène sur le chromosome 1 en<br />
1p22 ne peut être éliminée devant des translocations<br />
(t(1;13)(p34;q13), t(1;11)(p22;p13) et t(1;2)(p22.2;q21.1))<br />
retrouvées chez des patients porteurs de syndromes de<br />
Mœbius ou Poland-Mœbius familiaux [135, 152] .<br />
Une analyse de liaison a été réalisée au sein d’une grande<br />
famille hollandaise dont trente et un membres sont porteurs<br />
d’un syndrome de Mœbius atypique posant un problème<br />
nosologique avec une paralysie faciale congénitale. Les anomalies<br />
ophtalmologiques observées au sein de cette <strong>fr</strong>atrie<br />
402 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
sont peu spécifiques. Cette étude de liaison a permis de localiser<br />
le gène MBS2 rattaché à ce syndrome de Mœbius atypique<br />
sur le bras long du chromosome 3 [115] . Par analyse du lod<br />
score et d’événements de recombinaison chez différents<br />
patients, l’intervalle dans lequel ce gène est localisé a été<br />
réduit à une distance de 10 cM dans la région 3q21-22. La<br />
stratégie des gènes candidats a été utilisée pour identifier le<br />
gène MBS2, en testant au moins vingt-cinq gènes dont celui<br />
du syndrome blepharophimosis-ptosis-epicanthus inversus et celui<br />
de la neuropathie de Charcot-Marie-Tooth de type IIB, localisés<br />
dans cette même région, mais aucune mutation dans ces<br />
gènes n’a pu être retrouvée. Il en est de même en ce qui<br />
concerne le gène SOX14, homologue humain d’un gène de la<br />
souris et du poulet impliqué dans le développement cérébral<br />
et de la moelle, localisé en 3q23 [228] . De même, aucune mutation<br />
n’a été retrouvée dans le gène GATA2, de la famille de<br />
facteurs de transcription GATA, ni dans le gène PGT codant<br />
un transporteur des prostaglandines, tous deux localisés dans<br />
cette région.<br />
Un quatrième gène a été localisé sur le bras long du chromosome<br />
10 dans la région 21.3-22.1 au sein d’une grande<br />
famille, rapportée par Verzijl, dont certains membres sont<br />
porteurs d’un syndrome de Mœbius atypique. Ce dernier<br />
pose les mêmes problèmes nosologiques avec la paralysie<br />
faciale congénitale que ceux évoqués pour le gène MSB2 [223] .<br />
La pénétrance du syndrome de Mœbius lié à MBS3 est calculée<br />
à 60 %. Le gène Early Growth Response 2, situé dans cet<br />
intervalle, pourrait être un bon gène candidat du syndrome<br />
de Mœbius. En effet, la suppression de l’équivalent murin de<br />
ce gène chez la souris, Krox-20, aboutit à la disparition des<br />
rhombomères 3 et 5 au cours du développement. Mais,<br />
aucune mutation n’a pu y être retrouvée chez les patients<br />
atteints de syndrome de Mœbius.<br />
SCLÉROSE EN PLAQUES<br />
La sclérose en plaques (SEP) peut être responsable de manifestations<br />
neuro-ophtalmologiques diverses, au premier rang<br />
desquelles se placent la neuropathie optique rétrobulbaire et<br />
les paralysies oculomotrices d’origine nucléaire ou supranucléaire<br />
(ophtalmoplégie internucléaire). L’existence de facteurs<br />
héréditaires ou de formes familiales de SEP est restée longtemps<br />
controversée. Différents arguments ont été avancés en<br />
faveur de l’une ou l’autre de ces hypothèses. Le risque de<br />
développer une SEP est plus élevé chez les apparentés de<br />
patients atteints que dans la population générale et certaines<br />
séries font état de cas familiaux. De plus, différents haplotypes<br />
ou allèles du système majeur d’histocompatibilité de<br />
classe II seraient retrouvés avec une plus grande <strong>fr</strong>équence<br />
chez des patients porteurs de SEP, du moins dans la population<br />
européenne. Il s’agit de l’haplotype HLA DRB1 (et des<br />
haplotypes associés HLA DRB1*1501, HLA DQB1*0602<br />
[DR2] et HLA DRB5*0101). Si ces données constituent des<br />
arguments en faveur du rôle de facteurs génétiques, ils ne permettent<br />
pas d’exclure la participation de facteurs environnementaux.<br />
L’existence d’une répartition géographique<br />
inhomogène de la SEP plaiderait en faveur de causes non<br />
génétiques (virales, alimentaires…). Une étude canadienne a<br />
récemment démontré que le risque de développer une SEP<br />
n’est pas plus élevé pour les personnes vivant avec un patient<br />
porteur de SEP que dans la population générale et que le risque<br />
pour leurs demi-<strong>fr</strong>ères et demi-sœurs est environ moitié<br />
moindre que celui des <strong>fr</strong>ères et sœurs. Ces résultats consti-
Livre.book Page 403 Jeudi, 26. février 2009 3:40 15<br />
tuent des arguments forts en faveur de facteurs polygéniques.<br />
Il est actuellement admis que de nombreux facteurs génétiquement<br />
déterminés, comme les haplotypes du système<br />
majeur d’histocompatibilité de type II ou la Myelin Basic Protein<br />
(MBP), interagissent ensemble, sans qu’aucun d’entre eux<br />
ne soit prépondérant [19, 85] .<br />
Le rôle du système majeur d’histocompatibilité de classe II<br />
est diversement interprété. Il est admis que l’haplotype HLA<br />
DRB1 joue un rôle certain pour provoquer la survenue d’une<br />
SEP dans la population européenne ; toutefois, il n’est pas<br />
encore clairement établi si cet haplotype agit par lui-même ou<br />
si d’autres facteurs ou gènes voisins sont impliqués. Des facteurs<br />
associés en déséquilibre de liaison important avec cet<br />
haplotype HLA DRB1 (tels que l’haplotype DQB1*0602),<br />
pourraient être responsables de la survenue d’une SEP. Barcellos<br />
a retrouvé une <strong>fr</strong>équence très élevée (64 %) de l’haplotype<br />
DR2 dans les cas familiaux de SEP. Il semble que le risque de<br />
développer une SEP soit plus important et que celle-ci soit<br />
plus sévère chez les patients homozygotes pour l’haplotype<br />
DR2 [19] . Ce dernier serait également associé à des formes<br />
débutant par des névrites optiques et/ou des atteintes spinales.<br />
D’autres haplotypes pourraient également être en cause<br />
dans les familles non liées à DR2 : l’haplotype HLA DR13<br />
(DRB*1302) serait associé à des SEP peu évolutives.<br />
Le rôle des lymphocytes T est bien établi, puisque ces cellules<br />
répondent à un antigène dérivé de la myéline, la MBP. Il<br />
a été observé une modification des lymphocytes T avant le<br />
déclenchement d’une SEP et une activation des lymphocytes<br />
T dirigés contre la MBP chez les malades comparés à des<br />
témoins sains [88] . Enfin, leur rôle a été clairement démontré<br />
lors de l’encéphalite expérimentale auto-immune chez l’animal.<br />
Le gène du récepteur des lymphocytes T constitue donc<br />
un candidat comme facteur de risque génétique.<br />
Des anomalies ont été recherchées dans le gène de la protéine<br />
CD45 localisé sur le chromosome 1 en 1q31-q32, qui<br />
apparaissait comme un excellent gène candidat des facteurs<br />
génétiques de la SEP. En effet, la protéine CD45, exprimée<br />
dans les cellules lymphocytaires et les cellules progénitrices<br />
sanguines, est impliquée dans les réactions immunologiques.<br />
De plus, des lymphocytes activés CD45 + sont retrouvés dans<br />
le liquide céphalorachidien lors des poussées de la maladie et<br />
leur taux constitue un marqueur de l’activité de la SEP. Une<br />
mutation a été retrouvée dans le gène de CD45 chez quatre<br />
patients [139] . Les études ultérieures n’ont cependant pas permis<br />
de confirmer l’implication de cette mutation dans de<br />
grandes séries de patients.<br />
Le gène de la MBP constitue également un candidat<br />
comme facteur génétique de la SEP. Cette protéine existe<br />
sous plusieurs allèles, déterminés par le nombre variable de<br />
répétitions en tandem (TGGA) n présent. Le nombre de répétitions<br />
pourrait être important dans la détermination du risque<br />
de développer une SEP. Mais son action serait modulée par<br />
d’autres facteurs tels que le système d’histocompatibilité de<br />
type II [85] .<br />
Enfin, le rôle de l’apolipoprotéine E (APOE), dont le gène<br />
est situé sur le chromosome 19p13.2, a été évoqué comme<br />
facteur de risque génétiquement déterminé. Les patients porteurs<br />
de l’allèle APOE4 présenteraient une SEP d’évolution<br />
plus sévère que ceux porteurs de l’allèle APOE2. Ces différences<br />
seraient la conséquence des capacités des allèles de<br />
l’APOE à assurer un fonctionnement neuronal correct et à<br />
réparer les anomalies neuronales [43] .<br />
Des liaisons génétiques ont été retrouvées avec un grand<br />
nombre de loci, mais sans qu’aucune confirmation n’ait pu<br />
être apportée lors de l’étude d’autres séries. De plus, en<br />
dehors des gènes du système majeur d’histocompatibilité,<br />
plusieurs de ces loci ne sont pas associés à des gènes connus.<br />
PORPHYRIE AIGUË INTERMITTENTE<br />
La porphyrie aiguë intermittente peut être responsable d’accidents<br />
aigus caractérisés par la survenue de douleurs abdominales<br />
et de troubles neurologiques ou rénaux. Les accidents<br />
neurologiques réalisent principalement des neuropathies<br />
motrices, mais des accidents globaux ou focaux peuvent être<br />
observés. Des complications neuro-ophtalmologiques sévères<br />
à type de paralysie oculomotrice tronculaire ou nucléaire,<br />
mais aussi de cécité corticale, par infarcissement cérébral lors<br />
des épisodes aigus, ou de neuropathie par vasospasme ont été<br />
rapportées. Ces épisodes aigus rares chez l’enfant sont favorisés<br />
par des prises médicamenteuses ou des modifications hormonales.<br />
Des règles hygiéno-diététiques permettent d’éviter<br />
ces crises aiguës et d’améliorer le pronostic vital.<br />
Cette affection, transmise selon un mode dominant autosomique,<br />
est due à un déficit en porphobilinogène désaminase,<br />
enzyme codée par un gène localisé en 11q23.3. Cette<br />
enzyme dont le taux est réduit d’environ 50 % intervient<br />
dans la formation de l’uroporphyrinogène de type I. Elle<br />
s’exprime dans les cellules hépatiques, les hématies, les fibroblastes<br />
et les cellules amniotiques. La présence de cette<br />
enzyme dans le liquide amniotique permet un diagnostic<br />
anténatal de la porphyrie aiguë intermittente.<br />
Les autres types de porphyries sont également responsables<br />
d’atteintes ophtalmologiques cornéennes, sclérales, palpébrales<br />
ou conjonctivales.<br />
PARALYSIES OCULOMOTRICES<br />
SUPRANUCLÉAIRES<br />
SYNDROME DE LEIGH<br />
Le génome mitochondrial ne code que treize protéines de la<br />
chaîne respiratoire. Les autres protéines impliquées dans la<br />
respiration cellulaire sont codées par le génome nucléaire.<br />
C’est la raison pour laquelle le syndrome de Leigh, dû à un<br />
déficit énergétique cellulaire, peut être transmis soit selon le<br />
mode récessif autosomique ou selon le mode lié au chromosome<br />
X, traduisant une atteinte du génome nucléaire, soit<br />
selon un mode maternel caractéristique des atteintes de<br />
l’ADN mitochondrial (cf. chapitre 28) [60] .<br />
Symptomatologie<br />
Ce syndrome, d’abord dénommé « encéphalomyopathie<br />
nécrosante subaiguë », a été décrit en 1951 par Denis Leigh<br />
qui avait constaté la présence de foyers de nécrose et de prolifération<br />
capillaire cérébrale chez un garçon décédé à l’âge de<br />
8 mois. Les manifestations cliniques débutent très tôt au<br />
cours de la vie, souvent dans les premières semaines, et aboutissent<br />
au décès après une évolution de quelques mois.<br />
Cependant, des formes à début tardif ou d’évolution plus<br />
lente, compatibles avec une survie prolongée ne sont pas<br />
exceptionnelles [146, 204] . Les anomalies oculomotrices apparaissent<br />
parfois très précocement et sont au premier plan. Il s’agit<br />
de strabisme, d’apraxie oculomotrice, de paralysies horizontales<br />
du regard, d’ophtalmoplégies internucléaires, de lenteur<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 403
Livre.book Page 404 Jeudi, 26. février 2009 3:40 15<br />
des saccades ou de secousses nystagmiques des yeux et de la<br />
tête, pouvant en imposer pour un spasmus nutans. Le syndrome<br />
de Leigh peut également se manifester par un tableau<br />
neurologique et général évocateur, au sein duquel s’intègrent<br />
les troubles oculomoteurs. Ce tableau général associe des<br />
vomissements diffus, une perte de poids, des anomalies respiratoires,<br />
une cardiomyopathie, des troubles de la conscience,<br />
des crises comitiales, un retard psychomoteur, une ataxie<br />
cérébelleuse et un syndrome pyramidal. À un stade plus tardif,<br />
peut s’observer une atrophie optique, témoignant d’une<br />
progression des foyers de nécrose à la substance blanche<br />
cérébrale.<br />
Le diagnostic de syndrome de Leigh repose sur la mise en<br />
évidence du dysfonctionnement de la chaîne respiratoire. Le<br />
rapport lactate/pyruvate dans le sang et, surtout, dans le<br />
liquide céphalorachidien est anormalement élevé. Les anomalies<br />
neuroradiologiques sont très évocatrices quoique non<br />
spécifiques. Elles traduisent une atteinte de la substance grise,<br />
particulièrement au niveau des ganglions de la base, mais<br />
s’étendant également aux pédoncules cérébraux et à la région<br />
de l’aqueduc de Sylvius. En IRM, elles se manifestent par une<br />
diminution de signal lors des séquences en T1 et d’hypersignaux<br />
lors des séquences en T2 [45, 146, 151] . À un stade plus tardif,<br />
les examens neuroradiologiques mettent également en<br />
évidence des anomalies de la substance blanche. Des lésions<br />
focales de démyélinisation, de gliose, de nécrose parfois<br />
spongiforme et des proliférations capillaires sont retrouvées<br />
histologiquement.<br />
Génétique<br />
Le syndrome de Leigh est lié à un déficit de la production<br />
énergétique cellulaire. Il peut être dû à l’existence de mutations<br />
affectant soit le génome nucléaire, soit le génome mitochondrial.<br />
Les mitochondries sont les principales sources<br />
énergétiques cellulaires ; le contrôle de leur structure et de<br />
leur activité, ainsi que l’organisation de la chaîne respiratoire<br />
sont sous la dépendance conjointe des génomes mitochondrial<br />
et nucléaire.<br />
Trois modes de transmission ont été rapportés, chacun<br />
d’eux étant caractéristique d’un ou plusieurs gènes mutés,<br />
dont dépendraient l’âge de début et le mode évolutif de ce<br />
syndrome [60, 180] . Ainsi, le syndrome de Leigh peut être transmis<br />
selon un mode récessif lié au chromosome X en cas de<br />
mutation dans le gène de la sous-unité E 1α du complexe de la<br />
pyruvate déshydrogénase (CPDH). La transmission s’effectue<br />
selon un mode récessif autosomique lorsque la mutation<br />
porte sur le complexe IV de la chaîne respiratoire, en particulier<br />
en présence d’une mutation du gène SURF-1 [209] . Enfin,<br />
elle est de type maternel en cas de mutation du génome mitochondrial<br />
[60] .<br />
La première mutation du génome nucléaire a été mise en<br />
évidence dans la sous-unité E α du CPDH, complexe constitué<br />
de trois sous-unités, E 1, E 2 et E 3 , après qu’une transmission liée<br />
au chromosome X du syndrome de Leigh eut été évoquée<br />
[129] . Le gène de cette sous-unité E α est localisé au niveau<br />
du bras court du chromosome X, en Xp22.2-p22.1. Plusieurs<br />
mutations ponctuelles ont été décrites, pouvant être responsables<br />
d’une diminution d’affinité de la sous-unité E α pour son<br />
substrat, la thiamine pyrophosphate, ce qui confirme le caractère<br />
hétérogène des mutations au sein de cette sous-unité<br />
E α [125, 147] . Des mutations ont également été rapportées dans la<br />
sous-unité E 3 de la CPDH [82] .<br />
404 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
Plusieurs mutations ont été mises en évidence au niveau<br />
du gène de la flavoprotéine, sous-unité de la succinate déshydrogénase,<br />
ou complexe II de la chaîne respiratoire, localisé<br />
en 5p15 et dont un pseudogène est localisé en 3q29 [166, 219] . Le<br />
caractère délétère de ces mutations sur l’activité de ce<br />
complexe II a pu être confirmé : elles entraînent soit le<br />
remplacement d’une arginine chargée positivement par un<br />
tryptophane neutre ou la transformation en leucine d’une<br />
méthionine au niveau du codon d’initiation de lecture [166] .<br />
Un déficit de l’activité de la cytochrome c oxydase (COX),<br />
ou complexe IV, est également associé au syndrome de<br />
Leigh [60, 180] . Cette COX est composée de treize sous-unités,<br />
dont les trois principales sont codées par le génome mitochondrial<br />
et les autres par le génome nucléaire. Dans le syndrome<br />
de Leigh, son déficit est souvent d’origine nucléaire,<br />
comme Tiranti a pu le démontrer à l’aide de cultures de fibroblastes<br />
hybrides constitués, d’une part, du cytoplasme de<br />
fibroblastes sains injecté dans des fibroblastes provenant d’un<br />
patient porteur du syndrome de Leigh et débarrassés de leur<br />
ADNmt, et, d’autre part, des cellules saines fusionnées avec<br />
des cellules issues du même patient [208] . Dans le premier<br />
groupe, les cellules hybrides ne présentent aucune activité<br />
COX, alors que celle-ci est retrouvée dans le second groupe.<br />
Grâce à cette même technique de fusion cellulaire, il a été<br />
possible d’une part de rétablir un phénotype COX + chez sept<br />
patients présentant un déficit d’activité de la COX et d’autre<br />
part de déterminer la localisation du gène responsable du<br />
déficit en COX sur le chromosome 9. Par analyse de liaison<br />
génétique, étude d’accidents de recombinaison et transfert de<br />
chromosomes dans des cellules, un intervalle de 4,5 cM<br />
contenant ce gène a été déterminé, correspondant à la bande<br />
chromosomique 9q34 [233] . La taille de cet intervalle a permis<br />
l’utilisation de la méthode des gènes candidats, aboutissant à<br />
l’identification du gène SURF-1 [157, 233] . Ce gène est l’homologue<br />
humain du gène de levure Shy-1. À l’état normal, la protéine<br />
SURF-1 pénètre dans la mitochondrie et participe à<br />
l’assemblage de la COX à partir de ces différents sous-complexes<br />
précurseurs [209] . En son absence, les quatre premières<br />
sous-unités de la COX ne peuvent être réunies [209] . En revanche,<br />
le rôle de cette protéine sur la synthèse des différentes<br />
sous-unités de la COX n’est pas élucidé. Plus de trente mutations<br />
différentes du gène SURF-1 ont été rapportées chez<br />
quarante patients. Ces mutations sont responsables de la synthèse<br />
d’une protéine tronquée et/ou d’une perte de fonction<br />
de la protéine [171] . Cependant, ces mutations ne rendent<br />
compte que de 75 % des observations de syndrome de Leigh<br />
par déficit en COX [209] . D’autres sous-unités de la COX peuvent<br />
présenter des altérations, telles que la sous-unité III. Une<br />
insertion d’une cytosine au nucléotide 9537 de cette sousunité<br />
est responsable d’un décalage du cadre de lecture aboutissant<br />
à la création d’un codon stop et à la synthèse d’une<br />
protéine tronquée. Dans une forme particulière du syndrome<br />
de Leigh, dite de type Saguenay-Lac Saint Jean, le déficit<br />
d’activité de la COX est lié à une mutation du gène LRPPRC,<br />
localisé sur le chromosome 2 en 2p21-p16 [140] .<br />
Deux mutations différentes à l’état hétérozygote dans le<br />
gène de la sous-unité NDUFS8 ont été mises en évidence<br />
chez un jeune garçon présentant un syndrome de Leigh avec<br />
déficit d’activité du complexe I de la chaîne respiratoire.<br />
D’autres mutations ont par la suite été retrouvées dans les<br />
gènes d’origine nucléaire d’autres sous-unités du complexe I,<br />
les sous-unités NDUFS7, NDUFV1 et NDUFS4 [22, 172] . Des<br />
mutations ont également été retrouvées dans le gène d’origine<br />
mitochondriale de la sous-unité 5 du complexe I [45, 204] .
Livre.book Page 405 Jeudi, 26. février 2009 3:40 15<br />
Enfin, une mutation a été découverte dans un gène<br />
nucléaire d’une sous-unité du complexe III (BCS1L) de la<br />
chaîne respiratoire et une autre dans celui de l’ATP6 d’origine<br />
mitochondriale. Un déficit fonctionnel en coenzyme Q, un<br />
transporteur d’électrons des complexes I et II au complexe III<br />
de la chaîne respiratoire, a également été rapporté chez un<br />
enfant porteur d’un syndrome de Leigh associé à des troubles<br />
hépatique et pancréatique.<br />
MALADIE DE WILSON<br />
La maladie de Wilson (MW) est définie par une accumulation<br />
de cuivre dans le foie, le système nerveux central, le rein et<br />
l’œil [71] . Les manifestations cliniques sont parfois précoces —<br />
avant l’âge de dix ans —, mais l’évolution est le plus souvent<br />
lente et les manifestations hépatique ou neurologique peuvent<br />
n’apparaître qu’après 55 ans. L’atteinte hépatique se<br />
manifeste par une cirrhose à gros foie. Elle peut aboutir à une<br />
hépatite fulminante chez l’adulte jeune. Les manifestations<br />
neurologiques traduisent l’atteinte des noyaux gris centraux.<br />
Les patients développent des troubles extrapyramidaux avec<br />
tremblement, dysarthrie et rigidité, ataxie et mouvements<br />
choréo-athétosiques (fig. 27-10). Il peut également être noté<br />
une tubulopathie, une anémie hémolytique, des troubles du<br />
rythme cardiaque ou des douleurs articulaires.<br />
L’anneau de Kayser-Fleischer, par dépôts de cuivre en périphérie<br />
de la cornée, est très évocateur de MW, mais inconstant<br />
et souvent incomplet, n’étant présent que chez un tiers<br />
des patients environ (fig. 27-11). Une cataracte en « fleur de<br />
tournesol » est également caractéristique mais peu <strong>fr</strong>équente.<br />
Une infiltration choriorétinienne péripapillaire est possible<br />
(fig. 27-12).<br />
Les manifestations neuro-ophtalmologiques témoignant de<br />
l’atteinte des structures oculomotrices, associent des paralysies<br />
de fonction à type de paralysie du regard volontaire vertical<br />
puis horizontal, une atteinte de la convergence et de<br />
l’accommodation et une apraxie d’ouverture des paupières.<br />
Fig. 27-10 – Jeune homme atteint d’une maladie de Wilson. Rictus<br />
particulier secondaire à des mouvements choréo-athétosiques du visage,<br />
témoins des manifestations neurologiques. (Collection de J.-L. Dufier.)<br />
Fig. 27-11 – Dépôts de cuivre en périphérie cornéenne, aboutissant à la<br />
formation d’un anneau de Kayser-Fleischer. Cet anneau est ici incomplet,<br />
limité à la portion supérieure de la cornée. (Collection de J.-L. Dufier.)<br />
Fig. 27-12 – Infiltration choriorétinienne verdâtre en anneau<br />
péripapillaire au cours d’une maladie de Wilson.<br />
(Collection de J.-L. Dufier.)<br />
Le traitement des manifestations neurologiques et hépatiques<br />
repose sur deux chélateurs du cuivre : le sulfate de zinc<br />
et la D-pénicillamine. Cependant, l’utilisation de cette dernière<br />
reste controversée car elle pourrait aggraver les manifestations<br />
neurologiques. Sous traitement, l’anneau de Kayser-<br />
Fleischer se <strong>fr</strong>agmente puis disparaît progressivement mais<br />
incomplètement et constitue un bon test de surveillance thérapeutique.<br />
La transplantation hépatique constitue une alternative<br />
intéressante en cas d’atteinte hépatique sévère. Enfin,<br />
un traitement préventif chez des patients porteurs de mutations<br />
à l’état homozygote semble réduire l’évolution de la<br />
maladie vers des manifestations symptomatiques [230] .<br />
La MW est transmise selon le mode récessif autosomique.<br />
Dans la population générale, la <strong>fr</strong>équence d’une mutation à<br />
l’état hétérozygote est évaluée à 1,1 % et la prévalence de la<br />
MW est estimée à 0,3 pour 10 000, hormis en Sardaigne où<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 405
Livre.book Page 406 Jeudi, 26. février 2009 3:40 15<br />
elle est plus importante. Cette affection est due à une anomalie<br />
du transport du cuivre du compartiment intracellulaire, où<br />
il s’accumule, vers les secteurs extracellulaires, en particulier<br />
vers la cœruléoplasmine et vers la bile. Ce passage transmembranaire<br />
est assuré par un transporteur membranaire ATPdépendant<br />
de type P, situé à la face interne de la membrane<br />
cellulaire et codé par le gène ATP7B [55] . Ce gène est localisé<br />
au niveau du bras long du chromosome 13, en 13q14.3q21.1<br />
[114] . Du fait de sa très grande taille, environ 80 kb,<br />
l’étude d’haplotypes spécifiques d’anomalies géniques, à<br />
l’aide de microsatellites et de polymorphismes (répétition de<br />
paires de nucléotides CA), permet de rechercher plus facilement<br />
l’existence de mutations [27] . Celles-ci sont nombreuses,<br />
aboutissant à une absence de synthèse ou à la synthèse d’un<br />
transporteur tronqué et/ou non fonctionnel [71] . Les différentes<br />
formes que prend le transporteur muté permettent d’expliquer<br />
la diversité des tableaux cliniques, en particulier quant à<br />
l’âge d’apparition des désordres hépatiques et cérébraux. Les<br />
mutations semblent différer selon l’origine géographique des<br />
patients. En Europe, la mutation HIS1069GLN, la plus <strong>fr</strong>équente<br />
(28 à 42 % selon les études), altère la configuration de<br />
la protéine et provoque une accélération de sa dégradation. Il<br />
semble exister un effet fondateur de cette mutation retrouvée<br />
soit à l’état homozygote, soit à l’état hétérozygote dans la<br />
population européenne. Compte tenu du grand nombre de<br />
mutations existantes et du statut d’hétérozygote composite<br />
des patients atteints, le diagnostic prénatal nécessite d’associer<br />
une analyse de liaison génétique à une recherche directe<br />
de mutation.<br />
MALADIE<br />
DE STEELE-RICHARDSON-OLSZEWSKI<br />
La maladie de Steele-Richardson-Olszewski (MSRO), encore<br />
dénommée paralysie supranucléaire progressive, réalise un<br />
syndrome extrapyramidal associé à une paralysie supranucléaire<br />
de la verticalité du regard. L’évolution, différente de<br />
celle observée lors des syndromes parkinsoniens, se fait vers<br />
la survenue d’un état démentiel et vers le décès en quelques<br />
années. Quoique de nombreuses observations soient sporadiques,<br />
la MSRO peut être familiale, transmise selon un mode<br />
dominant autosomique. Le gène responsable a été identifié.<br />
Ce gène MAPT (Microtubule-associated Protein Tau) est également<br />
responsable d’autres affections neurodégénératives telles<br />
que la maladie de Pick, une forme de démence pré-sénile,<br />
ou une forme de maladie de Parkinson avec démence.<br />
Aspects cliniques<br />
La MSRO débute par l’apparition d’un syndrome extrapyramidal<br />
avec un ralentissement des mouvements vers l’âge de<br />
65 ans en moyenne, comme la maladie de Parkinson. Mais<br />
elle en diffère par la rigidité axiale précoce, amenant le corps<br />
en hyperextension, alors que le tremblement est peu important.<br />
Les troubles de l’équilibre sont également sévères, aggravés<br />
par la rigidité axiale et l’akinésie, et sont volontiers<br />
sources de chutes <strong>fr</strong>équentes. Les plaintes à type de flou<br />
visuel ou de véritables épisodes de diplopie sont précoces et<br />
<strong>fr</strong>équentes. L’atteinte oculomotrice est caractéristique et réalise<br />
une paralysie supranucléaire intéressant les mouvements<br />
verticaux, qui sont difficiles à initier et dont l’amplitude est<br />
limitée. L’atteinte affecte d’abord les mouvements dirigés<br />
vers le bas, les saccades, puis les mouvements de poursuite.<br />
406 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
En quelques mois, tous les mouvements verticaux puis horizontaux<br />
deviennent limités. Mais l’amplitude de ces mouvements<br />
verticaux est d’autant plus grande que la taille du<br />
stimulus est importante, ce qui traduit une anomalie supranucléaire<br />
[193] . Il s’associe au déficit oculomoteur une apraxie de<br />
l’ouverture palpébrale [232] . Les troubles du langage sont<br />
secondaires aux troubles moteurs, mais ils peuvent aussi<br />
s’intégrer dans un tableau de fléchissement des fonctions<br />
supérieures, aboutissant à une démence. Les patients ne<br />
répondent pas aux traitements par la L-dopa et l’évolution se<br />
fait vers le décès en quelques années. Une variabilité<br />
d’expression clinique de la MSRO a été retrouvée au sein de<br />
certaines <strong>fr</strong>atries, les troubles de l’équilibre ou la démence<br />
pouvant être plus ou moins au premier plan. Cette variabilité<br />
phénotypique risque de faire sous-estimer la <strong>fr</strong>équence de<br />
cette affection et de ses formes familiales. De plus, elle pose<br />
des problèmes diagnostique et nosologique difficiles avec une<br />
maladie de Parkinson associée à une démence. La maladie de<br />
Parkinson avec démence est elle aussi associée à des mutations<br />
survenant dans le gène MAPT, mais ces mutations sont<br />
différentes de celles de la MSRO. De plus, sa symptomatologie<br />
est proche de celle de la MSRO. Ces deux affections diffèrent<br />
moins par les troubles ophtalmologiques — réalisant<br />
l’une et l’autre une paralysie supranucléaire verticale — que<br />
par l’aspect de la rigidité axiale : les patients parkinsoniens<br />
sont courbés vers l’avant, alors que les patients porteurs de<br />
MSRO restent droits. L’analyse histologique dans la MSRO<br />
met en évidence des amas neurofibrillaires dans les neurones<br />
sous-corticaux et dans les cellules gliales, ainsi que des territoires<br />
de gliose sans plaque sénile, contrairement à la maladie<br />
d’Alzheimer.<br />
Génétique<br />
La plupart des observations de MSRO sont sporadiques, mais<br />
la <strong>fr</strong>équence des formes familiales est sans doute sous-estimée.<br />
Cette affection neurodégénérative est transmise selon<br />
un mode dominant autosomique à pénétrance incomplète,<br />
quoique, dans une <strong>fr</strong>atrie espagnole, la transmission évoque<br />
un mode récessif autosomique. Un polymorphisme de répétition<br />
dinucléotidique a été identifié dans l’intron 9 du gène<br />
MAPT localisé en 17q21.1. Ce polymorphisme a été utilisé<br />
pour confirmer l’association de différentes affections neurodégénératives,<br />
dont la MSRO, avec ce gène MAPT [53] . Cinq<br />
haplotypes différents, A0, A1, A2, A3 et A4, ont été définis<br />
en fonction du nombre de répétition de dinucléotides. Les<br />
patients porteurs de MSRO sont plus volontiers homozygotes<br />
pour l’allèle A0 (génotype A0/A0), alors que celui-ci est moins<br />
représenté dans la population saine. Deux haplotypes, H1 et<br />
H2, couvrant l’ensemble du gène MAPT et recoupant les<br />
haplotypes de l’intron 9 ont été identifiés. Une sur-représentation<br />
de l’haplotype H1 réalisant le génotype H1/H1 a été<br />
retrouvée chez les patients porteurs d’une MSRO [16] . En<br />
revanche, le génotype H2/H2 n’a été retrouvé chez aucun<br />
patient MSRO. Deux mutations du gène MAPT responsables<br />
de MSRO ont été rapportées [177] .<br />
Le gène MAPT code six isoformes de la protéine tau obtenues<br />
par épissage alternatif. Cette protéine tau appartient à la<br />
famille des microtubule-associated proteins qui participe à la<br />
polymérisation des microtubules intracellulaires, en association<br />
avec la tubuline. Ces isoformes diffèrent par le nombre<br />
de répétitions d’un ensemble de 18 acides aminés dans la portion<br />
carboxyterminale de la protéine qui assure la fixation de<br />
la protéine tau aux microtubules. Dans les neurones sains, les
Livre.book Page 407 Jeudi, 26. février 2009 3:40 15<br />
isoformes à trois ou quatre répétitions de cet ensemble de<br />
18 acides aminés sont présentes en quantité égale. Mais le<br />
profil biochimique de cette « tauopathie » résulte en l’accumulation<br />
anormale et prépondérante d’isoformes tau avec<br />
quatre motifs répétés. Quoique ces deux isoformes aient la<br />
même capacité de polymérisation des microtubules, celle à<br />
quatre répétitions les stabilise plus fortement. Il en résulterait<br />
une altération de la dynamique de ces microtubules. Une augmentation<br />
du taux de l’isoforme à quatre répétitions est responsable<br />
d’une démence et d’une mort cellulaire. Un<br />
équilibre correct entre isoformes à trois ou quatre répétitions<br />
nécessite une intégrité de l’exon 10 et de l’intron 10 [141] . L’une<br />
des mutations de la MSRO se trouve dans l’intron 10. La<br />
seconde mutation altérerait la capacité de la protéine tau à<br />
initier l’assemblage des microtubules, mais non la quantité de<br />
microtubules formés [177] .<br />
MALADIE DE NIEMANN-PICK<br />
La maladie de Niemann-Pick (MNP) est une sphingomyélinose,<br />
sous-catégorie des sphingolipidoses, caractérisée par<br />
une accumulation de sphingomyéline dans le réticulum<br />
endoplasmique et de cholestérol dans les organelles intracellulaires.<br />
Selon l’âge d’apparition et la symptomatologie prédominante,<br />
cinq formes de MNP ont été cliniquement<br />
isolées. Les anomalies oculomotrices s’observent uniquement<br />
dans la MNP de type C, encore dénommée syndrome<br />
DAF (Downgaze palsy, Ataxia-athetosis, Foamy macrophages).<br />
Celle-ci correspond à la forme chronique avec neuropathie,<br />
encore qualifiée de juvénile subaiguë. Elle rassemble plusieurs<br />
phénotypes selon l’âge d’apparition. La forme infantile<br />
apparaît précocement entre 2 et 4 ans et évolue vers une<br />
régression des acquisitions alors que surviennent des troubles<br />
neurologiques à type d’ataxie et de crises comitiales.<br />
Ces troubles neurologiques s’associent à une paralysie supranucléaire.<br />
Celle-ci se manifeste initialement par une paralysie<br />
du regard volontaire vertical vers le bas. Secondairement, la<br />
motilité oculaire horizontale est altérée par atteinte des centres<br />
de commande ponto-mésencéphaliques. Les réflexes<br />
vestibulo-oculaires sont préservés. L’atteinte viscérale est<br />
moins marquée qu’au cours des formes précédentes. Le<br />
décès survient entre 5 et 15 ans. Des formes plus tardives,<br />
pouvant survenir à l’adolescence ou à l’âge adulte, donnent<br />
des manifestations cliniques identiques mais d’évolution très<br />
lentement progressive. Cette MNP de type C est due dans<br />
95 % des cas à la présence de mutations dans le gène NPC1<br />
localisé en 18q11-q12 [41] . Ce gène code une glycoprotéine<br />
comportant treize domaines transmembranaires, principalement<br />
localisée au niveau du cerveau dans les cellules gliales<br />
proches des terminaisons synaptiques [220] . Cette protéine<br />
participe au transport intracellulaire du cholestérol vers la<br />
membrane cellulaire ou vers le réticulum endoplasmique. Les<br />
5 % restants sont dus à une mutation dans le gène NPC2<br />
localisé en 14q24.3, qui code une protéine lysosomale pouvant<br />
se lier au cholestérol. Ainsi, la physiopathogénie de la<br />
forme C de la NMP apparaît liée, d’une part, à une anomalie<br />
de transport ou de stockage du cholestérol libre au sein de la<br />
cellule aboutissant à une réduction de l’activité de la sphingomyélinase<br />
lysosomale, et, d’autre part, à des accumulations<br />
de microfibrilles intraneuronales, identiques à celles<br />
retrouvées dans la maladie d’Alzheimer, mais sans dépôt<br />
amyloïde. La forme D de MNP correspond à une variante de<br />
la MNP de type C, particulièrement <strong>fr</strong>équente en Nouvelle<br />
Écosse du fait d’un effet fondateur. Les manifestations dues<br />
à la surcharge seraient plus précoces que dans la MNP de<br />
type C.<br />
La MNP de type A correspond à la forme infantile de<br />
début précoce, au cours des six premiers mois. Il est noté<br />
chez les nourrissons une hépatosplénomégalie avec ictère,<br />
des troubles neurologiques sévères avec retard mental et<br />
retard des acquisitions. Les manifestations ophtalmologiques<br />
associent une tache rouge cerise, des opacités cornéennes et<br />
des anomalies cristalliniennes [225] . Cependant, l’atteinte<br />
maculaire peut être limitée à un halo [201] . Le décès survient<br />
vers l’âge de trois ans. Cette forme est due à des mutations<br />
dans le gène de la sphingomyéline phosphodiestérase-1, localisé<br />
en 11p15.4-p15.1, qui code la sphingomyélinase. Ces<br />
mutations font perdre son activité catalytique à la protéine<br />
qui clive la sphingomyéline en phosphorylcholine et céramide.<br />
La MNP de type B est une forme viscérale pure, sans<br />
atteinte neurologique. L’atteinte ophtalmologique est souvent<br />
limitée à un halo maculaire, sans tache rouge cerise (fig. 27-13).<br />
Cependant, cette dernière a été rapportée à plusieurs reprises<br />
chez des enfants porteurs d’une authentique MNP de type<br />
B [214] . Les manifestations hépatiques et spléniques sont identiques<br />
à celles observées lors de la forme A. D’autres anomalies<br />
viscérales, pulmonaires, vasculaires sont susceptibles de<br />
survenir chez ces patients atteignant l’âge adulte. Les mutations<br />
affectent également le gène de la sphingomyéline phosphodiestérase-1,<br />
mais la protéine synthétisée garde une<br />
activité enzymatique réduite suffisante pour éviter l’apparition<br />
des troubles neurologiques.<br />
Le diagnostic prénatal se fait par détermination de l’activité<br />
sphingomyélinase sur les villosités choriales ou à partir<br />
des cellules du liquide amniotique dans les types A et B. Pour<br />
le type C, le diagnostic prénatal repose sur la recherche<br />
d’anomalies cellulaires évocatrices. Il est possible de retrouver<br />
une proportion importante d’hétérozygotes dans les familles<br />
mais le dépistage des hétérozygotes est encore imparfait.<br />
Fig. 27-13 – Chez un enfant porteur d’une maladie de Niemann-Pick<br />
de type B, l’examen du fond d’œil objective un halo maculaire avec tache<br />
rouge cerise. (Collection de J.-L. Dufier.)<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 407
Livre.book Page 408 Jeudi, 26. février 2009 3:40 15<br />
III – APRAXIES OCULOMOTRICES ET ANOMALIES OCULOMOTRICES APPARENTÉES<br />
Une apraxie oculomotrice constitue la principale manifestation<br />
de l’apraxie congénitale de Cogan, au cours de laquelle<br />
seule la motilité oculaire horizontale est altérée. Cette même<br />
anomalie oculomotrice ou des anomalies oculomotrices peu<br />
différentes s’observent également dans des affections telles<br />
que l’ataxie-télangiectasie de Denise Louis-Bar, le syndrome<br />
de Joubert et l’hypoplasie vermienne isolée, la chorée de<br />
Huntington ou la maladie de Gaucher.<br />
APRAXIE CONGÉNITALE<br />
OCULOMOTRICE DE COGAN<br />
L’apraxie oculomotrice de Cogan (AOMC) est une anomalie<br />
congénitale et idiopathique, caractérisée par une anomalie de<br />
l’initiation des saccades volontaires horizontales s’améliorant<br />
avec l’âge. Quoique les formes sporadiques soient les plus<br />
<strong>fr</strong>équentes, un gène responsable de formes héréditaires serait<br />
localisé sur le bras long du chromosome 2, en 2q13, à proximité<br />
du gène NPHP1, responsable de la néphronophtise [23] .<br />
Symptomatologie et diagnostic<br />
Au cours de l’AOMC, seules les saccades volontaires horizontales<br />
sont perturbées. En revanche, les saccades réflexes et<br />
les phases rapides des nystagmus sont préservées, de même<br />
que les mouvements de poursuite. L’AOMC est une affection<br />
congénitale dont les manifestations ne deviennent évidentes<br />
que lorsque les bébés sont capables de maintenir leur tête et<br />
d’en contrôler les mouvements. En effet, les patients vont<br />
développer une stratégie visuelle reposant sur la réalisation de<br />
clignements palpébraux, afin de perdre la fixation initiale, suivis<br />
d’un mouvement brusque de la tête dirigé vers la cible<br />
périphérique qu’ils souhaitent fixer mais en la dépassant. Lors<br />
de ce mouvement céphalique rapide d’acquisition de la cible,<br />
les yeux effectuent un mouvement de contraversion du fait<br />
de la persistance du réflexe vestibulo-oculaire (phénomène<br />
des « yeux de poupée »). Puis, lorsque la fixation est assurée,<br />
la tête et les yeux reviennent en position primaire tout en<br />
continuant à fixer l’objet souhaité. Le mouvement céphalique<br />
ne serait pas uniquement un mécanisme de compensation<br />
mais il pourrait s’intégrer dans des syncinésies oculocéphaliques<br />
facilitant l’initiation des saccades. Ces manifestations<br />
ont tendance à s’atténuer dans le temps et elles ne sont presque<br />
plus perceptibles dès l’adolescence, hormis lors de situations<br />
de stress ou de fatigue [175] . L’AOMC est généralement<br />
isolée. Néanmoins, l’existence d’un retard des acquisitions ou<br />
de troubles de l’élocution est parfois signalée. Il est possible<br />
d’observer des malformations cérébrales à type d’agénésie du<br />
corps calleux, de porencéphalie, de syndrome de Dandy-Walker<br />
ou d’hypoplasie vermienne [91] . Cette dernière malformation<br />
est intéressante du point de vue de la nosologie et de la<br />
compréhension des mécanismes physiopathogéniques à<br />
l’origine de l’AOMC. Au sein d’une même <strong>fr</strong>atrie, certains<br />
patients porteurs d’une AOMC peuvent présenter une hypoplasie<br />
vermienne alors que le cervelet apparaît normal chez<br />
d’autres [91] . Mais les anomalies cérébelleuses peuvent être<br />
purement histologiques ou biochimiques [91] .<br />
408 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
Génétique<br />
La plupart des AOMC sont sporadiques. Néanmoins, avant<br />
d’éliminer une forme familiale, il faut rechercher de très discrètes<br />
anomalies des saccades horizontales chez les parents,<br />
puisque les manifestations cliniques vont devenir imperceptibles<br />
avec l’âge [175] . Les formes familiales d’AOMC rapportées<br />
dans la littérature sont peu nombreuses et présentent parfois<br />
quelques particularités intéressantes pour l’étude de la transmission<br />
génétique. Dans deux familles, les enfants porteurs<br />
d’AOMC sont des jumeaux monozygotes [188] . Une consanguinité<br />
au premier degré a été retrouvée dans deux <strong>fr</strong>atries<br />
différentes [86] . Une transmission d’un père à ses quatre<br />
enfants (un garçon et trois filles dont des jumelles) dans une<br />
<strong>fr</strong>atrie et une transmission d’un père à sa fille dans une autre<br />
ont été rapportées [96, 175] . La structure de ces différentes <strong>fr</strong>atries<br />
ne permet pas de porter de conclusion quant au mode de<br />
transmission de l’AOMC. Une transmission dominante autosomique<br />
est plausible devant l’existence de transmissions<br />
père-fils et de patients atteints sur deux générations au<br />
moins [96, 175] . Cependant, aucun de ces différents éléments ne<br />
constitue un argument déterminant du fait du très faible<br />
nombre de générations concernées. Il n’est donc pas possible<br />
d’éliminer une transmission récessive autosomique avec<br />
pseudodominance, en faveur de laquelle il faut retenir l’existence<br />
d’une consanguinité au sein de certaines <strong>fr</strong>atries et le<br />
grand nombre de patients atteints dans une même génération<br />
[86] .<br />
Aucun gène de l’AOMC n’est identifié. Une localisation,<br />
encore incertaine, a été proposée au niveau du bras long du<br />
chromosome 2 dans la région 2q13. L’association d’une<br />
AOMC à une néphronophtise, rapportée par Betz chez deux<br />
enfants, ne semble pas fortuite et pourrait entrer dans le cadre<br />
des syndromes de gènes contigus [23] . Une délétion dans la<br />
région du gène de la néphronophtise NPHP1, localisé en<br />
2q13, a été retrouvée chez ces deux enfants. Chez un enfant,<br />
cette large délétion concerne les deux chromosomes, alors<br />
que chez le second enfant, la délétion ne touche qu’un chromosome<br />
mais une mutation ponctuelle dans le gène de la<br />
néphronophtise est retrouvée sur le second chromosome.<br />
Cependant, Takano évoque que le gène NPHP1 puisse jouer<br />
un rôle important dans le développement du tissu rénal, mais<br />
aussi du tronc cérébral et du cervelet [203] . Toutefois, aucune<br />
mutation de ce gène NPHP1 n’a encore été décrite à ce jour<br />
au cours de l’AOMC.<br />
HYPOPLASIE VERMIENNE<br />
L’hypoplasie vermienne est caractérisée par l’existence d’un<br />
syndrome cérébelleux présent dès la naissance et strictement<br />
non évolutif, associant des troubles moteurs, une ataxie<br />
motrice des membres et du tronc ou une dysmétrie. Les troubles<br />
oculomoteurs associent un nystagmus vertical ou horizontal<br />
à une ataxie optique perturbant les mouvements<br />
oculaires horizontaux et verticaux — contrairement à ce qui<br />
est observé lors de l’AOMC. Le développement intellectuel<br />
est normal. Aucune anomalie systémique n’est retrouvée, ce<br />
qui permet de différencier cette affection du syndrome de
Livre.book Page 409 Jeudi, 26. février 2009 3:40 15<br />
Joubert ou de la néphronophtise [203] . Les examens neuroradiologiques<br />
confirment l’existence d’une atrophie cérébelleuse<br />
prédominant dans la région vermienne et retrouvent<br />
parfois une augmentation des sillons des hémisphères cérébelleux<br />
ou un « signe de la molaire » [34] . Celui-ci traduit l’existence<br />
d’une hypoplasie vermienne aboutissant à un<br />
élargissement de l’espace interpédonculaire associé à des anomalies<br />
de la jonction ponto-mésencéphalique. Cet aspect<br />
radiologique n’est pas propre à l’hypoplasie vermienne isolée.<br />
Il est systématiquement retrouvé lors du syndrome de Joubert<br />
et il peut l’être au cours de l’apraxie oculomotrice de Cogan<br />
et de la néphronophtise [203] . Les nombreuses observations<br />
d’hypoplasie vermienne familiale publiées permettent d’évoquer<br />
une transmission dominante autosomique, avec cependant<br />
un excès de filles atteintes. La localisation du gène de<br />
l’hypoplasie vermienne n’est pas connue.<br />
SYNDROME DE JOUBERT<br />
Le syndrome de Joubert est caractérisé par l’existence<br />
d’une hypoplasie vermienne associée à des manifestations<br />
générales et à des anomalies neuroradiologiques très évocatrices.<br />
Les patients sont volontiers porteurs d’une dysmorphie<br />
avec un <strong>fr</strong>ont proéminent, des oreilles bas situées, une<br />
implantation haute des sourcils et un épicanthus. L’atteinte<br />
générale est marquée par une tachypnée en période néonatale,<br />
un retard des acquisitions et du développement psychomoteur,<br />
une hypotonie, une ataxie. Un retard mental, parfois<br />
profond, est quasi constant. Les manifestations ophtalmologiques<br />
sévères, responsables d’une cécité ou d’une profonde<br />
malvoyance, peuvent associer une dystrophie rétinienne atypique<br />
ou pouvant en imposer pour une amaurose congénitale<br />
de Leber, un colobome choriorétinien ou du nerf optique et<br />
des troubles de la motilité oculaire horizontale et verticale à<br />
type d’apraxie optique, de nystagmus de type see-saw ou<br />
d’abolition de la poursuite. La neuro-imagerie confirme la<br />
présence de malformations importantes au niveau de la fosse<br />
postérieure, à type d’hypoplasie ou d’aplasie vermienne,<br />
d’élargissement de l’espace interpédonculaire et d’anomalies<br />
de la jonction ponto-mésencéphalique avec des pédoncules<br />
cérébelleux supérieurs épaissis. Ces malformations réalisent<br />
le classique « signe de la molaire » sur les coupes axiales de<br />
l’IRM (fig. 27-14). Il peut s’y associer une malformation de<br />
Dandy-Walker et une agénésie du corps calleux. Les examens<br />
neuroradiologiques objectivent également des anomalies des<br />
noyaux du tronc cérébral, qui peuvent être hypoplasiques ou<br />
<strong>fr</strong>agmentés, ce qui explique les troubles respiratoires et oculomoteurs.<br />
Le syndrome de Joubert est transmis selon un mode<br />
récessif autosomique. Plusieurs gènes responsables de ce syndrome<br />
ont été localisés ou identifiés. Le premier gène a été<br />
localisé en 1999 au sein de quatre familles consanguines sur le<br />
bras long du chromosome 9 en 9q34.3. Il est associé à un syndrome<br />
de Joubert typique nommé JBTS1. Natacci a évoqué<br />
l’existence d’un deuxième gène localisé en 17p11.2, chez un<br />
enfant également atteint d’un syndrome de Smith-Magenis.<br />
L’étude chromosomique a mis en évidence une délétion dans<br />
cette région du bras court du chromosome 17 [150] . Toutefois,<br />
aucune liaison génétique n’a pu être retrouvée chez plus de<br />
vingt et un patients atteints d’un syndrome de Joubert non lié<br />
au chromosome 9 [25] . Récemment, un troisième gène,<br />
nommé AHI1, et responsable d’un syndrome de Joubert<br />
appelé JBTS3, a été identifié sur le bras long du chromo-<br />
Fig. 27-14 – « Signe de la molaire » sur une coupe axiale d’IRM passant<br />
par la jonction ponto-mésencéphalique, chez un enfant porteur d’un<br />
syndrome de Joubert. Cette coupe permet d’observer l’épaississement<br />
des pédoncules cérébelleux supérieurs et l’atrophie vermienne. (Collection<br />
de J.-L. Dufier.)<br />
some 6, en 6q23.3. Ce gène, qui possède un domaine SH3 et<br />
des sites de liaison SH3 et qui code une protéine dénommée<br />
joubertine, est particulièrement exprimé dans les neurones<br />
qui formeront les pédoncules cérébelleux supérieurs [61] . Un<br />
quatrième gène responsable d’un syndrome cérébello-oculorénal,<br />
CORS2 ou JBTS2, a été localisé en 2003 sur le bras<br />
court du chromosome 11, en 11p12-q13.3 [108] . Ce syndrome<br />
est considéré comme une variante du syndrome de Joubert,<br />
puisque sa présentation clinique en est peu différente et<br />
qu’est retrouvée la caractéristique « image en molaire » au<br />
cours des examens neuroradiologiques. En revanche, ce syndrome<br />
s’accompagne d’anomalies rénales peu sévères à type<br />
de dysplasie kystique ou de néphronophtise [218] . Aucune<br />
mutation n’a pu être retrouvée dans les gènes candidats localisés<br />
sur cette région du chromosome 11 et qui ont été testés<br />
jusqu’à présent [25] . Enfin, des mutations dans le gène de la<br />
néphronophtyse, NPHP1, localisé en 2q13, ont été retrouvées<br />
chez plusieurs enfants porteurs soit d’un syndrome de Joubert<br />
peu sévère soit d’un tableau évocateur d’un syndrome de<br />
Joubert associé à des anomalies systémiques, en particulier<br />
hépatiques. Ce gène de la néphronophtise code la néphrocystine,<br />
une protéine signal comportant un domaine SH3, qui<br />
pourrait jouer un rôle important dans le développement du<br />
tissu rénal, mais aussi du tronc cérébral et du cervelet [203] .<br />
MALADIE OU CHORÉE DE HUNTINGTON<br />
La maladie de Huntington (MH) est une affection dégénérative<br />
du système central dont la <strong>fr</strong>équence est de l’ordre de<br />
0,7 pour 10 000 individus. Cette affection lentement progressive<br />
débute exceptionnellement avant l’âge de vingt ans. Elle<br />
se manifeste par la survenue de mouvements choréiques et<br />
par une démence de plus en plus marquée. Le décès survient<br />
après une évolution de dix-sept ans en moyenne. Cependant,<br />
on observe une grande variabilité phénotypique de la MH.<br />
Les manifestations oculaires portent essentiellement sur<br />
l’oculomotricité. Les saccades horizontales deviennent précocement<br />
hypométriques et ralenties, avec une difficulté d’ini-<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 409
Livre.book Page 410 Jeudi, 26. février 2009 3:40 15<br />
tiation des saccades volontaires réalisant une apraxie du<br />
regard peu différente de celle observée lors de l’AOMC [229] .<br />
L’instabilité de la fixation et la distractibilité du regard sont<br />
responsables de saccades réflexes involontaires. Ces anomalies<br />
oculomotrices sont interprétées comme la conséquence<br />
de lésions <strong>fr</strong>onto-caudées. À un stade plus avancé de la maladie,<br />
l’atteinte oculomotrice porte également sur les saccades<br />
verticales et sur la poursuite.<br />
La MH est transmise selon un mode dominant autosomique<br />
avec pénétrance complète. Le gène de la MH, nommé<br />
IT15 (Important Transcript 15) a été localisé sur le bras court du<br />
chromosome 4 en 4p16.3 en 1989, puis identifié en 1993. Il<br />
comporte un polymorphisme par un nombre de répétitions<br />
variable de triplets de nucléotides CAG localisés dans sa<br />
séquence codante. Cette augmentation de triplets CAG aboutit<br />
à une augmentation de motifs polyglutamates au niveau<br />
de la protéine codée par ce gène. Le nombre de répétitions,<br />
inférieur à 30 chez les sujets sains, est supérieur à 38 chez les<br />
patients atteints de MH. Les patients porteurs de 36 à 40 triplets<br />
peuvent rester asymptomatiques [189] . Le nombre de triplets<br />
peut s’accroître de génération en génération, de manière<br />
plus importante lorsque la transmission est paternelle. Le risque<br />
de passer au-delà de la barrière des 38 triplets est plus<br />
grand en cas de MH dans la <strong>fr</strong>atrie [213] . Cette différence pourrait<br />
être sous la dépendance de facteurs liés aux chromosomes<br />
X ou Y, ou due à une sélection négative des ovocytes<br />
porteurs d’un grand nombre de triplets. De plus, Trottier a<br />
noté l’existence d’une corrélation négative entre le nombre de<br />
répétitions et l’âge d’apparition des symptômes [213] . Cette<br />
augmentation du nombre des répétitions permet de comprendre<br />
le phénomène d’anticipation, la MH apparaissant de plus<br />
en plus tôt de génération en génération ; mais elle rend également<br />
plus difficile le conseil génétique puisqu’un enfant<br />
atteint peut naître d’un père ayant un nombre de triplets<br />
intermédiaire. La taille de l’allèle « sain » influence également<br />
l’âge d’apparition de la maladie [62] . La recherche directe de<br />
l’expansion des triplets CAG par PCR et électrophorèse sur<br />
gel d’agarose permet de confirmer le diagnostic en l’absence<br />
d’antécédents familiaux. En revanche, le diagnostic présymptomatique<br />
ne doit être envisagé que chez un patient à risque<br />
cliniquement indemne et désireux de ce test. Le diagnostic<br />
prénatal est possible si l’un des parents est porteur du gène<br />
muté et a donc lui-même réalisé le test diagnostique. Le gène<br />
IT15 code une protéine ubiquitaire dénommée huntingtine,<br />
n’appartenant à aucune famille protéique connue [213] . La MH<br />
serait la conséquence du déclenchement de signaux pro-apoptotiques.<br />
La liaison d’une protéine dénommée Huntingtin-<br />
Interacting Protein-1 (HIP1) au <strong>fr</strong>agment aminoterminal de<br />
l’huntingtine serait perturbée du fait de l’élongation des<br />
motifs polyglutamates. Cette HIP1 en excès formerait un<br />
hétérodimère pro-apoptotique avec l’HIP1 protein-interactor.<br />
Par ailleurs, le <strong>fr</strong>agment aminoterminal de l’huntingtine se<br />
clive au sein des neurones et devient intranucléaire. Ce <strong>fr</strong>agment<br />
interagit alors avec des facteurs transcriptionnels intranucléaires<br />
et réprime la synthèse de la protéine P53. Enfin,<br />
Zuccato a mis en évidence le rôle de l’huntingtine pour réprimer<br />
le neuron-restrictive silencer element, en piégeant son activateur<br />
au niveau cytoplasmique, et pour induire la synthèse<br />
d’un facteur de croissance, le BDNF, nécessaire au trophisme<br />
des neurones [236] . Ces différents mécanismes, non opposés,<br />
permettent d’approcher la physiopathogénie de la MH.<br />
Trois pour cent environ des patients dont la symptomatologie<br />
est identique à celle de la MH n’ont pas d’anomalie du<br />
nombre des triplets CAG au niveau du gène IT15 et sont por-<br />
410 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
teurs d’une phénocopie de la MH. La Huntington disease-like 2<br />
est due à une augmentation du nombre de triplets CAG au<br />
niveau d’un des exons du gène JPH3, localisé en 16q24.3 et<br />
codant une protéine dénommée junctophiline-3 [95] . Cette<br />
protéine de la famille des junctophilines est un élément des<br />
complexes assurant la jonction entre le réticulum endoplasmique<br />
et la membrane cellulaire au niveau des cellules<br />
excitables et utilisant des canaux calciques. Deux autres phénocopies<br />
de la MH, respectivement Huntington disease-like 1 et<br />
Huntington disease-like 3, ont été rapportées. La première est<br />
due à la présence d’une insertion dans le gène PrNP de la protéine<br />
PrP (prion), localisée au niveau de la portion terminale<br />
du bras court du chromosome 20 (20pter-p12). Le gène Huntington<br />
disease-like 3 est localisé au niveau du chromosome 4,<br />
en 4p15.3.<br />
ATAXIE-TÉLANGIECTASIE<br />
DE DENISE LOUIS-BAR<br />
L’ataxie-télangiectasie de Denise Louis-Bar est une affection<br />
récessive autosomique qui associe des désordres oculomoteurs<br />
et des télangiectasies conjonctivales à des troubles neurologiques,<br />
un déficit immunitaire et une susceptibilité<br />
particulière aux tumeurs malignes. Une sensibilité particulière<br />
de la chromatine aux radiations ionisantes et l’augmentation<br />
des cassures de l’ADN sont également importantes pour le<br />
diagnostic et la constitution de sous-groupes de cette maladie.<br />
Chez les patients homozygotes, l’ataxie cérébelleuse,<br />
d’apparition précoce et progressive par dégénérescence des<br />
cellules de Purkinje, s’associe à une neuropathie périphérique<br />
dont témoignent l’abolition des réflexes tendineux et la fonte<br />
musculaire, un syndrome extrapyramidal, des mouvements<br />
choréo-athétosiques et un retard mental très inconstant.<br />
L’apraxie oculomotrice est peu différente de celle observée<br />
dans le syndrome de Cogan (cf. supra), quoique le défaut<br />
d’initiation des saccades concerne également les saccades verticales<br />
et s’associe à des anomalies de la poursuite et, parfois,<br />
à un nystagmus (fig. 27-15). Un strabisme est retrouvé chez<br />
plus de 30 % des patients. Ces anomalies oculomotrices précèdent<br />
l’apparition des télangiectasies conjonctivales, quasi<br />
constantes à partir de 3 ou 5 ans dans l’aire d’ouverture des<br />
fentes palpébrales (fig. 27-16). Elles peuvent atteindre la face.<br />
Le déficit immunitaire est dû à une diminution de synthèse<br />
des IgA et des IgG et, à un moindre degré, des IgM et des IgE,<br />
avec une diminution du nombre des plasmocytes. Il explique<br />
la susceptibilité particulière de ces enfants aux infections,<br />
principalement des voies aériennes supérieures et bronchiques,<br />
avec formation de bronchectasies. Le risque de développer<br />
une leucémie lymphoïde de type T, un lymphome malin<br />
de type B ou une tumeur maligne solide est accru chez les<br />
homozygotes atteints. Les porteurs hétérozygotes auraient<br />
aussi un risque accru de développer une tumeur maligne, en<br />
particulier du sein chez la femme, soit par susceptibilité aux<br />
toxiques et/ou aux radiations ionisantes, soit par perte de<br />
l’allèle sain dans une lignée de cellules somatiques réalisant<br />
un mécanisme identique à la perte d’un gène suppresseur de<br />
cancer. Ces données sont très controversées. Le diagnostic<br />
peut être porté devant l’augmentation de l’α-fœtoprotéine et<br />
la diminution des immunoglobulines dans le sang. L’augmentation<br />
de la susceptibilité d’une cellule lymphocytaire aux<br />
radiations ionisantes et l’augmentation de lésions de la chromatine<br />
constituent les tests les plus fiables quoique difficiles<br />
à réaliser.
Livre.book Page 411 Jeudi, 26. février 2009 3:40 15<br />
a b<br />
c<br />
Fig. 27-16 – Multiples télangiectasies conjonctivales dans la fente<br />
d’ouverture palpébrale chez un enfant atteint d’ataxie-télangiectasie<br />
de Denise Louis-Bar. (Collection de J.-L. Dufier.)<br />
Le gène ATM de l’ataxie-télangiectasie est localisé sur le<br />
chromosome 11, en 11q23.3 ; il comporte 66 exons. Il code<br />
une sérine/thréonine protéine kinase, principalement localisée<br />
dans le noyau et impliquée dans la régulation du cycle cellu-<br />
Fig. 27-15 – Ataxie-télangiectasie de Denise Louis-Bar chez un<br />
jeune garçon. Lors des saccades horizontales volontaires, cet enfant<br />
réalise un mouvement de contraversion oculaire. Noter la présence<br />
de télangiectasies conjonctivales bilatérales dans la fente d’ouverture<br />
palpébrale. a. Lors d’une saccade dirigée vers la droite, cet enfant<br />
effectue un mouvement de la tête qui dépasse la cible et s’associe à<br />
un phénomène des « yeux de poupée ». b. Puis, ses yeux commencent<br />
à se recentrer alors que la tête revient vers la cible. c. La tête<br />
et les yeux sont centrés sur la cible. (Collection de J.-L. Dufier.)<br />
laire et dans la détection et l’induction de la réparation des<br />
cassures des brins d’ADN [13] . Cette protéine kinase possède<br />
un domaine phosphatidylinositol-3-kinase (PI3K). Plusieurs<br />
mutations ont été mises en évidence dans la région codant ce<br />
domaine hautement conservé entre les espèces, responsables<br />
de la synthèse de protéines tronquées ou de l’absence de protéine.<br />
Elles affectent le contrôle du cycle cellulaire et de la<br />
réparation des brins d’ADN puisque ce domaine PI3K régule<br />
la phosphorylation du p53 en réponse à certaines agressions<br />
contre l’ADN, comme une irradiation [191] . Cette absence de<br />
phosphorylation permettrait d’expliquer la survenue de certaines<br />
tumeurs, en particulier hématologiques. De plus, la<br />
protéine Atm est impliquée dans le déclenchement de l’apoptose<br />
des neurones dont le patrimoine génétique est altéré, en<br />
interaction avec p53 et la protéine Bax [46] . Ses mutations<br />
expliqueraient une diminution de l’apoptose lors du développement<br />
cérébral, source de lésions neurologiques précoces. La<br />
protéine Atm possède plusieurs autres domaines, dont le site<br />
de liaison c-Abl, le motif leucine-zipper et la région de liaison<br />
avec la β-adaptine. Atm interagit avec de nombreuses protéines<br />
nucléaires également impliquées dans la réparation de<br />
l’ADN, telles que le complexe MRE11/RAD50/NBS1, activé<br />
en présence d’une rupture des deux brins de l’ADN et sous<br />
dépendance de la phosphorylation de la protéine Nbs1 par la<br />
protéine Atm. Quoique cette affection soit récessive autosomique,<br />
les variations du phénotype en réponse à une irradiation<br />
dépendent du type de mutations, dont certaines peuvent<br />
avoir un effet négatif pseudodominant [192] .<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 411
Livre.book Page 412 Jeudi, 26. février 2009 3:40 15<br />
APRAXIE OCULOMOTRICE<br />
AVEC ATAXIE<br />
Cette entité a été décrite par Aicardi en 1988. Les anomalies<br />
neurologiques et ophtalmologiques sont peu différentes de<br />
celles observées lors du syndrome d’ataxie-télangiectasie,<br />
mais celles-ci ne s’accompagnent d’aucun déficit immunitaire.<br />
En revanche, il peut exister une hypoalbuminémie. Cette<br />
affection apparaît dans l’enfance — âge moyen de sept ans<br />
environ. Les manifestations choréiques sont précoces et<br />
s’atténuent avec le temps. Il existe néanmoins une hétérogénéité<br />
phénotypique corrélée à la nature des mutations géniques.<br />
Les autres anomalies neurologiques sont un syndrome<br />
cérébelleux avec atrophie du cervelet en IRM, une neuropathie<br />
périphérique. Le retard mental est souvent rapporté, mais<br />
semble inconstant. L’apraxie optique s’accompagne de mouvements<br />
de la tête dans de nombreux cas, comme dans<br />
l’apraxie de Cogan ou l’ataxie-télangiectasie. En revanche,<br />
chez ces patients, il n’est pas noté de télangiectasies conjonctivales.<br />
Ce syndrome, transmis selon un mode récessif autosomique,<br />
est secondaire à la présence d’anomalies dans le gène de<br />
l’aprataxine (APTX) localisé en 9p13.3 [141] . Par épissage alternatif,<br />
ce gène code deux isoformes de cette protéine ubiquitaire<br />
appartenant à la famille des « triades histidines » et qui<br />
possède également un motif en doigt de zinc liant l’ADN.<br />
Cette protéine possède une activité d’hydroxylation et de<br />
réparation de cassures des brins d’ADN [142] .<br />
SYNDROMES MYASTHÉNIQUES<br />
Les myasthénies constituent un ensemble de maladies affectant<br />
la transmission synaptique au niveau de la jonction neuromusculaire.<br />
Leur caractéristique clinique est l’existence<br />
d’une faiblesse musculaire variable et progressive au cours de<br />
la journée, qui prend l’aspect d’une fatigabilité. La jonction<br />
neuromusculaire est une structure complexe, constituée de<br />
nombreuses protéines dont les différents gènes peuvent être<br />
porteurs d’anomalies génétiques. Une classification fondée sur<br />
ces mécanismes physiopathogéniques a permis d’établir plusieurs<br />
sous-groupes au sein des syndromes myasthéniques.<br />
Ceux-ci répondent à au moins deux modes de transmission<br />
génétique, dominant autosomique et récessif autosomique.<br />
CLASSIFICATION<br />
Il faut différencier les myasthénies néonatales, congénitales,<br />
infantiles et les formes de l’adulte.<br />
L’origine exacte des myasthénies néonatales n’est pas totalement<br />
élucidée. S’il est évoqué un passage transplacentaire<br />
d’anticorps maternels anti-récepteurs à l’acétylcholine (Ac-<br />
ARACh) vers le fœtus lors de la grossesse, ce mécanisme ne<br />
permet pas d’expliquer toutes les myasthénies néonatales. En<br />
effet, des Ac-ARACh sont retrouvés chez la plupart des<br />
412 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
IV – MYOPATHIES<br />
MALADIE DE GAUCHER<br />
La maladie de Gaucher entre dans le cadre des sphingolipidoses.<br />
Il s’agit d’une cérébrosidose liée à un déficit en β-glucocérébrosidase.<br />
Ce déficit enzymatique aboutit à une<br />
accumulation de glucocérébroside dans les différents tissus de<br />
l’organisme. Le diagnostic repose sur le dosage de l’activité de<br />
la β-glucocérébrosidase dans les leucocytes circulants. Il<br />
existe trois types de maladie de Gaucher. Le type I ne comporte<br />
aucune atteinte neurologique. Le type II réalise une<br />
atteinte sévère avec des troubles neurologiques précoces et<br />
un décès avant l’âge d’1 an. Le type III associe des troubles<br />
hématologiques, hépatiques, osseux et pulmonaires précoces<br />
pouvant aboutir à une hypertension artérielle pulmonaire, des<br />
troubles neurologiques (ataxie, paraplégie, démence, comitialité)<br />
et neuro-ophtalmologiques à type d’apraxie oculomotrice<br />
verticale et horizontale. Un traitement par enzymologie<br />
recombinante est actuellement disponible et permet de normaliser<br />
les paramètres hépatique et hématologique et de<br />
ralentir l’évolution des troubles neurologiques. Cette maladie<br />
à transmission récessive autosomique est due à la présence de<br />
mutations dans le gène de la β-glucocérébrosidase, localisé<br />
sur le chromosome 1, en 1q21. Un diagnostic prénatal peut<br />
être réalisé, soit par mesure de l’activité enzymatique des villosités<br />
choriales à 10-12 semaines d’aménorrhée ou des cellules<br />
amniotiques en culture vers 16 semaines d’aménorrhée,<br />
soit par biologie moléculaire — mais il est alors rendu complexe<br />
par la présence d’un pseudogène de la β-glucocérébrosidase,<br />
proche du gène transcrit, à très forte homologie<br />
nucléotidique. Il n’est proposé que dans les cas de maladie de<br />
Gaucher de type II ou III.<br />
enfants nés de mères myasthéniques alors que seule la moitié<br />
de ces enfants développe des manifestations cliniques notables.<br />
De plus, des enfants dont la symptomatologie est caractéristique<br />
peuvent naître de mères en rémission ou chez<br />
lesquelles les Ac-ARACh ne sont plus décelables. Enfin, le risque<br />
d’avoir un deuxième enfant atteint d’une myasthénie<br />
néonatale est plus élevé quand un premier enfant a lui-même<br />
été atteint. Une susceptibilité particulière, éventuellement<br />
fondée sur un facteur HLA, ou d’origine génétique a été évoquée<br />
mais non prouvée.<br />
Les myasthénies congénitales héréditaires sont parfois difficiles<br />
à différencier des formes infantiles avec lesquelles elles<br />
partagent le même âge de début des manifestations. Il ne<br />
s’agit pas de pathologies auto-immunes et il n’est jamais<br />
retrouvé d’Ac-ARACh. Elles résultent de l’atteinte de l’une<br />
des différentes étapes de la transmission synaptique au<br />
niveau de la jonction neuromusculaire. La dépolarisation nerveuse<br />
entraîne la fusion de vésicules d’acétylcholine avec la<br />
membrane présynaptique et la libération de ce neurotransmetteur.<br />
Une partie de l’acétylcholine se lie aux récepteurs à<br />
l’acétylcholine (RACh). Cette fixation de l’acétylcholine à son<br />
récepteur ouvre un canal cationique passif au sein du récepteur<br />
pour une durée d’environ 2 ms. La dépolarisation induite<br />
génère un potentiel d’action qui provoque la contraction musculaire.<br />
Le reste de l’acétylcholine libérée est dégradé par<br />
l’acétylcholinestérase avant d’atteindre les RACh, permettant
Livre.book Page 413 Jeudi, 26. février 2009 3:40 15<br />
de réguler la transmission synaptique. Selon le mécanisme<br />
physiopathogénique, la réponse des traitements anticholinestérasiques<br />
est variable.<br />
Une classification internationale sépare les myasthénies<br />
congénitales en trois groupes :<br />
– le groupe I, de transmission récessive autosomique, est<br />
lui-même divisé en quatre sous-groupes : Ia, myasthénie<br />
congénitale familiale ; Ib, myasthénie des ceintures ; Ic, myasthénie<br />
congénitale par déficit en acétylcholinestérase ; Id,<br />
myasthénie congénitale par anomalie des récepteurs de l’acétylcholine<br />
;<br />
– le groupe II correspond aux myasthénies congénitales<br />
postsynaptiques dominantes autosomiques dites « à canal<br />
lent » par mutations dans les gènes des différentes sous-unités<br />
du récepteur nicotinique à l’acétylcholine. Ces myasthénies<br />
congénitales entrent dans le cadre des canalopathies. Les<br />
mutations sont responsables d’anomalies structurelles au<br />
niveau du canal cationique qui altèrent le passage ionique<br />
transmembranaire au sein du RACh ;<br />
– les cas sporadiques forment le groupe III.<br />
Outre l’âge de début, les myasthénies infantiles diffèrent<br />
des myasthénies de l’adulte par la <strong>fr</strong>équence et la sévérité<br />
des manifestations ophtalmologiques. Des Ac-ARACh sont<br />
volontiers retrouvés lors de ces myasthénies auto-immunes,<br />
souvent associées à d’autres pathologies partageant la même<br />
déviation du système immunitaire [215] . Les myasthénies<br />
infantiles et de l’adulte sont exceptionnellement familiales<br />
[116] .<br />
ASPECTS CLINIQUES<br />
Nous ne reviendrons pas sur la variabilité de la faiblesse musculaire<br />
au cours de la journée, en fonction du degré de fatigue<br />
du patient. Cette fatigabilité est mise à profit dans les différents<br />
tests diagnostiques.<br />
Manifestations cliniques<br />
de la myasthénie néonatale<br />
Elles apparaissent précocement, parfois avant la naissance<br />
sous forme d’hydramnios ou de diminution des mouvements<br />
fœtaux, ou lors des trois premiers jours de vie. Elles peuvent<br />
rapidement mettre en jeu le pronostic vital par détresse respiratoire<br />
[57] . Les troubles oculomoteurs sont peu <strong>fr</strong>équents,<br />
observés uniquement dans environ 15 % des cas dans cette<br />
forme dominée par les difficultés à la succion, une hypotonie<br />
ou une diplégie faciale. Cette myasthénie régresse en une<br />
semaine à deux mois, temps nécessaire pour que les anticorps<br />
d’origine maternelle soient éliminés.<br />
Premiers signes de la myasthénie<br />
congénitale<br />
Ces signes sont retrouvés avant l’âge de 2 ans dans 42 % des<br />
observations et avant l’âge de 20 ans dans 60 % des cas [35] .<br />
Néanmoins, l’apparition d’une myasthénie dès la naissance<br />
ou dans les premières années de vie oriente vers cette forme<br />
de myasthénie. Chez l’enfant, la symptomatologie de la<br />
myasthénie congénitale est peu différente de celle de la myasthénie<br />
juvénile. Les manifestations ophtalmologiques, parésie<br />
oculomotrice, ptosis et strabisme, sont relativement constants<br />
(fig. 27-17). Mullaney insiste sur l’existence de formes de gravités<br />
différentes et souligne que les troubles oculomoteurs<br />
sont au premier plan lors de formes de gravité moyenne [145] .<br />
L’évolution de la symptomatologie peut se faire vers l’amélioration<br />
avec l’âge, mais elle est variable en fonction du gène<br />
muté et du type de mutation.<br />
Fig. 27-17 – Présence d’un ptosis bilatéral chez un jeune garçon atteint<br />
d’une myasthénie congénitale. (Collection de J.-L. Dufier.)<br />
Myasthénie auto-immune<br />
L’atteinte de la musculature respiratoire y est souvent au premier<br />
plan chez l’enfant comme chez l’adulte et fait toute la<br />
gravité de l’affection. Les manifestations neuro-ophtalmologiques<br />
sont <strong>fr</strong>équentes, observées chez 85 à 96 % des patients<br />
à un moment quelconque de l’évolution. Elles réalisent des<br />
parésies oculomotrices, inaugurales dans près de la moitié des<br />
cas, impliquant principalement les muscles droit interne, droit<br />
inférieur, oblique supérieur ou de releveur de la paupière<br />
supérieure, ce qui entraîne diplopie et ptosis. L’atteinte de<br />
l’orbiculaire des paupières est rare. En revanche, la musculature<br />
intrinsèque n’est jamais affectée puisque les neuromédiateurs<br />
en jeu sont différents. Le ptosis, retrouvé chez plus de<br />
90 % des enfants myasthéniques, peut parfois s’accompagner<br />
d’une rétraction de la paupière supérieure controlatérale en<br />
raison de la loi de Hering [111] . Il faut signaler l’importance des<br />
strabismes, retrouvés dans plus de 85 % des cas au cours des<br />
myasthénies de l’enfant. Il s’agit le plus souvent d’exotropies,<br />
parfois combinées avec des strabismes verticaux [111] . La variabilité<br />
dans le temps de ces strabismes permet d’orienter le<br />
diagnostic. Les manifestations neuro-ophtalmologiques restent<br />
plus souvent isolées chez l’enfant (35 % de formes oculaires<br />
pures pour Mullaney) que chez l’adulte (10 % de<br />
formes oculaires pures) [145] . S’il doit y avoir généralisation,<br />
celle-ci survient le plus souvent au cours des deux premières<br />
années. La myasthénie auto-immune intéresse également les<br />
muscles des ceintures, de la face et du cou ou du carrefour<br />
oropharyngé. Des régressions spontanées ont été rapportées<br />
après deux ans d’évolution avec une <strong>fr</strong>équence variant entre<br />
10 et 35 % selon l’âge des patients et les séries [145] . Agius a<br />
proposé une classification en trois groupes des myasthénies<br />
auto-immunes, en fonction de la cible principale des autoanticorps<br />
: récepteurs à l’acétylcholine, récepteurs à l’acétylcholine<br />
et protéine myocardique titine, kinase musculaire [7] .<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 413
Livre.book Page 414 Jeudi, 26. février 2009 3:40 15<br />
GÉNÉTIQUE<br />
Les nombreuses formes de myasthénie congénitale sont<br />
secondaires à des mutations dans différents gènes et suivent<br />
plusieurs modes de transmission.<br />
Myasthénie congénitale de type I<br />
Les quatre formes de myasthénie congénitale de type I sont<br />
toujours transmises selon un mode récessif autosomique.<br />
Type Ia<br />
Un premier gène de la myasthénie congénitale de type Ia,<br />
FIMG1, a été localisé en 1997 par Christodoulou dans la<br />
région télomérique du bras court du chromosome 17, au<br />
niveau de la bande 17p13 [47] . Le gène de la synaptobrévine-2,<br />
localisé par Zoraqi dans la région télomérique du bras court<br />
du chromosome 17, est un gène candidat de cette myasthénie<br />
FIMG1. Il code une protéine dont la fonction reste encore mal<br />
connue, mais qui serait impliquée dans la libération de l’acétylcholine<br />
(ACh) dans la fente synaptique, à une étape encore<br />
non précisée. Cette protéine réalise des complexes avec<br />
d’autres protéines, la syntaxine et la synaptotagmine d’une<br />
part, la synaptophysine d’autre part, qui fusionnent avec des<br />
complexes similaires de la membrane synaptique.<br />
La myasthénie congénitale Ia par mutation du gène CHAT<br />
(FIMG2), décrite pour la première fois en 2001 chez cinq nouveau-nés<br />
non apparentés, apparaît dès la naissance. Elle se<br />
caractérise par la survenue d’épisodes aigus de faiblesse musculaire,<br />
de paralysies bulbaires et de déficits respiratoires survenant<br />
à la suite d’efforts ou lors de poussées de fièvre.<br />
L’évolution de ces épisodes aigus peut être fatale. Au repos et<br />
en dehors de poussées, les enregistrements électromyographiques<br />
et l’enregistrement des potentiels de plaque postsynaptique<br />
sont normaux. En revanche, ces potentiels sont diminués<br />
après cinq minutes de stimulation évoquant un défaut de<br />
resynthèse ou de stockage vésiculaire de l’ACh. Ces observations<br />
ont permis d’identifier deux gènes candidats, le gène<br />
VACHT permettant le transport de l’ACh dans ses vésicules<br />
de stockage, et le gène CHAT (choline acétyltransférase),<br />
localisé sur le chromosome 10q11.2. Celui-ci code la protéine<br />
permettant la synthèse de l’ACh à partir de l’acétyl-coenzyme<br />
A et de la choline au niveau des synapses cholinergiques.<br />
Les mutations de l’homologue du gène CHAT chez le<br />
ver Caenorhabditis elegans aboutissent à un déficit de la synthèse<br />
d’ACh. Ce déficit est responsable de troubles de la<br />
motilité de l’animal. Ohno a retrouvé dix mutations récessives<br />
du gène CHAT chez ces cinq nouveau-nés, causant soit<br />
l’absence de la protéine soit la synthèse d’une protéine à<br />
l’activité catalytique réduite [159] .<br />
Type Ib<br />
La myasthénie congénitale Ib, dite « des ceintures », de transmission<br />
récessive autosomique est particulière par sa localisation<br />
limitée aux ceintures sans aucune manifestation<br />
ophtalmologique. Aucun gène n’a encore été localisé.<br />
Type Ic<br />
La myasthénie congénitale Ic par déficit en acétylcholinestérase<br />
(AChE) au niveau de la jonction neuromusculaire a été<br />
décrite dès 1977 et est probablement la seconde cause de<br />
myasthénie congénitale. Les manifestations myasthéniques<br />
414 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
sévères sont présentes dès la naissance et s’aggravent lors des<br />
efforts, aboutissant parfois au décès. Elles ne répondent pas<br />
aux traitements par les AChE. L’AChE existe sous deux formes<br />
dans le muscle humain : une forme homomérique globuleuse<br />
libre et une forme hétéromérique fixée à la membrane<br />
synaptique. Cette forme enzymatique asymétrique est constituée<br />
d’un à trois tétramères et d’une queue, dont la structure<br />
proche de celle du collagène permet son ancrage à la<br />
membrane synaptique [158] . Lors de cette forme Ic de myasthénie<br />
congénitale, les tétramères sont présents, permettant<br />
d’exclure une mutation du gène codant leur synthèse. Plus de<br />
quinze mutations récessives ont été retrouvées dans le gène<br />
ColQ comportant dix-neuf exons et 71 618 paires de bases,<br />
localisé au niveau du bras court du chromosome 3, en 3p24.2.<br />
Ce gène code le système d’ancrage des tétramères [64] . Ces<br />
mutations aboutissent à l’absence de forme hétéromérique<br />
d’AChE et à son impossibilité de se fixer à la lame basale de<br />
la jonction neuromusculaire. Il existe un effet fondateur de la<br />
mutation G240X dans des familles palestiniennes [158] .<br />
Type Id<br />
L’existence d’une myasthénie congénitale Id par anomalie des<br />
RACh a été évoquée chez des patients atteints d’une myasthénie<br />
congénitale postsynaptique sans mutation dans les<br />
gènes codant les différentes sous-unités du RACh. Il existe<br />
deux phénotypes distincts de cette myasthénie Id [35] . Le premier,<br />
sévère, parfois léthal, apparaît très précocement. Les<br />
manifestations peuvent être présentes dès avant la naissance<br />
avec une diminution des mouvements fœtaux intra-utérins,<br />
ou observées dans la période néonatale. Elles sont toujours<br />
évidentes avant l’âge d’un an, marquées par une atteinte ophtalmologique,<br />
ptosis ou strabisme volontiers divergent, et une<br />
fatigabilité des membres. Des épisodes d’apnée et des crises<br />
aiguës d’insuffisance respiratoire sont <strong>fr</strong>équents, surtout lors<br />
des épisodes infectieux. Ce syndrome myasthénique précoce<br />
peut s’améliorer vers l’âge de six ans. À l’inverse, un second<br />
phénotype au cours duquel les manifestations myasthéniques<br />
sont tardives, débute à l’adolescence ou l’âge adulte, sans<br />
trouble respiratoire ni bulbaire. Le ptosis est <strong>fr</strong>équent. Des<br />
mutations ont été retrouvées dans le gène de la rapsyne<br />
(receptor-associated protein of synapses) localisé sur le bras court<br />
du chromosome 11, en 11p11.2-p11.1, et qui constitue un<br />
excellent gène candidat [67, 160] . La rapsyne joue un rôle essentiel<br />
dans l’ancrage du RACh à la membrane postsynaptique et<br />
est hautement conservée entre les espèces. La mutation fauxsens<br />
N88K paraît constante, puisqu’elle est retrouvée chez<br />
tous les patients présentant une myasthénie congénitale de<br />
type Id, soit à l’état homozygote, soit à l’état hétérozygote<br />
composite associée à une autre mutation.<br />
Myasthénies congénitales par mutation<br />
dans les gènes des différentes sous-unités<br />
du RACh nicotinique<br />
Cette catégorie regroupe des affections dont le cadre est plus<br />
large que celui du type II de la classification internationale<br />
(« canal lent »). Ces myasthénies entrent dans le cadre d’affections<br />
maintenant regroupées sous le terme de canalopathies.<br />
Les différentes mutations aboutissent à différentes anomalies<br />
structurelles du canal cationique et à une altération du transport<br />
ionique transmembranaire lors de l’activation du RACh.<br />
À ce jour, plus de cinquante mutations différentes ont été<br />
décrites et élucidées dans les gènes des sous-unités α, β, δ
Livre.book Page 415 Jeudi, 26. février 2009 3:40 15<br />
ou ε du RACh. Ces différentes mutations ponctuelles ou délétions<br />
affectent autant les domaines transmembranaires que<br />
les domaines intra- ou extracellulaires du RACh nicotinique<br />
et perturbent la transmission synaptique. Certaines de ces<br />
mutations ponctuelles ou délétions augmentent l’affinité de<br />
l’ACh pour son récepteur, aboutissant à une augmentation de<br />
la durée d’ouverture du canal cationique au sein du récepteur<br />
(slow-channel myasthenic syndrome). À l’inverse, les autres<br />
mutations diminuent la vitesse d’ouverture du canal<br />
cationique et accélèrent sa fermeture (fast-channel myasthenic<br />
syndrome). Il en résulte une diminution des potentiels postsynaptiques<br />
et une réduction du taux de canaux ouverts lors<br />
d’une stimulation. Enfin, ces mutations peuvent altérer le site<br />
pentamérique de liaison du RACh. L’anomalie fonctionnelle<br />
des RACh peut cependant être compensée par une augmentation<br />
du nombre de plaques postsynaptiques sur lesquelles ils<br />
sont fixés et/ou une augmentation de la quantité d’ACh libérée<br />
à chaque stimulation. Enfin, lorsque l’anomalie génétique<br />
affecte la sous-unité ε, une persistance de la sous-unité γ<br />
réduit les conséquences phénotypiques. En effet, chez le<br />
fœtus, les RACh musculaires sont constitués de cinq sousunités<br />
(deux sous-unités de type α et une sous-unité respectivement<br />
de type β, γ ou δ). La sous-unité γ est normalement<br />
remplacée par la sous-unité de type ε durant les deux<br />
semaines suivant la naissance. Les myasthénies slow-channel<br />
sont transmises selon un mode dominant autosomique,<br />
quoiqu’une transmission récessive autosomique soit possible<br />
lorsque la mutation porte sur la sous-unité ε du RACh. Les<br />
mutations responsables d’un fast-channel myasthenic syndrome<br />
ou d’un déficit d’expression du RACh sont transmises selon<br />
un mode récessif autosomique [196] .<br />
Gène de la sous-unité α du RACh nicotinique<br />
La myasthénie congénitale et « à canal lent » par mutation<br />
dans le gène de la sous-unité α peut se révéler dès l’enfance ;<br />
elle est alors sévère [197] . Bien souvent, elle débute à l’adolescence<br />
et s’aggrave à l’occasion des grossesses chez la femme.<br />
Le gène de la sous-unité α du RACh a été localisé sur le bras<br />
long du chromosome 2 en 2q24-q31. Ce gène comporte onze<br />
exons et code une protéine de 482 acides aminés. Par épissage<br />
alternatif, la sous-unité α du RACh existe sous deux isoformes<br />
P3A– et P3A+, cette dernière résultant de l’insertion<br />
d’un exon supplémentaire, P3A, compris entre les exons 3<br />
et 4. Ces deux isoformes sont retrouvées en proportions égales<br />
dans le tissu musculaire humain. L’isoforme P3A– n’est<br />
exprimée que dans le muscle, alors que la seconde l’est également<br />
dans le cerveau, le cœur, le rein, le poumon et le thymus.<br />
L’effet de certaines mutations sur l’activité du RACh a<br />
été étudié. La mutation N217K augmente l’affinité du RACh<br />
pour l’ACh et la mutation G153S entraîne une diminution du<br />
taux de dissociation entre l’ACh et son RACh. Ces mutations<br />
maintiennent le canal cationique transmembranaire en position<br />
ouverte ou augmentent sa <strong>fr</strong>équence d’ouverture, aboutissant<br />
à un blocage de la transmission synaptique. À<br />
l’inverse, la mutation V285I est responsable d’un ralentissement<br />
de la vitesse d’ouverture du canal cationique et de sa<br />
fermeture prématurée [226] . Les mutations S269I et V132L<br />
affectent chacune un domaine extracellulaire du RACh impliqué<br />
dans la fixation de l’ACh, tel que la boucle cystéine. La<br />
mutation V132L réduit d’un facteur 30 à 48 la capacité de<br />
fixation d’une première ou d’une seconde molécule d’ACh<br />
sur son RACh, mais seulement d’un facteur 2 l’ouverture du<br />
canal [197] . Un remodelage de la membrane postsynaptique<br />
permet de compenser les conséquences de cette mutation sur<br />
la transmission neuromusculaire.<br />
Gène de la sous-unité β 1 du RACh nicotinique<br />
Le phénotype associé à une mutation dans le gène de la sousunité<br />
β 1 est marqué par l’apparition précoce de manifestations<br />
myasthéniques affectant la musculature oculomotrice,<br />
faciale et des membres. L’évolution se fait vers une aggravation<br />
progressive, sans rémission à l’adolescence. Le gène de<br />
treize exons de la sous-unité β 1 du RACh a été localisé sur le<br />
bras court du chromosome 17, au niveau de la bande<br />
17p13.1 [21] . La mutation affectant le codon 263 est responsable<br />
d’une myasthénie « à canal lent » et du phénotype le plus<br />
sévère puisqu’elle multiplie par huit le temps d’ouverture du<br />
canal cationique et est responsable d’un remodelage de la<br />
membrane postsynaptique. Les délétions dans l’exon 3 et<br />
dans l’exon 8 sont responsables de myasthénies congénitales<br />
récessives autosomiques. Elles entraînent respectivement une<br />
perte d’interaction entre les sous-unités β 1 et δ du RACh et<br />
une anomalie de la surface pentamérique du RACh, ce qui<br />
aboutit à une diminution de fixation de l’ACh [178] .<br />
Gène de la sous-unité δ du RACh nicotinique<br />
L’existence d’une mutation dans le gène de la sous-unité δ du<br />
RACh nicotinique est toujours responsable d’un phénotype<br />
sévère, débutant parfois avant la naissance, avec une réduction<br />
des mouvements fœtaux et une ankylose articulaire à la<br />
naissance. Chez l’enfant ou l’adolescent, l’évolution peut<br />
imposer un déplacement en fauteuil roulant ou causer une<br />
réduction de la capacité respiratoire, pouvant atteindre 25 %,<br />
dont les complications peuvent être mortelles. L’atteinte ophtalmologique,<br />
qu’il s’agisse de ptosis ou de parésies oculomotrices,<br />
est <strong>fr</strong>équente. Le gène de la sous-unité δ a été d’abord<br />
localisé sur le bras long du chromosome 2 en 2q33-q34. Cette<br />
localisation est cependant contestée, le gène étant probablement<br />
en position plus distale, au-delà de la bande q36, éventuellement<br />
en 2q37.1. Au moins quatre mutations et une<br />
microdélétion ont été rapportées au niveau de ce gène de<br />
quatorze exons et 9 477 paires de bases [33] . Brownlow et<br />
Gomez ont rapporté des mutations récessives (S268P et<br />
E59K) responsables d’un syndrome myasthénique congénital<br />
« à canal rapide » [33] . Les autres mutations sont responsables<br />
de myasthénies « à canal lent » [196] .<br />
Gène de la sous-unité ε du RACh nicotinique<br />
Les myasthénies « à canal lent » par mutation du gène de la<br />
sous-unité ε du RACh nicotinique peuvent être transmises<br />
selon un mode récessif autosomique ou dominant autosomique.<br />
Le phénotype de ces myasthénies congénitales « à canal<br />
lent » est caractérisé par un début précoce, dès la période néonatale<br />
ou du moins durant la première année de vie, avec une<br />
atteinte sévère marquée par des épisodes de détresse respiratoire<br />
et la nécessité de se déplacer en fauteuil roulant dès<br />
l’enfance chez un tiers des patients. L’atteinte ophtalmologique,<br />
à type de ptosis et de parésies oculomotrices progressives<br />
et fluctuantes, est constante [4] . D’autres phénotypes ont<br />
été rapportés, avec un début plus tardif, jusqu’à 34 ans, une<br />
aggravation dans l’enfance et l’adolescence ou, à l’inverse,<br />
une rémission vers 10 ans [136] . Le gène de la sous-unité ε, qui<br />
code une protéine de 473 acides aminés et pour un peptide<br />
signal de 20 acides aminés, est localisé sur le chromosome 17,<br />
à 5 cM du gène de la sous-unité β 1 , probablement en 17p13.2.<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 415
Livre.book Page 416 Jeudi, 26. février 2009 3:40 15<br />
Les mutations de la sous-unité ε sont volontiers responsables<br />
d’une diminution du nombre de récepteurs postsynaptiques<br />
ou de leur perte de fonction [4, 136] . Il est admis que ces anomalies<br />
sont en partie compensées par une persistance de<br />
l’expression de la sous-unité γ. Elles peuvent également être<br />
responsables de syndromes myasthéniques « à canal lent ».<br />
Myasthénies auto-immunes familiales<br />
L’existence de myasthénies auto-immunes familiales a été<br />
bien étudiée. Les atteintes sont principalement retrouvées<br />
chez des <strong>fr</strong>ères et sœurs, les transmissions parents-enfants<br />
étant plus rares. Cependant, le taux de consanguinité est également<br />
très faible, ce qui n’est pas en faveur d’une transmission<br />
récessive autosomique. Ces myasthénies auto-immunes<br />
familiales ne répondent à aucune forme de transmission mendélienne.<br />
Il est possible qu’il n’existe qu’une prédisposition<br />
liée à l’auto-immunité, en particulier aux haplotypes du système<br />
d’histocompatibilité HLA. En effet, l’association de la<br />
myasthénie à d’autres maladies auto-immunes, troubles<br />
thyroïdiens et thymomes, est <strong>fr</strong>équente. En outre, il a été<br />
démontré une plus grande <strong>fr</strong>équence des haplotypes<br />
HLA DR3-B8-A1 chez des patients atteints d’une myasthénie<br />
auto-immune d’apparition précoce ou associée à une hyperplasie<br />
thymique [77] . En revanche, l’haplotype HLA DR11 est<br />
volontiers associé à la présence d’un thymome. Giraud évoque<br />
l’existence d’une liaison entre le locus HLA D et un locus<br />
qu’il nomme MYAS1 situé sur le chromosome 6 en<br />
6p21.3 [77] . Lors de la myasthénie auto-immune, les auto-anticorps<br />
sont dirigés contre les différentes sous-unités du RACh,<br />
mais principalement contre les sous-unités α et ε. Le thymus<br />
exprime des auto-anticorps contre ces différentes sous-unités,<br />
de même que la sous-unité β 1, mais non la sous-unité δ.<br />
L’apparition de ces auto-anticorps met en jeu de nombreux<br />
systèmes : les cytokines de l’inflammation du groupe Tumor<br />
Necrosis Factor ou la voie du complément.<br />
MYOPATHIE DE DUCHENNE<br />
La myopathie de Duchenne est une maladie essentiellement<br />
musculaire, due à une mutation dans le gène DMD codant la<br />
dystrophine. Les premiers signes de cette affection apparaissent<br />
très précocement, avant l’âge de trois ans. L’atteinte porte<br />
d’abord sur la musculature striée sous forme d’une faiblesse<br />
musculaire responsable de troubles de la marche. Cette<br />
atteinte de la musculature squelettique est d’évolution progressive<br />
mais elle empêche tout déplacement autonome avant<br />
l’âge de dix ans. Ce déficit musculaire contraste avec une<br />
peusdo-hypertrophie musculaire qui résulte du remplacement<br />
du tissu musculaire par un tissu fibreux et adipeux. Un retard<br />
mental peut être observé, mais il ne semble pas corrélé à des<br />
génotypes particuliers. L’atteinte musculaire peut également<br />
concerner la musculature lisse. L’atteinte myocardique est<br />
constante, survenant progressivement au cours de l’évolution<br />
et pouvant aboutir à une défaillance cardiaque. D’autres signes<br />
d’atteintes de la musculature lisse peuvent être observés, en<br />
particulier au niveau digestif. L’atteinte ophtalmologique se<br />
manifeste essentiellement sous la forme d’anomalies du système<br />
scotopique à l’électrorétinogramme, avec une diminution<br />
d’amplitude de l’onde b en condition scotopique alors<br />
que l’onde a est normale et bien que les patients ne se plaignent<br />
pas de cécité nocturne ni de trouble de l’adaptation à<br />
l’obscurité. De plus, s’il n’est observé aucun déficit patent de<br />
la motilité oculaire cliniquement, les enregistrements oculo-<br />
416 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
moteurs mettent en évidence un ralentissement de la vitesse<br />
des saccades, d’autant plus important que la cible à fixer est<br />
plus excentrée [120] . Biochimiquement, il apparaît très tôt une<br />
élévation de la créatine kinase dans le sang, témoignant de la<br />
dégénérescence musculaire. La mort survient vers 20 ans, probablement<br />
du fait de troubles de la régulation potassique.<br />
Les symptômes de la dystrophie musculaire de Becker ne<br />
diffèrent de ceux de la myopathie de Duchenne que par une<br />
apparition plus tardive et un retentissement moindre. L’espérance<br />
de vie est plus longue.<br />
Cette myopathie est transmise selon un mode récessif lié<br />
au chromosome X et affecte principalement les garçons.<br />
Néanmoins, des femmes conductrices peuvent être expressives<br />
et présenter des troubles cardiaques et musculaires, caractéristiques<br />
de la myopathie de Duchenne. Cette présence de<br />
manifestations phénotypiques caractéristiques mais modérées<br />
chez des femmes proviendrait d’un biais dans le phénomène<br />
d’inactivation d’un chromosome X. Le chromosome X inactivé<br />
serait préférentiellement le chromosome porteur de<br />
l’allèle normal chez les femmes symptomatiques alors que<br />
chez les femmes conductrices phénotypiquement indemnes,<br />
le phénomène d’inactivation survient de manière aléatoire.<br />
Ainsi, il existe autant de chromosomes X porteurs de l’allèle<br />
normal que de chromosomes X porteurs du gène muté qui<br />
soient inactivés chez ces femmes conductrices phénotypiquement<br />
indemnes.<br />
Le gène DMD codant la dystrophine, de la famille des<br />
spectrines, est localisé au niveau du bras court du chromosome<br />
X au niveau de la bande Xp21.2. Ce gène possède plusieurs<br />
promoteurs de lecture, chacun d’eux étant spécifique<br />
d’un tissu : muscle, cerveau… La dystrophine peut donc être<br />
retrouvée sous différentes isoformes, chacune étant spécifique<br />
d’un tissu particulier. Les mutations retrouvées sont principalement<br />
des délétions d’un ou plusieurs exons, mais aussi<br />
des mutations ponctuelles ou des duplications. La détection<br />
des grandes délétions peut être réalisée par PCR-multiplexes<br />
avec un taux de sensibilité satisfaisant ou par étude des polymorphismes,<br />
essentiellement des répétitions de séquences<br />
dinucléotidiques. La détection des mutations ponctuelles<br />
reste difficile. Les anomalies génétiques apparues de novo sont<br />
plus <strong>fr</strong>équentes que ne le voudraient les lois de la génétique<br />
chez ces patients. Cette <strong>fr</strong>équence anormale de mutations<br />
apparues de novo pourrait résulter soit d’un taux plus important<br />
de mutations masculines, soit de la présence d’une<br />
mosaïque germinale chez les femmes conductrices.<br />
La forme « musculaire » de la dystrophine se lie d’une part<br />
à l’actine et d’autre part à des protéines et à des glycoprotéines,<br />
l’ensemble formant le complexe dystrophine-glycoprotéine.<br />
Les anomalies génétiques sévères peuvent être<br />
responsables d’une absence ou d’un taux très faible de dystrophine,<br />
aboutissant à la formation d’un complexe altéré et à<br />
des anomalies structurelles du muscle, comme dans la myopathie<br />
de Duchenne. Les anomalies génétiques moins sévères<br />
sont compatibles avec la synthèse d’une dystrophine anormale,<br />
responsable d’un phénotype moins grave, la myopathie<br />
de Becker. Les altérations de la dystrophine et des complexes<br />
qu’elle forme dans le muscle sont responsables d’anomalies<br />
dans la concentration de calcium intracellulaire. L’absence<br />
d’atteinte des muscles oculomoteurs serait le témoin de leur<br />
aptitude à réguler leur concentration en calcium. Les isoformes<br />
Dp71 et Dp260 de la dystrophine s’expriment respectivement<br />
dans la membrane limitante interne et dans les cellules<br />
de Müller de la rétine. Les anomalies électrophysiologiques<br />
retrouvées au cours de la myopathie de Duchenne pourraient
Livre.book Page 417 Jeudi, 26. février 2009 3:40 15<br />
être la conséquence du rôle de protéine de structure et du rôle<br />
de protéine signal de la dystrophine Dp71 et des glycoprotéines<br />
associées à la dystrophine [50] . Une voie de recherche thérapeutique<br />
actuelle consiste à réguler par thérapie génique<br />
une protéine de structure, l’utrophine, dont l’action est voisine<br />
de celle de la dystrophine, qui est capable de diminuer les<br />
manifestations de cette myopathie chez l’animal.<br />
MYOTONIE DE STEINERT<br />
Le phénomène myotonique est caractéristique de cette affection<br />
transmise selon un mode dominant autosomique. Il réalise<br />
une lenteur à la décontraction musculaire associée à une<br />
faiblesse et à une fonte musculaire (fig. 27-18). Tous les muscles<br />
de l’organisme sont impliqués, tout particulièrement les<br />
muscles striés : mains, face, pharynx et muscles oculomoteurs.<br />
Une atteinte des muscles lisses est également possible<br />
aux niveaux digestif et cardiaque. La myotonie de Steinert<br />
débute entre 10 et 30 ans avec une aggravation lorsqu’elle est<br />
transmise par la mère aboutissant parfois à des formes néonatales.<br />
Les manifestations ophtalmologiques et neuro-ophtalmologiques<br />
sont nombreuses : survenue précoce d’une cataracte<br />
et troubles oculomoteurs in<strong>fr</strong>acliniques de nature myotonique<br />
[162] . La cataracte est précoce et peut prendre deux aspects<br />
différents. La cataracte de Vogt, la plus <strong>fr</strong>équente, associe des<br />
petites opacités punctiformes blanchâtres à des cristaux avec<br />
chatoiement polychrome du cortex antérieur et postérieur<br />
(fig. 27-19). La cataracte de Fleisher est caractérisée par des opa-<br />
Fig. 27-18 – La lenteur de décontraction des doigts est le témoin<br />
du phénomène myotonique chez un patient porteur d’une maladie<br />
de Steinert. Noter également l’existence d’un certain degré d’atrophie<br />
musculaire. (Collection de J.-L. Dufier.)<br />
Fig. 27-19 – Présence d’une cataracte de Vogt, caractérisée par<br />
l’existence de multiples opacités avec chatoiement polychrome, chez un<br />
patient porteur d’une maladie de Steinert. (Collection de J.-L. Dufier.)<br />
cités polaires postérieures (fig. 27-20). Il a été rapporté une<br />
hypotonie oculaire ainsi qu’une lenteur du jeu pupillaire<br />
secondaire au phénomène myotonique [10] . Au niveau oculomoteur,<br />
ce phénomène myotonique est responsable d’un ptosis<br />
souvent sévère, avec diminution de l’action du muscle<br />
releveur de la paupière supérieure, et d’une diminution de la<br />
vitesse maximale des saccades, corrélée au nombre de répétitions<br />
des triplets CTG au stade symptomatique [162] . L’atteinte<br />
oculomotrice est moins marquée lors de saccades répétitives<br />
par un mécanisme d’échauffement [222] . Enfin, il a été rapporté<br />
des anomalies maculaires réticulées évolutives, cliniques et<br />
électrophysiologiques, ainsi que des atrophies optiques<br />
bilatérales, parfois uniquement décelables en PEV (fig. 27-<br />
21) [75] .Une calvitie <strong>fr</strong>ontale, une azoospermie, une hypoacousie<br />
et un discret retard mental sont également observés lors<br />
de cette maladie (fig. 27-22).<br />
La myotonie de Steinert est liée à l’augmentation du nombre<br />
de triplets de nucléotides CTG dans le gène d’une protéine<br />
kinase spécifique localisée sur le chromosome 19 en<br />
19q13.2-q13.3 [181] . Le gène de la protéine kinase spécifique de<br />
la maladie de Steinert comporte quinze exons et code une<br />
protéine kinase avec un domaine catalytique et un domaine<br />
hydrophobe spécifique, de localisation cytoplasmique, qui<br />
s’exprime au niveau du muscle, du cœur et du cerveau [173] .<br />
Les allèles mutés comportent une augmentation au-delà de 50<br />
et, parfois, à plus de 2 000 répétitions de triplets nucléotidiques<br />
CTG situées dans la région 3’ non traduite (3’ UTR),<br />
alors que les individus normaux en comportent moins de 30.<br />
Cette affection est dominante autosomique mais il existe une<br />
aggravation, anciennement appelée phénomène d’« anticipation<br />
», par expansion allélique, lorsque la transmission est<br />
maternelle. La maladie apparaît d’autant plus tôt que le nombre<br />
d’allèles est important. Les mécanismes par lesquels cette<br />
augmentation du nombre de triplets non transcrits est responsable<br />
de la maladie de Steinert restent imparfaitement élucidés.<br />
La grande variabilité d’expression phénotypique et le<br />
phénomène d’« anticipation » rendent le conseil génétique<br />
Fig. 27-20 – Chez un autre patient atteint d’une maladie de Steinert,<br />
l’examen cristallinien met en évidence des opacités polaires postérieures<br />
en étoile caractéristiques de la cataracte de Fleischer.<br />
(Collection de J.-L. Dufier.)<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 417
Livre.book Page 418 Jeudi, 26. février 2009 3:40 15<br />
Fig. 27-21 – Opacités finement réticulées maculaires chez un patient<br />
porteur d’une maladie de Steinert. (Collection de J.-L. Dufier.)<br />
très délicat. Le diagnostic anténatal peut être réalisé sur biopsie<br />
de trophoblaste à la douzième semaine d’aménorrhée. Le<br />
diagnostic génétique préimplantatoire est une alternative au<br />
NYSTAGMUS CONGÉNITAL<br />
IDIOPATHIQUE<br />
Le nystagmus congénital idiopathique (NCI) est une anomalie<br />
de la statique oculaire caractérisée par la présence<br />
d’oscillations des globes, apparaissant dès la naissance ou au<br />
cours des trois premiers mois de la vie [1] . Ce NCI persiste<br />
tout au long de la vie et une intervention peut être nécessaire<br />
pour en réduire les conséquences sur la vision [81] . Tous les<br />
modes de transmission peuvent être observés [36, 134] . Néanmoins,<br />
aucune différence phénotypique n’a été retrouvée en<br />
fonction du mode de transmission.<br />
DÉFINITION ET SYMPTOMATOLOGIE<br />
Définition et diagnostic différentiel<br />
Le NCI est caractérisé par la survenue d’oscillations ou<br />
secousses involontaires des globes oculaires, incontrôlables,<br />
spontanées, bilatérales, conjuguées et synchrones. Celles-ci<br />
persistent habituellement à la fermeture des yeux mais peuvent<br />
diminuer de <strong>fr</strong>équence et d’intensité lors de tâches non<br />
visuelles. Un examen ophtalmologique et un bilan électrophysiologique<br />
sont indispensables afin d’éliminer un nystagmus<br />
symptomatique d’une affection sous-jacente [1] . Il en est<br />
de même des examens neuroradiologiques, toujours nécessai-<br />
418 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
Fig. 27-22 – L’existence d’une calvitie d’apparition précoce constitue<br />
une manifestation caractéristique de la maladie de Steinert.<br />
(Collection de J.-L. Dufier.)<br />
V – GÉNÉTIQUE DES MOUVEMENTS ANORMAUX<br />
diagnostic prénatal, admis mais de réalisation difficile. Pour<br />
cette raison, une thérapie prenant l’ARN pour cible pourrait<br />
être envisagée [74] .<br />
res pour éliminer une éventuelle atteinte du système nerveux<br />
central.<br />
Symptomatologie<br />
Il n’y a pas de différences phénotypiques du NCI en fonction<br />
du mode de transmission ou du gène altéré. Le bilan oculomotilographique<br />
est parfois utile pour en préciser les caractéristiques.<br />
Il est généralement congruent, d’amplitude<br />
identique sur les deux yeux. Sa direction est parfois verticale<br />
ou horizonto-rotatoire. Mais chez 95 % des patients, elle est<br />
horizontale. Rarement pendulaire, le NCI se présente avant<br />
tout comme un nystagmus à ressort. Les formes unidirectionnelles<br />
sont plus rares que les formes bidirectionnelles au cours<br />
desquelles le sens de la phase lente change avec la direction<br />
de regard. Deux zones d’inversion peuvent coexister chez un<br />
même patient. Dans la zone neutre ou zone d’inversion du<br />
nystagmus, celui-ci s’atténue ou disparaît, entraînant une<br />
amélioration de l’acuité visuelle que les patients cherchent à<br />
utiliser. Les secousses nystagmiques induisent un glissement<br />
continu des images devant la fovéa, perturbant la fonction<br />
visuelle. Une corrélation a été mise en évidence entre la diminution<br />
de l’acuité visuelle, la <strong>fr</strong>équence et l’amplitude des<br />
secousses nystagmiques et la durée des périodes de fovéation.<br />
Plus le temps de fovéation est augmenté, meilleure est l’acuité<br />
visuelle. Celle-ci est habituellement mieux préservée au cours<br />
du NCI qu’au cours des nystagmus sensoriels. Elle est habi-
Livre.book Page 419 Jeudi, 26. février 2009 3:40 15<br />
tuellement comprise entre 5/10 e et 10/10 e , avec une valeur<br />
moyenne chif<strong>fr</strong>ée à 8/10 e . L’acuité visuelle semble un peu plus<br />
basse dans les formes dominantes autosomiques que dans les<br />
formes liées au chromosome X [36, 109, 110] . Les patients ne perçoivent<br />
pas d’oscillopsies au cours du NCI, sauf s’il apparaît<br />
un nouveau trouble sensoriel tel qu’un strabisme.<br />
Le traitement des NCI repose sur la correction des troubles<br />
de la ré<strong>fr</strong>action déterminés sous cycloplégie atropinique au<br />
ré<strong>fr</strong>acteur automatique. Les lentilles de contact sont mieux<br />
adaptées à leur correction que les lunettes qui induisent des<br />
effets prismatiques lors des secousses nystagmiques. Néanmoins,<br />
des prismes peuvent être préconisés pour recentrer la<br />
zone neutre en position primaire lorsque cette dernière est<br />
peu excentrée, et réduire le torticolis. Le sommet des prismes<br />
doit être dirigé vers la zone neutre. Le Baclofen, qui inhibe la<br />
libération du glutamate, pourrait améliorer l’acuité<br />
visuelle [200] . En cas d’excentration importante de la zone neutre,<br />
celle-ci peut être déplacée chirurgicalement en position<br />
primaire à l’aide de résections et/ou raccourcissements des<br />
quatre muscles horizontaux. Une récession importante des<br />
quatre muscles droits horizontaux peut avoir un effet <strong>fr</strong>einateur<br />
sur l’intensité des secousses nystagmiques.<br />
FRÉQUENCE ET PHYSIOPATHOGÉNIE<br />
La <strong>fr</strong>équence du NCI est estimée à un pour 1 500 naissances<br />
[36] . Le mode de transmission dominant lié au chromosome<br />
X à pénétrance variable est vraisemblablement le plus<br />
<strong>fr</strong>équent [36] .<br />
Plusieurs hypothèses ont été proposées pour en expliquer<br />
la physiopathogénie. Le NCI serait dû à une anomalie de<br />
développement ou de maturation de la commande nerveuse<br />
du système de fixation, sans qu’il soit possible de mettre en<br />
évidence la moindre anomalie du système nerveux central.<br />
On invoque aussi une instabilité de l’intégrateur cérébral responsable<br />
de la stabilité du regard. Cependant, les mécanismes<br />
de fixation semblent être robustes puisque les réflexes de<br />
fixation sont de bonne qualité chez ces patients. De plus, la<br />
<strong>fr</strong>équence et l’intensité du NCI peuvent être accentuées par<br />
les efforts de fixation alors qu’elles diminuent lors de tâches<br />
non visuelles. C’est la raison pour laquelle il a été suggéré<br />
qu’il pourrait résulter d’une anomalie de connexion neuronale<br />
entre le système de fixation et les systèmes cérébraux de stabilisation<br />
oculaire. En fait, il n’a pas été possible d’établir une<br />
corrélation entre les caractéristiques électrophysiologiques de<br />
ce nystagmus congénital et un possible dysfonctionnement<br />
du système oculomoteur.<br />
GÉNÉTIQUE<br />
Modes de transmission<br />
Le NCI peut être transmis selon un mode récessif autosomique,<br />
dominant autosomique, dominant lié au chromosome X<br />
et récessif lié au chromosome X [36] . Dans les formes dominantes<br />
liées au chromosome X, la pénétrance du NCI est<br />
incomplète et varie de 29 à 54 % selon les études chez les<br />
femmes conductrices obligatoires [110] .<br />
Au moins quatre gènes pourraient être responsables du<br />
NCI : le gène NYS2, localisé en 6p12, un deuxième gène<br />
localisé sur le chromosome X au niveau du bras court en<br />
Xp11.4-p11.3, un troisième gène également localisé sur le<br />
chromosome X, mais au niveau de son bras long en Xq26-<br />
q27, et un quatrième gène qui serait localisé au niveau du<br />
bras court du chromosome 7 en 7p11 [36, 110, 113, 156] . Dans la littérature,<br />
le terme NYS1 est utilisé pour définir le gène<br />
Xp11.4-p11.3 ou le gène Xq26-q27 [36, 110] . Enfin, à ce jour,<br />
aucun gène responsable de la transmission récessive autosomique<br />
n’a été localisé.<br />
Les différents loci<br />
Grâce à une étude des polymorphismes de restriction de<br />
l’ensemble du génome, le gène NYS2 associé à la forme de<br />
transmission dominante autosomique a été localisé au niveau<br />
du bras court du chromosome 6, en 6p12 [109] . Aucun candidat<br />
n’y a été identifié.<br />
Une étude réalisée dans une famille comportant douze<br />
patients atteints et dix apparentés sains sur quatre générations<br />
a retrouvé une liaison génétique avec le chromosome X<br />
en Xp11.4. Les gènes de nombreuses pathologies ophtalmologiques<br />
liées au chromosome X sont également localisés au<br />
niveau de ce locus, en particulier celui de la cécité nocturne<br />
congénitale stationnaire (CSNB1), de la dystrophie des cônes<br />
(COD1), de l’atrophie optique liée au chromosome X (OPA2)<br />
et d’une forme de rétinopathie pigmentaire (RP2). On ne sait<br />
pas actuellement si le NCI est lié à une mutation spécifique<br />
au niveau de l’un de ces gènes, ou s’il possède son propre<br />
gène dans cette région du chromosome X.<br />
Un troisième gène du NCI a été retrouvé au locus Xq26q27<br />
dans différentes familles comportant des patients atteints<br />
sur plusieurs générations [110] . Ce gène est situé à proximité du<br />
gène de l’opsine des cônes aux moyennes et grandes longueurs<br />
d’onde [110] . Cette proximité entre les deux gènes explique<br />
probablement l’existence d’une deutéranomalie observée<br />
chez cinq patients et chez treize apparentés non atteints au<br />
sein de la même famille [134] . Plusieurs gènes candidats existent<br />
dont celui de la protéine SLC25A14, ou brain mitochondrial<br />
carrier protein-1. Il s’agit d’une protéine s’exprimant dans le<br />
cerveau et intervenant dans les phénomènes de découplage<br />
de la phosphorylation au sein des mitochondries. Un homologue<br />
de ce gène (UPC4) est situé au niveau du bras court du<br />
chromosome 6, à proximité du locus du gène du nystagmus<br />
congénital dominant (NYS2). Néanmoins, aucune mutation<br />
n’a pu être mise en évidence au niveau de ce gène chez quatre<br />
patients issus de quatre familles différentes liées au locus<br />
Xq26-q27 [109] . Aucune mutation des gènes CDR1 et SOX3 n’a<br />
non plus été retrouvée.<br />
Enfin, dans plusieurs familles, une liaison génétique au<br />
chromosome 6 a pu être exclue alors que des transmissions<br />
père-fils ont éliminé une transmission liée au chromosome X.<br />
C’est la raison pour laquelle l’existence d’un quatrième gène a<br />
été avancée [113, 156] . Dans une famille, une translocation équilibrée<br />
entre les chromosomes 7 et 15, t(7p11;15q11), a été<br />
identifiée, permettant d’incriminer l’un ou l’autre de ces chromosomes.<br />
L’analyse d’une autre famille a exclu une liaison<br />
génétique avec les loci 6p12 et 15q11 ; en revanche, elle a<br />
confirmé l’existence d’une liaison avec le bras court du chromosome<br />
7, en 7p11 [113] .<br />
NYSTAGMUS SYMPTOMATIQUES<br />
ET NON CONGÉNITAUX<br />
Le nystagmus congénital idiopathique doit être distingué du<br />
nystagmus congénital d’origine sensorielle dont le mode de<br />
présentation est identique [1] . Ce dernier est associé à une<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 419
Livre.book Page 420 Jeudi, 26. février 2009 3:40 15<br />
déficience visuelle, elle-même volontiers d’origine génétique,<br />
qu’il s’agisse de cataracte congénitale, d’aniridie avec hypoplasie<br />
maculaire, des différentes formes d’albinisme, de dystrophies<br />
rétiniennes précoces, comme l’amaurose congénitale<br />
de Leber, de cécité nocturne congénitale stationnaire dans sa<br />
forme liée au chromosome X, d’achromatopsie congénitale<br />
ou de monochromatisme aux cônes bleus, d’atrophie optique<br />
récessive ou de malformations papillaires, colobome ou<br />
hypoplasie [1] . Il faut également éliminer une atteinte du système<br />
nerveux central, quelle qu’en soit l’origine et qui peut se<br />
manifester par un nystagmus pouvant en imposer pour un<br />
nystagmus congénital idiopathique.<br />
Il faut évoquer à part le nystagmus dit « précoce », apparaissant<br />
dans l’enfance et qui est secondaire à des anomalies<br />
cérébelleuses, probablement au niveau du floculus. Ce nystagmus<br />
est volontiers associé à un strabisme. Il est transmis<br />
selon le mode dominant autosomique et est lié au chromosome<br />
13 [179] . Le gène responsable, dénommé NYS4, est localisé<br />
sur le bras long du chromosome 13, en 13q31-q33.<br />
MALADIE DE PELIZAEUS-MERZBACHER<br />
Depuis sa description en 1885, trois formes de la maladie de<br />
Pelizaeus-Merzbacher (MPM) dont la transmission est récessive<br />
liée au chromosome X [184] ont été identifiées.<br />
La forme I correspond à la forme la plus classique de cette<br />
affection, débutant dans la prime enfance par l’apparition<br />
d’un nystagmus particulier et d’un syndrome extrapyramidal.<br />
Chez ces enfants, on observe un nystagmus pendulaire ellipsoïdal<br />
associé à un nystagmus battant vers le haut et à un<br />
dodelinement de la tête pouvant évoquer un spasmus nutans.<br />
Il apparaît une perte des acquisitions aboutissant à un retard<br />
mental, une ataxie et des signes cérébelleux, des mouvements<br />
choréo-athétosiques et une spasticité. Tardivement, le nystagmus<br />
peut s’atténuer ou disparaître alors qu’apparaît une<br />
atrophie optique. Le décès survient à l’adolescence. La<br />
deuxième forme est caractérisée par un début très précoce et<br />
une évolution rapide aboutissant au décès dans l’enfance. La<br />
troisième forme présente une évolution intermédiaire.<br />
Le bilan IRM montre des anomalies de la myélinisation<br />
sans anomalie de la substance blanche. Ce bilan est intéressant<br />
pour la détection des femmes conductrices chez lesquelles<br />
il met en évidence des hypersignaux de la substance<br />
blanche périventriculaire [20] . Quelques rares cas de femmes<br />
symptomatiques ont été rapportés.<br />
Le gène responsable de cette affection a été localisé en<br />
Xq22. Ce gène de sept exons code une protéine très conservée<br />
entre les espèces, dénommée protéolipide protéine (PLP),<br />
un constituant de la myéline dont il existe deux isoformes<br />
(PLP1 et DM20). C’est la raison pour laquelle la myélinisation<br />
est anormale. Les mutations ou autres anomalies de ce gène<br />
peuvent être responsables d’un autre syndrome, la paraplégie<br />
spastique liée au chromosome X. De multiples anomalies<br />
génétiques ou chromosomiques ont été retrouvées chez des<br />
patients porteurs de MPM au niveau de ce gène. Plusieurs<br />
mutations ponctuelles ont été décrites, mais l’anomalie la<br />
plus <strong>fr</strong>équente, retrouvée chez 60 à 70 % des enfants, est la<br />
duplication du gène PLP, survenant souvent à la suite d’une<br />
translocation. L’existence d’une délétion ne serait pas viable<br />
sauf lorsqu’elle est de petite taille [99] . Il est admis que les<br />
mutations sont responsables des formes les plus sévères de<br />
MPM alors que les duplications du gène PLP ne donnent que<br />
des formes classiques ou modérées.<br />
420 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
La transmission est récessive liée au chromosome X. Le<br />
taux de mutations retrouvé chez les mères est conforme à ce<br />
qui est attendu dans ce mode de transmission. Mais, dans<br />
plus de 90 % des cas, les mères sont conductrices de la duplication.<br />
Ces anomalies géniques surviennent entre la génération<br />
maternelle et grand-parentale avec un biais masculin [138] .<br />
Elles proviennent dans la majorité des cas des cellules germinales<br />
du grand-père maternel de l’enfant.<br />
Certains patients présentent un tableau clinique identique<br />
à celui de la MPM, mais dont la transmission est récessive<br />
autosomique. Cette variante de la MPM est due à la présence<br />
de mutations dans le gène GJA12, situé en 1q41-q42 et<br />
codant une connexine (connexine 46.2) [216] . Cette protéine<br />
retrouvée au niveau des gap-junctions, s’exprime particulièrement<br />
au niveau des oligodendrocytes. Une autre variante de<br />
la MPM serait transmise selon un mode récessif lié au chromosome<br />
X, mais ne serait pas causée par des mutations dans<br />
le gène de la PLP.<br />
MALADIE D’ALEXANDER<br />
La maladie d’Alexander est une maladie rare, secondaire à<br />
une anomalie astrocytaire plutôt qu’à une leucodystrophie. Il<br />
en existe trois formes, infantile, juvénile et adulte, selon l’âge<br />
de début, caractérisées par des troubles neurologiques et<br />
neuro-ophtalmologiques.<br />
La forme infantile qui débute dès la première année associe<br />
des manifestations neuro-ophtalmologiques à type d’atrophie<br />
optique à un retard psychomoteur, des crises comitiales,<br />
une hydrocéphalie et une macrocéphalie [126] . Le décès survient<br />
en quelques mois. Dans les formes juvénile et adulte,<br />
d’évolution plus lente et sans déficit intellectuel, les manifestations<br />
neuro-ophtalmologiques s’intègrent dans le cadre de<br />
dysfonctionnements bulbaires et pseudobulbaires : nystagmus<br />
à ressort et nystagmus parétique, anomalie des mouvements<br />
de poursuite et du nystagmus optocinétique, ptosis et<br />
ondes carrées en électromotilographie [126] . On observe par<br />
ailleurs une paralysie faciale et une atrophie linguale. Le diagnostic<br />
de maladie d’Alexander — qui reposait sur la mise en<br />
évidence de lésions de démyélinisation et de fibres de Rosenthal<br />
dans les astrocytes sur des pièces de biopsie cérébrale —<br />
peut être affirmé en IRM devant la présence d’au moins quatre<br />
des cinq signes suivants : anomalies de la substance blanche<br />
à prédominance <strong>fr</strong>ontale, présence d’hypersignaux<br />
périventriculaires en T1 et d’hyposignaux en T2, anomalie de<br />
signal des ganglions de la base, anomalie de signal du tronc<br />
cérébral et anomalie du contraste entre les structures blanches<br />
et grises. Le LCR met en évidence une augmentation des βcristallines.<br />
Les fibres de Rosenthal renferment une grande<br />
quantité de protéine fibrillaire gliale acide (PFGA), d’origine<br />
astrocytaire [101] . Cette protéine entre dans la constitution de<br />
filaments astrocytaires intracytoplasmiques et intervient dans<br />
les phénomènes de myélinisation. Les patients atteints présentent<br />
à l’état hétérozygote l’une des mutations dans le gène<br />
(17q21) codant cette protéine, mais généralement apparues de<br />
novo. Néanmoins, une transmission récessive ou dominante<br />
autosomique avec mosaïque germinale est évoquée dans certaines<br />
formes familiales. Un diagnostic prénatal, reposant sur<br />
la recherche de mutations dans le gène de cette protéine, peut<br />
être proposé à chaque nouvelle grossesse dans les familles de<br />
patients atteints. Il semble que ces mutations soient responsables,<br />
par gain de fonction, de l’accumulation de PFGA non<br />
intégrées dans les filaments astrocytaires du cytoplasme et<br />
auraient, de ce fait, un effet toxique.
Livre.book Page 421 Jeudi, 26. février 2009 3:40 15<br />
VI – GÉNÉTIQUE DES ANOMALIES DU SYSTÈME NERVEUX<br />
GANGLIOSIDOSES<br />
Cet ensemble de maladies métaboliques entre dans le cadre<br />
des sphingolipidoses. Selon le déficit enzymatique, l’accumulation<br />
concerne soit la forme GM1 du ganglioside (gangliosidose<br />
GM1), soit la forme GM2 (gangliosidose GM2). Les<br />
gangliosidoses GM1 sont causées par un déficit en gangliosido-β-galactosidase.<br />
Les gangliosidoses GM2 sont secondaires<br />
à un déficit en β-hexosaminidase, enzyme dimérique<br />
existant sous trois formes. La forme A est constituée d’une<br />
sous-unité α et d’une sous-unité β alors que la forme B est<br />
composée de deux sous-unités β [170] . La forme S correspond à<br />
l’homodimère composé de deux sous-unités α. Il existe plusieurs<br />
types de gangliosidoses, en fonction du gène muté et<br />
de l’activité résiduelle de l’enzyme, ce qui conditionne l’âge<br />
d’apparition de la symptomatologie.<br />
GANGLIOSIDOSES GM2<br />
Maladie de Tay-Sachs<br />
La maladie de Tay-Sachs est une gangliosidose GM2 de<br />
type 1, transmise selon un mode récessif autosomique. Cette<br />
maladie métabolique rare aboutit à l’accumulation de ganglioside<br />
GM2 au niveau des neurones, qui prennent un aspect<br />
ballonisé lors des études histologiques post mortem. Cliniquement,<br />
cette accumulation aboutit à des manifestations neurologiques<br />
d’apparition très précoce, vers l’âge de deux ou trois<br />
mois, avec une perte des acquisitions. La survenue d’une<br />
réaction anormale aux bruits sous forme de sursauts excessifs<br />
en extension — les clonies audiogènes —, est très caractéristique<br />
et est observée dès le stade initial de la maladie. Il s’y<br />
associe un syndrome pyramidal bilatéral, des convulsions et<br />
un tableau de démence. Le décès survient vers l’âge de trois<br />
ou quatre ans en moyenne [231] . Les manifestations ophtalmologiques<br />
et neuro-ophtalmologiques sont constantes, aboutissant<br />
précocement à la cécité (fig. 27-23). L’accumulation du<br />
ganglioside GM2 blanchâtre au niveau des cellules ganglionnaires<br />
permet d’expliquer la teinte anormalement blanc grisâ-<br />
Fig. 27-23 – Enfant porteur d’une maladie de Tay-Sachs, responsable de<br />
cécité. (Collection de J.-L. Dufier.)<br />
tre de la région périfovéolaire qui tranche avec la coloration<br />
normale rouge sombre de la région fovéolaire (fig. 27-24).<br />
Cette région, dépourvue de cellules ganglionnaires, garde sa<br />
coloration normale, donnant l’aspect de tache rouge cerise.<br />
L’angiographie est le plus souvent normale, de même que<br />
l’ERG. Enfin, ces enfants développent une atrophie optique.<br />
Les études en IRM ont retrouvé la présence d’anomalies de<br />
signal au niveau des noyaux gris centraux dès les premiers<br />
stades de la maladie. À un stade avancé, il est en outre<br />
observé une atrophie corticale importante associée à des anomalies<br />
de signal de la substance blanche [144] .<br />
La maladie de Tay-Sachs est due à un déficit en sousunité<br />
α de la β-hexosaminidase A, enzyme lysosomale. Seule<br />
cette forme hétérodimérique A, associée à un activateur<br />
GM2, possède la capacité de dégrader le GM2 [231] . Ce déficit<br />
est la conséquence de la présence de différentes mutations<br />
dans le gène de la sous-unité α de la β-hexosaminidase A [164] .<br />
Ce gène de quatorze exons est localisé sur le chromosome 15,<br />
en 15q23-q24. Plus de 80 mutations ont été rapportées, tant<br />
au niveau des exons que des introns, et sont responsables<br />
d’une perte plus ou moins importante de l’activité de la sousunité<br />
α de la β-hexosaminidase A. Les mutations associées à<br />
la maladie de Tay-Sachs entraînent une absence presque<br />
totale de l’activité de la sous-unité α de cette enzyme. Par<br />
ailleurs, plusieurs de ces mutations sont plus volontiers<br />
retrouvées dans la population ashkénaze polonaise, au sein<br />
de laquelle cette maladie est particulièrement <strong>fr</strong>équente du<br />
fait du fort taux de consanguinité.<br />
Il est possible de mesurer l’activité de la β-hexosaminidase<br />
A vis-à-vis de différents substrats (4-méthylumbelliféryl-β-D-<br />
N-acétylglucosamine, ou 4MUG, et 4-méthylumbelliferyl-β-<br />
D-N-acétylglucosamine-6-SO4, ou 4MUGS) à partir du sang.<br />
Mais il est également possible de pratiquer une recherche de<br />
Fig. 27-24 – Chez le même patient qu’à la figure 27-23, l’accumulation<br />
du ganglioside GM2 au niveau des cellules ganglionnaires est<br />
responsable de la teinte blanchâtre de la rétine, hormis au niveau<br />
fovéolaire. La fovéa, dépourvue de cellules ganglionnaires, a pris, par<br />
contraste un aspect de tache rouge cerise. (Collection de J.-L. Dufier.)<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 421
Livre.book Page 422 Jeudi, 26. février 2009 3:40 15<br />
mutations, en particulier lors de dépistages prénataux, lorsque<br />
l’anomalie génétique s’accompagne de la préservation d’une<br />
certaine activité enzymatique.<br />
Variants de la maladie de Tay-Sachs<br />
Il faut citer le variant B1 de la maladie de Tay-Sachs, dont les<br />
manifestations cliniques sont peu différentes de la forme classique.<br />
L’activité de la β-hexosaminidase A est normale lors<br />
des tests usuels vis-à-vis de substrats neutres (4MUG) alors<br />
qu’elle est effondrée vis-à-vis de son substrat naturel ou d’un<br />
substrat chargé négativement (4MUGS) [32] . Les mutations<br />
modifieraient des acides aminés situés près du site de liaison<br />
de la sous-unité α à son substrat, gênant ainsi la fixation du<br />
substrat ou son hydrolyse.<br />
Le variant AB de la maladie de Tay-Sachs correspond à<br />
une déficience du gène de l’activateur GM2, dont le gène est<br />
situé sur le bras long du chromosome 5. La présentation clinique<br />
de cette forme est identique à celle de la maladie de Tay-<br />
Sachs, tant au point de vue de l’âge de début qu’en ce qui<br />
concerne les manifestations neurologiques, dont les clonies<br />
audiogènes, qu’ophtalmologiques avec présence d’une tache<br />
rouge cerise. L’activité de la β-hexosaminidase A et de la βhexosaminidase<br />
B est normale.<br />
Autres gangliosidoses GM2<br />
La forme juvénile de la gangliosidose GM2, dite de type 3,<br />
diffère de la maladie de Tay-Sachs par un âge d’apparition<br />
plus tardif. Les premières manifestations neurologiques à<br />
type d’ataxie cérébelleuse apparaissent après l’âge de 3 ans.<br />
L’évolution se fait vers une régression des acquisitions et un<br />
tableau de démence. Les manifestations ophtalmologiques, à<br />
type d’atrophie optique ou de tache rouge cerise sont inconstantes<br />
et tardives. Il en est de même de la cécité qui est tardive.<br />
Le décès, parfois retardé au-delà de l’âge de 25 ans,<br />
survient le plus souvent vers l’âge de 15 ans. Il n’existe pas de<br />
véritable <strong>fr</strong>ontière entre cette forme et celle de l’adulte dont<br />
l’âge d’apparition est plus tardif et dont l’évolution est plus<br />
lente.<br />
Les manifestations neurologiques de la forme de l’adulte<br />
de la gangliosidose GM2 peuvent en imposer pour une atrophie<br />
spinale puisque cette affection associe de façon variée<br />
une ataxie cérébelleuse, des troubles de l’équilibre et des déficits<br />
musculaires proximaux avec fasciculation, anomalies de<br />
l’EMG et des CPK. En revanche, les troubles intellectuels<br />
seraient moins marqués que dans la forme juvénile [102] . Enfin,<br />
il est rapporté des troubles oculomoteurs à type d’ataxie,<br />
d’ophtalmoplégie internucléaire ou de paralysie supranucléaire<br />
[97] . En revanche, il n’existe ni cécité ni surcharge rétinienne.<br />
Enfin, la surcharge en ganglioside peut concerner<br />
d’autres tissus, comme en témoignent certaines descriptions<br />
de biopsies de tissus digestifs [102] .<br />
Les formes juvénile et de l’adulte de gangliosidose GM2<br />
sont l’une et l’autre secondaires à la présence de mutations<br />
dans le gène de la sous-unité α de la β-hexosaminidase A. Les<br />
mutations retrouvées chez les patients ne sont responsables<br />
que d’un déficit enzymatique partiel. Plus ce déficit est important,<br />
plus les manifestations cliniques débutent précocement.<br />
Maladie de Sandhoff<br />
Cette gangliosidose GM2, encore dénommée variant 0, peut<br />
également être considérée comme une cérébrosidose. Elle<br />
422 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
existe sous plusieurs formes selon son âge d’apparition. Le<br />
type 1 de la maladie de Sandhoff est cliniquement peu différent<br />
de la maladie de Tay-Sachs. En effet, elle débute au<br />
cours de la première année de vie et associe des troubles neurologiques<br />
à type de déficit moteur progressif, de crises<br />
convulsives, de détérioration mentale et de surdité, à des<br />
troubles ophtalmologiques. La cécité est en effet constante au<br />
cours de l’évolution de la maladie de Sandhoff et le fond<br />
d’œil montre une tache rouge cerise maculaire chez ces<br />
patients. Le décès survient entre 2 et 3 ans.<br />
Ce tableau neurodégénératif est secondaire à une surcharge<br />
neuronale en globosides et en ganglioside GM2 du fait d’un<br />
déficit en β-hexosaminidase A (hétérodimère comportant une<br />
sous-unité α et β) et β-hexosaminidase B (homodimère comportant<br />
deux sous-unités β). En effet, les mutations responsables<br />
de cette affection concernent le gène de la sous-unité β de<br />
la β-hexosaminidase, localisé sur le chromosome 5, en 5q13.<br />
Cette affection n’est pas l’apanage de la population ashkénaze.<br />
Il existe également une forme juvénile (type 2) dont l’âge<br />
d’apparition est plus tardif, entre 3 et 11 ans ; elle est compatible<br />
avec une survie plus longue, jusqu’à l’âge adulte [154] . Les<br />
manifestations cliniques sont principalement neurologiques, à<br />
type d’ataxie cérébelleuse, de déficit musculaire proximal<br />
progressif et de détérioration mentale. Les manifestations ophtalmologiques,<br />
en particulier la tache rouge cerise, sont inconstamment<br />
rapportées. Enfin, la forme adulte revêt surtout la<br />
forme d’un déficit moteur évoquant une atteinte de la corne<br />
antérieure de la moelle. Il n’existe ni détérioration ni cécité. Ces<br />
deux formes de la maladie de Sandhoff sont dues à la présence<br />
de mutations dans le gène de la sous-unité β de la β-hexosaminidase,<br />
différentes de celles observées lors de la forme infantile.<br />
GANGLIOSIDOSES GM1<br />
La gangliosidose GM1, ou gangliosidose généralisée, est une<br />
maladie métabolique transmise selon un mode récessif autosomique<br />
qui existe sous trois formes (types 1, 2 et 3).<br />
Cette pathologie est due à un déficit en gangliosido-β-galactosidase<br />
et aboutit à une accumulation précoce de gangliosides<br />
GM1 dans de nombreux tissus de l’organisme : tissu nerveux,<br />
cardiaque, hépatique, splénique et rénal. C’est la raison pour<br />
laquelle les premières manifestations de cette affection apparaissent<br />
dès les premières semaines de vie. Les patients atteints<br />
développent des troubles neurologiques à type d’hypotonie et<br />
de détérioration mentale, d’hépatosplénomégalie et d’insuffisance<br />
rénale. La présence d’une tache rouge cerise au niveau de<br />
la macula est présente chez tous les patients selon Giugliani [78] .<br />
Enfin, on reconnaît ces patients par leur faciès en gargouille<br />
évocateur de maladie de Hurler et des anomalies cutanées à<br />
type d’angiokératomes ou de mélanocytoses cutanée [89] . Le<br />
décès survient avant la troisième année de vie dans cette forme<br />
infantile (GM1 de type 1). Celle-ci est liée à un déficit des trois<br />
isoformes A, B et C de la gangliosido-β-galactosidase qui clive<br />
une molécule de galactose du GM1. De nombreuses mutations<br />
du gène de cette enzyme, localisée sur le chromosome 3, en<br />
3p21.33, ont été rapportées.<br />
Il n’existe aucune manifestation viscérale au cours de la<br />
forme juvénile de la GM1 (ou GM1 de type 2) dont les premières<br />
manifestations neurologiques n’apparaissent que vers<br />
l’âge de 2 ans et sont d’évolution très progressive. La dégradation<br />
neurologique aboutit au décès vers l’âge de 10 ou 15 ans.<br />
Le déficit enzymatique ne porte que sur les isoformes B et C<br />
de la gangliosido-β-galactosidase. La GM1 de type 3, ou
Livre.book Page 423 Jeudi, 26. février 2009 3:40 15<br />
forme adulte de la GM1, débute tardivement, entre 10 et<br />
20 ans et est d’évolution prolongée. Les patients porteurs de<br />
cette forme de GM1 présentent des manifestations neurologiques<br />
à type d’ataxie cérébelleuse, de mouvements anormaux<br />
et de détérioration mentale, et des anomalies cutanées. Une<br />
baisse d’acuité visuelle peut être observée. En revanche, la<br />
rétine est indemne de toute lésion de surcharge.<br />
SYNDROME D’AICARDI<br />
Décrit en 1969 par Aicardi, ce syndrome, transmis selon un<br />
mode dominant lié au chromosome X, est léthal chez le garçon.<br />
Il n’est observé que chez les filles. Hopkins a rapporté le<br />
seul cas masculin chez un garçon qui avait deux chromosomes<br />
X du fait d’un syndrome de Klinefelter associé.<br />
Les principales manifestations du syndrome d’Aicardi sont<br />
neurologiques. Chez les filles atteintes, une comitialité à type<br />
de spasmes en flexion apparaît dans les premières semaines de<br />
vie, associée à un retard psychomoteur dont l’importance est<br />
extrêmement variable. L’acquisition du langage et de la marche<br />
est souvent impossible. Il existe une corrélation entre le<br />
niveau de contrôle de la comitialité et la profondeur du retard<br />
psychomoteur. Des tumeurs cérébrales, principalement des<br />
papillomes des plexus choroïdes, ont été rapportées, parfois<br />
associées à des tumeurs bénignes ou malignes extracérébrales<br />
[212] . Plus d’un tiers des patients sont également porteurs<br />
d’anomalies vertébrales ou costales. Les lacunes<br />
choriorétiniennes arrondies « à l’emporte-pièce », pseudotoxoplasmiques,<br />
surtout lorsqu’elles sont localisées dans la région<br />
péripapillaire, constituent une manifestation ophtalmologique<br />
quasi pathognomonique (fig. 27-25). L’EEG retrouve des anomalies<br />
comitiales multifocales et asynchrones entre les deux<br />
hémisphères survenant par bouffées (hypsarythmie). Les examens<br />
neuroradiologiques retrouvent l’agénésie du corps calleux<br />
complète chez 72 % des enfants, ou simplement partielle,<br />
qui constitue l’un des signes cardinaux de ce syndrome<br />
Fig. 27-25 – Présence de plusieurs lacunes choriorétiniennes « à<br />
l’emporte-pièce » péripapillaires chez une fille porteuse d’un syndrome<br />
d’Aicardi. Ces lacunes d’allure pseudotoxoplasmiques sont très<br />
caractéristiques de ce syndrome. (Collection de J.-L. Dufier.)<br />
(fig. 27-26). Ils mettent également en évidence des anomalies<br />
de la gyration, des dilatations ventriculaires, des malformations<br />
de Dandy-Walker, des kystes arachnoïdiens [174] .<br />
La mise en évidence d’anomalies chromosomiques, en particulier<br />
de translocations affectant la région 22 du bras court<br />
du chromosome X, a permis de localiser le gène responsable<br />
du syndrome d’Aicardi. Toutes les filles atteintes de ce syndrome<br />
sont porteuses d’une mutation apparue de novo. La<br />
présence d’une mutation dans la région p22 du chromosome<br />
X est responsable des avortements du premier trimestre<br />
chez le garçon. L’inactivation d’un chromosome X surviendrait<br />
de manière aléatoire et ne toucherait pas de manière<br />
préférentielle le chromosome X muté. Cette inactivation aléatoire<br />
est paradoxale compte tenu du mode de transmission.<br />
Hoag a proposé plusieurs hypothèses pour expliquer cette<br />
discordance. Le produit du gène muté pourrait être léthal<br />
chez les garçons et responsable du syndrome d’Aicardi chez<br />
les filles hétérozygotes. Une autre hypothèse serait que la<br />
mutation pourrait entraîner une anomalie d’inactivation du<br />
chromosome X, en particulier dans cette région Xp22. En<br />
effet, l’absence d’inactivation des gènes situés en Xp22 sur<br />
l’un des deux chromosomes X a déjà été rapportée et n’est<br />
pas léthale, mais responsable de troubles mentaux et physiques<br />
sévères par surexpression des gènes. Dans un tel cas,<br />
seules les filles sont atteintes [94] , tous les garçons étant phénotypiquement<br />
sains.<br />
DYSAUTONOMIE FAMILIALE<br />
DE RILEY-DAY<br />
Riley a décrit en 1949 une alacrymie congénitale de cause<br />
inconnue. Elle n’a été rattachée à une anomalie du système<br />
nerveux autonome que plusieurs années plus tard, ce qui a justifié<br />
le terme de dysautonomie familiale. Cette dysautonomie<br />
transmise selon un mode récessif autosomique est presque<br />
exclusivement retrouvée chez des patients d’origine ashkénaze<br />
[161] . Elle est due à la présence de mutations dans le gène<br />
IKBKAP qui code une protéine associée à un complexe kinase.<br />
Fig. 27-26 – Chez la même patiente qu’à la figure 27-25, le scanner<br />
cérébral permet de confirmer l’agénésie du corps calleux.<br />
(Collection de J.-L. Dufier.)<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 423
Livre.book Page 424 Jeudi, 26. février 2009 3:40 15<br />
CLINIQUE<br />
La dysautonomie familiale de Riley-Day entre dans le cadre<br />
des neuropathies héréditaires sensitives et dysautonomiques<br />
dont il existe cinq formes. Elle est encore dénommée HSAN3.<br />
Elle aboutit à la dégénérescence sélective des nerfs sensitifs et<br />
du système nerveux autonome (SNA). Elle se manifeste donc<br />
par des manifestations générales traduisant l’absence de régulation<br />
du SNA : troubles du rythme cardiaque, poussées<br />
d’hypertension artérielle paroxystique, d’hypotension orthostatique,<br />
troubles de la microcirculation, pouvant évoquer un<br />
syndrome de Raynaud, et bouffées érythémateuses du<br />
visage [210] . L’aréflexie tendineuse doit être rattachée à la neuropathie<br />
sensorielle. Chez ces patients, une labilité émotionnelle<br />
témoigne également du dysfonctionnement cérébral.<br />
L’atteinte ophtalmologique est marquée par une absence de<br />
sécrétion lacrymale, résultant du dysfonctionnement du SNA,<br />
et par une anesthésie cornéenne secondaire à la dégénérescence<br />
des nerfs sensitifs (fig. 27-27). Des neuropathies optiques<br />
d’apparition tardive ont été rapportées [210] . Il a également<br />
été décrit une perte des papilles linguales responsable de troubles<br />
du goût et une cypho-scoliose sévère pouvant nécessiter<br />
une prise en charge chirurgicale [210] . L’instillation conjonctivale<br />
de chlorydrate de métacholine, provoquant un myosis, et<br />
l’injection sous-cutanée d’histamine n’entraînant aucune réaction<br />
cutanée, constituent deux tests pharmacologiques décisifs<br />
pour le diagnostic. Le décès survient généralement brutalement<br />
chez des adultes jeunes du fait d’accidents cardiovasculaires<br />
ou de complications bronchopulmonaires liées aux<br />
troubles de la déglutition. Les progrès thérapeutiques et de la<br />
chirurgie permettent d’améliorer la survie.<br />
Fig. 27-27 – Dysautonomie de Riley-Day. (Collection de J.-L. Dufier.)<br />
GÉNÉTIQUE<br />
L’origine ashkénaze fait partie des critères diagnostiques de la<br />
dysautonomie familiale de Riley-Day, du fait de l’effet fondateur<br />
d’une mutation au sein de cette population. Néanmoins,<br />
cette affection peut s’observer en dehors de ce contexte ethnique<br />
[117] . Blumenfeld a localisé le gène de cette affection au<br />
niveau du bras long du chromosome 9. Les études ultérieures<br />
réalisées à l’aide de marqueurs et d’analyses de polymorphisme<br />
ont permis d’affiner la localisation du gène situé dans<br />
la bande 9q31 [26] . Un haplotype retrouvé sur plus de 98,5 %<br />
des chromosomes de patients atteints a été identifié dans cette<br />
région. La méthode du gène candidat appliquée aux différents<br />
gènes présents dans cette région a permis de retrouver deux<br />
424 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
mutations dans le gène IKBKAP chez des patients porteurs<br />
d’une dysautonomie familiale de Riley-Day [198] . Plus de 99 %<br />
des allèles mutés portent la même mutation [198] . Celle-ci est<br />
située dans l’intron 20 et aboutit, par anomalie d’épissage, à la<br />
synthèse d’une protéine anormale au niveau du système nerveux<br />
central. La seconde mutation, dans l’exon 19, altère le site<br />
de phosphorylation de la protéine. Les mécanismes physiopathologiques<br />
par lesquels les mutations aboutissent à la dégénérescence<br />
nerveuse sont encore mal connus. Un diagnostic<br />
prénatal est possible dans les familles à risque [68, 155] .<br />
ANOMALIES CONGÉNITALES<br />
DE LA PAPILLE OPTIQUE<br />
Les anomalies congénitales de la papille apparaissent généralement<br />
sporadiques. Une cause accidentelle, infectieuse ou<br />
toxique est d’ailleurs <strong>fr</strong>équemment invoquée. Néanmoins, il a<br />
été rapporté des formes génétiques de malformation papillaire,<br />
quelle qu’en soit la présentation clinique, ce qui souligne<br />
la nécessité d’examiner systématiquement les deux<br />
parents et la <strong>fr</strong>atrie à la recherche d’anomalies minimes de la<br />
papille (cf. chapitre 4).<br />
Les colobomes papillaires sont des anomalies généralement<br />
bilatérales mais pouvant être asymétriques. Lorsqu’ils<br />
ont une composante héréditaire, les colobomes des nerfs<br />
optiques sont transmis selon un mode dominant autosomique<br />
et sont dus à des mutations dans deux gènes de la famille<br />
PAX (cf. chapitres 5 et 6). Les mutations du gène PAX2, localisé<br />
sur le chromosome 10 à la limite des bandes q24.3 et<br />
q25.1 (10q24.3-q25.1), sont responsables du syndrome oculorénal<br />
associant, outre le colobome papillaire, une insuffisance<br />
rénale progressive aboutissant à la mise en dialyse [12, 48] . Des<br />
mutations du gène PAX6 ont également été retrouvées chez<br />
des patients porteurs de colobomes papillaires et choriorétiniens,<br />
de papilles « en fleur de liseron » (morming glory syndrome)<br />
et même d’hypoplasie des nerfs optiques ou d’aplasie<br />
des nerfs optiques [15] . La papille en « fleur de liseron » est<br />
généralement unilatérale mais peut s’associer à un autre type<br />
d’anomalie papillaire sur l’œil controlatéral. Elle résulterait<br />
d’un défaut de maturation de la sclère dans sa portion postérieure<br />
et de la partie adjacente des gaines du nerf optique,<br />
mais sa pathogénie reste controversée. L’aplasie du nerf optique<br />
est volontiers unilatérale. La papille apparaît alors<br />
absente ou pâle ou encore excavée, suggérant fortement une<br />
involution du nerf optique. L’absence de vascularisation rétinienne<br />
d’une part et l’absence de tout nerf optique au sein de<br />
l’orbite en IRM d’autre part confirment le diagnostic. Il est<br />
rare que l’hypoplasie des nerfs optiques, — habituellement<br />
bilatérale puisque l’atteinte unilatérale n’est notée que dans<br />
7 % des cas — reste isolée sans qu’aucune anomalie cérébrale<br />
ne puisse être mise en évidence. En effet, elle peut s’intégrer<br />
dans le cadre du syndrome de De Morsier, dont l’origine<br />
génétique est maintenant bien établie [59] . Sa présentation très<br />
caractéristique sera abordée plus loin. L’implication du gène<br />
PAX6 dans ces différentes anomalies papillaires est expliquée<br />
par le rôle important que celui-ci joue durant la vie embryonnaire.<br />
En effet, il s’exprime au niveau du système nerveux, de<br />
la cupule optique et des cellules ganglionnaires, et participe à<br />
la mise en place de ces différents éléments.<br />
Si des anomalies cérébrales, en particulier de la ligne<br />
médiane, sont <strong>fr</strong>équemment rapportées chez des patients porteurs<br />
d’anomalies congénitales de la papille, celles-ci ne sont pas<br />
constantes, à moins qu’elles ne dépassent les moyens actuels
Livre.book Page 425 Jeudi, 26. février 2009 3:40 15<br />
d’investigation. Quoi qu’il en soit, elles doivent être systématiquement<br />
recherchées par un bilan neuro-radiologique (échographie<br />
trans-fontanellaire, scanner, IRM cérébrale) et endocrinien.<br />
SYNDROME DE DE MORSIER,<br />
OU DYSPLASIE SEPTO-OPTIQUE<br />
ASPECTS CLINIQUES<br />
Le syndrome de De Morsier serait responsable de 30 % environ<br />
des observations d’hypoplasies hypophysaires. L’hypoplasie<br />
papillaire, parfois au premier plan du syndrome de De<br />
Morsier chez un nourrisson au comportement de cécité ou de<br />
trouble du développement visuel, doit amener à poursuivre le<br />
bilan clinique à la recherche d’autres anomalies. Cette hypoplasie<br />
papillaire est évoquée devant une papille de très petite taille<br />
par diminution du nombre d’axones au niveau du nerf optique.<br />
Elle est toujours bilatérale, mais son importance est variable,<br />
plus ou moins marquée. C’est la raison pour laquelle son retentissement<br />
sur la fonction visuelle n’est pas prévisible. Au maximum,<br />
il peut être observé un nystagmus traduisant une<br />
profonde malvoyance. L’altération de la vision est souvent<br />
moins sévère et l’hypoplasie des nerfs optiques est découverte<br />
lors du bilan d’un strabisme ou d’un comportement visuel<br />
anormal chez un jeune enfant. Il faut insister sur la nécessité de<br />
réaliser une rééducation de l’amblyopie organique associée<br />
chez ces enfants. Dans les formes majeures, le diagnostic est<br />
facile devant une papille de taille très réduite (fig. 27-28). En<br />
revanche, le diagnostic est plus difficile dans les formes minimes,<br />
segmentaires, avec une papille ovalaire, allongée verticalement<br />
ou irrégulière. De plus, il arrive qu’une bande de sclère,<br />
due à un arrêt de l’épithélium pigmenté à distance de la papille<br />
hypoplasique, entoure cette petite papille lui donnant un<br />
aspect en double anneau ou d’image « en cocarde », pouvant<br />
laisser croire à tort que la papille a une surface normale. Le<br />
bilan électrophysiologique redresse alors le diagnostic en<br />
retrouvant une diminution d’amplitude des PEV. Le diagnostic<br />
est confirmé en neuro-imagerie, qui objective la gracilité des<br />
nerfs optiques. Ces examens permettent de retrouver des anomalies<br />
cérébrales associées.<br />
Les manifestations endocriniennes sont parfois au premier<br />
plan. L’hypophyse peut être en position ectopique ou absente,<br />
comme en témoignent les observations neuroradiologiques de<br />
selle turcique vide. Les manifestations endocriniennes, caractérisées<br />
par un déficit de la sécrétion hypophysaire plus ou<br />
moins complet, trouvent leur origine dans un dysfonctionnement<br />
hypothalamique. Ces déficits hypothalamo-hypophysaires<br />
sont parfois sévères et leurs conséquences dramatiques :<br />
lors d’épisodes infectieux, l’hypocorticosolémie induite par cet<br />
hypopituitarisme, associé ou non à un diabète insipide et à des<br />
anomalies de la thermorégulation, peut aboutir à un décès brutal.<br />
L’atteinte hypophysaire peut entraîner une insuffisance<br />
thyroïdienne due à un déficit en TSH, un déficit en hormone<br />
de croissance et un déficit en hormone gonadotrophique. Une<br />
atteinte dissociée est possible, avec des retentissements spécifiques<br />
sur l’évolution de la croissance ou l’âge de la puberté [149] .<br />
Les manifestations neurologiques sont souvent in<strong>fr</strong>acliniques<br />
et les enfants atteints sont généralement totalement<br />
asymptomatiques. Cependant, la neuro-imagerie permet de<br />
retrouver l’agénésie du septum lucidum ou du corps calleux<br />
(fig. 27-29) [195] . Des anomalies cérébelleuses ont également<br />
été rapportées [31] .<br />
Fig. 27-28 – Hypoplasie papillaire évidente chez un patient dont la<br />
papille est de taille nettement inférieure à la normale.<br />
(Collection de J.-L. Dufier.)<br />
ASPECTS GÉNÉTIQUES<br />
Mode de transmission<br />
Les formes sporadiques du syndrome de De Morsier sont les<br />
plus <strong>fr</strong>équentes, ce qui avait amené à réfuter l’existence de<br />
formes familiales. Mais de rares observations de plusieurs<br />
enfants atteints, garçons ou filles, nés de parents indemnes,<br />
parfois consanguins, ont été rapportées. Une transmission<br />
récessive autosomique a été évoquée sur ces données jusqu’à<br />
ce que Thomas rapporte en 2001 l’existence de mutations<br />
hétérozygotes dans le gène HESX1 au cours d’authentiques<br />
syndromes de De Morsier, permettant d’évoquer une transmission<br />
dominante autosomique à pénétrance variable [206] .<br />
Gène du syndrome de De Morsier<br />
Une première mutation faux-sens (Arg53Cys/R160C), présente<br />
à l’état homozygote, a été identifiée dès 1998 dans le gène<br />
Fig. 27-29 – L’examen neuroradiologique met en évidence une agénésie<br />
du septum lucidum chez un enfant porteur d’une hypoplasie papillaire,<br />
permettant de porter le diagnostic de syndrome de De Morsier.<br />
(Collection de J.-L. Dufier.)<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 425
Livre.book Page 426 Jeudi, 26. février 2009 3:40 15<br />
HESX1 chez un <strong>fr</strong>ère et une sœur atteints d’un syndrome de De<br />
Morsier et nés de parents consanguins [58] . Ce gène HESX1,<br />
localisé en 3p21.2-p21.1 et possédant quatre exons, est l’homologue<br />
du gène murin Hesx1. Ce dernier est un gène essentiel<br />
dans la mise en place de l’encéphale puisqu’il s’exprime au<br />
niveau de la poche de Rathke dont dérive l’antéhypophyse. Le<br />
phénotype des souris porteuses d’une mutation au niveau de ce<br />
gène est très peu différent de celui des patients porteurs d’un<br />
syndrome de De Morsier. En effet, ces souris sont anophtalmes<br />
ou microphtalmes. On retrouve une dysplasie hypophysaire,<br />
des anomalies du septum lucidum et du corps calleux, ainsi que<br />
des malformations de la portion antérieure du cerveau et de la<br />
région hippocampique. Le rôle du gène HESX1/Hesx1 semble<br />
donc essentiel dans la mise en place de cette région cérébrale.<br />
La découverte de mutations dans ce gène HESX1 a permis de<br />
démontrer une identité dans les mécanismes génétiques responsables<br />
du syndrome de De Morsier ou des hypoplasies hypophysaires<br />
isolées sans anomalie ophtalmologique ni de la ligne<br />
médiane. Trois autres mutations faux-sens du gène HESX1 présentes<br />
à l’état hétérozygote ont été associées à des hypoplasies<br />
hypophysaires isolées peu sévères de pénétrance variable dans<br />
la <strong>fr</strong>atrie. Tajima a décrit une quatrième mutation associée à un<br />
syndrome de De Morsier atypique puisqu’unilatéral gauche [202] .<br />
Cette mutation (306/307insAG) est responsable d’un décalage<br />
du cadre de lecture aboutissant à un codon stop et à la synthèse<br />
d’une protéine tronquée.<br />
La protéine HESX1 appartient à la famille des protéines Paired.<br />
Du fait de la présence de son homéodomaine, elle est<br />
capable de former un dimère au niveau d’un site de liaison spécifique<br />
de l’ADN présentant des motifs TAAT [42] . Chez la souris,<br />
la liaison de la protéine Hesx1 sur l’ADN aboutit à une<br />
action répressive vis-à-vis de la protéine Prop1. Cette protéine<br />
Prop1 est nécessaire à la prolifération et à la différenciation des<br />
cellules de l’antéhypophyse. En effet, Hesx1 et Prop1 se fixent<br />
sur le même site de liaison de l’ADN et — par un mécanisme<br />
dit « de répression hétéromérique » — la protéine Hesx1 inhibe<br />
l’activité de Prop1. Lorsque l’expression de Hesx1 diminue<br />
dans le temps, la différenciation cellulaire de l’hypophyse sous<br />
la dépendance de Prop1 s’accroît. La plupart des mutations du<br />
gène HESX1 décrites dans le syndrome de De Morsier aboutissent<br />
à la synthèse d’une protéine présentant une altération de<br />
son homéodomaine. Il en résulte une moindre liaison ou une<br />
impossibilité de liaison de cette protéine mutée à son site<br />
ADN, diminuant ainsi son activité répressive sur la protéine<br />
Prop1. À l’inverse, Cohen a décrit une délétion (g1684delG) qui<br />
aboutit à la synthèse d’une protéine dont la fixation sur son<br />
site de liaison ADN est accrue [52] . Cette protéine développe<br />
une action répressive trop importante sur la protéine Prop1.<br />
Certaines mutations observées lors des hypoplasies hypophysaires<br />
isolées affectent le site répresseur de la protéine.<br />
MICROCÉPHALIES PRIMITIVES<br />
Les microcéphalies peuvent être primitives, lorsqu’elles sont<br />
d’origine génétique, ou secondaires lorsqu’elles sont dues à<br />
des causes toxiques, iatrogènes ou infectieuses. Les<br />
microcéphalies primitives sont des malformations au cours<br />
desquelles le périmètre crânien est inférieur à au moins trois<br />
déviations standards de la valeur normale compte tenu de<br />
l’âge du patient. Cette différence peut atteindre sept<br />
déviations standards. Elles sont secondaires à un défaut de<br />
développement cérébral dont la croissance conditionne<br />
l’expansion de la boîte crânienne. Au cours des microcépha-<br />
426 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
lies, le cerveau est de morphologie strictement normale mais<br />
son volume est réduit. C’est la raison pour laquelle il n’est pas<br />
retrouvé d’anomalie neurologique. Cependant, l’existence<br />
d’un retard mental modéré ou sévère est <strong>fr</strong>équemment rapportée.<br />
Ces microcéphalies primitives sont transmises selon<br />
un mode récessif autosomique. Au moins cinq loci ont été<br />
localisés, mais aucun n’a été identifié. Le gène MCPH1 a été<br />
localisé dans deux familles consanguines pakistanaises en<br />
8p22-pter, le gène MCPH2 est situé sur le bras long du chromosome<br />
19, en 19q, et le gène MCPH3, également localisé<br />
dans une famille consanguine pakistanaise, est localisé en<br />
9q34. Un gène MCPH4 a été rapporté en 15q et le gène<br />
MCPH5 a été localisé en 1q25-q32 dans une famille turque<br />
consanguine, de huit enfants dont trois étaient atteints.<br />
Microcéphalie et lacunes rétiniennes<br />
Il a été rapporté une forme particulière de microcéphalie primitive<br />
associée à des anomalies choriorétiniennes [11] . Au cours de<br />
cette association, la microcéphalie et le déficit mental sont plus<br />
ou moins marqués (fig. 27-30, a et b). Les anomalies choriorétiniennes<br />
réalisent des plages atrophiques multiples dont le diamètre<br />
varie d’un demi à un diamètre papillaire. Leur aspect est<br />
peu différent de celui observé au décours des infections toxoplasmiques<br />
(fig. 27-30, c et d). D’autres anomalies ophtalmologiques<br />
ont été rapportées, telles qu’une hypoplasie papillaire ou<br />
une gracilité vasculaire. Les anomalies choriorétiniennes ne sont<br />
sans doute pas limitées aux seules plages atrophiques,<br />
puisqu’une étude électrorétinographique a mis en évidence des<br />
réductions des réponses pouvant atteindre 60 à 70 %. Ces anomalies<br />
électrophysiologiques sont stables au cours du temps sur<br />
une étude longitudinale de quatorze ans [124] .<br />
La transmission peut être dominante autosomique (maladie de<br />
[2, 11,<br />
Dufier) ou récessive autosomique (maladie de Giacomini)<br />
190] . De plus, il a été rapporté une hétérogénéité intrafamiliale<br />
puisqu’on retrouve l’association des deux désordres chez certains<br />
enfants alors qu’il n’est retrouvé qu’une microcéphalie<br />
chez d’autres. Il n’existe encore aucun gène candidat permettant<br />
d’expliquer la présence de ce syndrome.<br />
CÉPHALÉES<br />
Il a été établi depuis de nombreuses années que les différentes<br />
formes de céphalées ont une composante héréditaire.<br />
Mais leur mode de transmission n’est pas clairement établi.<br />
Ainsi, des données contradictoires ont été obtenues en ce qui<br />
concerne l’algie vasculaire de la face dont la transmission<br />
pourrait être dominante autosomique ou récessive autosomique.<br />
La migraine simple avec ou sans aura serait transmise<br />
selon un mode multifactoriel. Enfin, différentes formes de<br />
céphalées peuvent coexister au sein d’une même <strong>fr</strong>atrie.<br />
Néanmoins, au moins six gènes responsables de migraine simple<br />
avec ou sans aura ont été localisés en 4q24 (MGR1), Xq<br />
(MGR2), 6q21.1-p21.2 (MGR3), 14q21.2-q22.3 (MGR4), 19q13<br />
(MGR5) et 1q31 (MGR6). Cette dernière localisation est identique<br />
à celle d’une forme de migraine hémiplégique familiale<br />
dominante autosomique. Deux autres gènes de migraine hémiplégique<br />
familiale dominante autosomique ont été identifiés.<br />
Le premier, localisé en 19q13 code un canal calcique de type L<br />
(CACNL1A4) et le second, en 1q21, code une sous-unité α 2<br />
d’une ATPase. Ces différentes formes de migraines peuvent<br />
comporter des auras visuelles à type de phosphènes scintillants,<br />
scotomes positifs ou hallucinations visuelles.
Livre.book Page 427 Jeudi, 26. février 2009 3:40 15<br />
a b<br />
c d<br />
Fig. 27-30 – Dans sa forme dominante autosomique, la microcéphalie primitive associée à des lacunes rétiniennes réalise le syndrome de Dufier.<br />
a. b. Le périmètre crânien est réduit, ce que confirme la radiographie du crâne. Le volume de la boîte crânienne est inférieur à la normale. c. L’examen du fond<br />
d’œil met en évidence des plages d’atrophie choriorétinienne multiples. d. Chez un autre patient, présence d’un pli falciforme. (Collection de J.-L. Dufier.)<br />
Il faut évoquer à part le CADASIL, ou Cerebral Autosomal<br />
Dominant Arteriopathy with Subcortical Infarcts and Leucoencephalopathy,<br />
artériopathie cérébrale intéressant principalement<br />
les artérioles cérébrales de moyen calibre et responsable de la<br />
survenue d’accidents ischémiques cérébraux sous-corticaux<br />
récidivants et précoces. Au stade initial, ces accidents vasculaires<br />
cérébraux peuvent en imposer pour des épisodes de<br />
migraine avec aura, dont la récupération est plus ou moins<br />
complète [217] . Puis, l’évolution se fait en quelques années vers<br />
une aggravation des déficits neurologiques avec apparition<br />
d’un syndrome pseudobulbaire et d’une détérioration progressive<br />
des fonctions supérieures. À ce stade, les examens<br />
neuroradiologiques mettent en évidence de multiples hypersignaux<br />
diffus de la substance blanche et des noyaux gris centraux,<br />
correspondant aux différents accidents ischémiques. Le<br />
décès survient rapidement dans ce tableau de démence vasculaire.<br />
Les anomalies vasculaires ne sont pas limitées au sys-<br />
tème nerveux central. L’existence d’anomalies spécifiques des<br />
parois d’artères cutanées ou musculaires peut aider au diagnostic<br />
[104] . Des malformations des artérioles rétiniennes ont<br />
été rapportées chez des patients porteurs de CADASIL, ainsi<br />
que des anomalies pouvant être la conséquence d’une ischémie<br />
rétinienne localisée [90] .<br />
Cette artériopathie cérébrale est transmise selon un mode<br />
dominant autosomique et le gène responsable a été identifié<br />
en 1996. Des mutations ont été retrouvées dans le gène<br />
NOTCH3. Ce gène, localisé sur le chromosome 19 en<br />
19p13.2-p13.1, code une protéine-signal comportant un<br />
domaine intracellulaire et un domaine extracellulaire, elle<br />
joue un rôle dans le développement [103] . Les mutations responsables<br />
du CADASIL affectent le domaine extracellulaire et<br />
certaines d’entre elles altèrent la liaison de cette protéine à ses<br />
protéines régulatrices [105] .<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 427
Livre.book Page 428 Jeudi, 26. février 2009 3:40 15<br />
TABLEAU 27-IV<br />
Dégénérescences spinocérébelleuses et paraparésie spastiques.<br />
Autres manifestations<br />
Manifestation<br />
neurologique<br />
Manifestation<br />
ophtalmologique<br />
Mode<br />
évolutif<br />
Âge<br />
de début<br />
Mode de<br />
transmission<br />
Nom Localisation Gène Protéine<br />
Cardiomyopathie<br />
Pieds creux<br />
Syndrome cérébelleux<br />
Syndrome cordonal<br />
postérieur<br />
Atrophie optique chez 12 à<br />
50 % des patients<br />
Altération des PEV<br />
Freidreich 9q13 Frataxine AR 6 ans Lentement<br />
évolutif<br />
9p23-p11 ?<br />
Surdité<br />
Atrophie optique Amyotrophie progressive<br />
distale des membres<br />
Syndrome cordonal<br />
postérieur<br />
Pied creux<br />
Cf. note de bas de tableau AD, AR, RLX Entre 3 ans<br />
et 68 ans<br />
selon les<br />
gènes en<br />
cause<br />
Charcot-Marie-<br />
Tooth<br />
Néant Paraparésie spastique<br />
Pied creux<br />
Syndrome cordonal<br />
postérieur<br />
Syndrome pyramidal<br />
14q11.2-q21 SPG3 Atlastine AD 20 ans Lentement<br />
évolutif<br />
Maladie de<br />
Strumpell<br />
Lorrain (SPG3)<br />
428 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
Retard mental<br />
Évolutif Identique SPG3, mais avec<br />
un tableau plus sévère<br />
SPG4 2p22-p21 SPG4 Spastine Plus tardif<br />
que SPG3<br />
Amyoptrophie des mollets<br />
Paraparésie spastique<br />
Syndrome pyramidal<br />
Pied creux<br />
Syndrome cordonal<br />
postérieur<br />
20 ans Lentement<br />
évolutif<br />
SPG6 15q11.1 NIPA Transporteur<br />
membranaire<br />
?<br />
? 18 à 26 ans Syndrome pyramidal<br />
SPG8 823-q24 Gène de la<br />
protéine<br />
associée à la<br />
dystrophine<br />
? 10 à 20 ans<br />
SPG10 12q13 Gène de la<br />
kinésine 5A<br />
Anomalies des voies<br />
urinaires basses<br />
SPG12 19q13 ? ? 14 ans Paraparésie spastique<br />
Pied creux<br />
Syndrome cordonal<br />
postérieur<br />
Syndrome pyramidal<br />
Amyoptrophie<br />
Reflux gastro-œsophagien<br />
Anomalies squelettiques<br />
Cataracte congénitale Identique SPG3, mais avec<br />
un tableau incomplet,<br />
moins marqué<br />
SPG9 10q23.3-q24.1 ? ? AD 10 à 20 ans Lentement<br />
évolutif
Livre.book Page 429 Jeudi, 26. février 2009 3:40 15<br />
TABLEAU 27-IV (suite)<br />
Dégénérescences spinocérébelleuses et paraparésie spastiques.<br />
Autres manifestations<br />
Manifestation<br />
neurologique<br />
Manifestation<br />
ophtalmologique<br />
Mode<br />
évolutif<br />
Âge<br />
de début<br />
Mode de<br />
transmission<br />
Nom Localisation Gène Protéine<br />
Atteinte des IXe , Xe et XIIe paires crâniennes<br />
Néant Paraparésie spastique<br />
Troubles de la marche<br />
Syndrome cordonal<br />
postérieur des membres<br />
inférieurs<br />
Syndrome pyramidal<br />
SPG5 8p12-q13 ? ? AR Précoce Lentement<br />
évolutif<br />
Pâleur papillaire Paraparésie spastique Dysarthrie<br />
Troubles de la marche Dysphagie<br />
Syndrome cordonal<br />
Néant Retard mental<br />
postérieur des membres<br />
inférieurs<br />
Syndrome pyramidal<br />
Pied creux<br />
SPG7 16q24.3 SPG7 Paraplégine 25 à 40 ans Lentement<br />
évolutif<br />
SPG14 3q27-q28 ? ? 30 ans Lentement<br />
évolutif<br />
Retard mental<br />
Dysarthrie<br />
Amyoptrophie distale<br />
Remaniement maculaire Paraparésie spastique<br />
Syndrome pyramidal<br />
SPG15 14q ? ? 30 à 35 ans Lentement<br />
évolutif<br />
Retard mental possible<br />
Paraparésie spastique<br />
Troubles de la marche<br />
Syndrome cordonal<br />
postérieur<br />
Syndrome pyramidal<br />
Atrophie optique <strong>fr</strong>équente<br />
Nystagmus<br />
RLX Précoce Lentement<br />
évolutif<br />
Constituant<br />
de la myéline<br />
SPG2 Xq22 Gène de la<br />
protéolipide<br />
myélinique<br />
Dysarthrie<br />
Dysphagie<br />
Spasticité des membres<br />
inférieurs<br />
Syndrome pyramidal<br />
Ataxie +/- pied creux et<br />
syndrome cordonal<br />
postérieur<br />
Diminution de la vitesse<br />
des saccades, pertes de la<br />
verticalité du regard, ptosis<br />
ou rétraction de la paupière<br />
supérieure<br />
12p13 SAX1 ? AD Tardif Évolutif<br />
Ataxie spastique<br />
(ataxie de Pierre<br />
Marie)<br />
Retard mental<br />
Spasticité des membres<br />
inférieurs<br />
Syndrome pyramidal<br />
Ataxie<br />
? ? ? AR vers 10 ans Ophtalmoplégie internucléaire<br />
Atrophie optique (?)<br />
Dysarthrie<br />
Prolpasus de la valve<br />
mitrale<br />
Amyotrophie distale<br />
Spasticité des membres<br />
inférieurs<br />
Syndrome pyramidal<br />
Ataxie<br />
Nystagmus<br />
Altération de la poursuite<br />
Anomalies rétiniennes<br />
13q12 SACS Sacsine AR Dès l’enfance Peu évolutif<br />
après 20<br />
ans<br />
NB : Plus de quinze gènes différents de la maladie de Charcot-Marie-Tooth ont été localisés ou identifiés. Ces gènes sont situés soit sur des autosomes, soit sur le chromosome X, et tous les modes de<br />
transmission ont été évoqués.<br />
AD, autosomique récessif ; AR, autosomique récessif ; RLX, récessif lié au chromosome X.<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 429
Livre.book Page 430 Jeudi, 26. février 2009 3:40 15<br />
TABLEAU 27-V<br />
Ataxies spinocérébelleuses responsables d’anomalies oculomotrices.<br />
Les ataxies spinocérébelleuses dominantes sont séparées en trois groupes. Le premier groupe est caractérisé par l’existence d’un syndrome cérébelleux associé à un syndrome pyramidal et à des troubles<br />
oculomoteurs <strong>fr</strong>ancs. Dans le deuxième groupe, une dégénérescence rétinienne sévère est retrouvée en complément des anomalies déjà évoquées dans le premier groupe. Génétiquement, ces deux<br />
groupes sont caractérisés par l’existence d’expansions de triplets de nucléotides CAG. De nombreuses ataxies spinocérébelleuses relevant d’anomalies génétiques différentes dans des gènes propres ont<br />
été réunies dans le troisième groupe. Elles sont caractérisées par la prédominance du syndrome cérébelleux sur les autres anomalies neurologiques. Dans ce troisième groupe, nous ne citons que les<br />
ataxies spinocérébelleuses responsables d’anomalies oculomotrices<br />
Neuroradiologie<br />
Manifestation<br />
neurologique<br />
Manifestation<br />
ophtalmologique<br />
Protéine Âge de début<br />
Anomalie<br />
génétique<br />
Gène<br />
Localisation<br />
Type Nom<br />
Atrophie<br />
cérébelleuse<br />
et pontique<br />
Syndrome cérébelleux<br />
Syndrome pyramidal<br />
30 ans Augmentation d’amplitude<br />
des saccades / saccades<br />
hypermétriques<br />
Diminution du gain de la poursuite<br />
Ataxine-1 (rôle<br />
dans<br />
l’ubiquitination<br />
des protéines)<br />
ADAC I SCA 1 6p23 ATX-1 Expansion de CAG<br />
avec anticipation<br />
Atrophie<br />
cérébelleuse<br />
et pontique<br />
Syndrome cérébelleux<br />
Syndrome pyramidal<br />
Diplopie<br />
Diminution de la vitesse<br />
des saccades<br />
Augmentation du nombre<br />
d’erreurs lors d’épreuves<br />
d’anti-saccades<br />
Ataxine-2 2 à 65 ans<br />
(40% avant<br />
25 ans)<br />
SCA 2 12q24 ATX-2 Expansion de CAG<br />
avec anticipation<br />
430 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
Élargissement<br />
du 4e ventricule<br />
Syndrome cérébelleux<br />
Syndrome pyramidal<br />
Ataxine-3 Après 40 ans Nystagmus<br />
Saccades hypométriques<br />
Diminution du gain de la poursuite<br />
14q24.3-q31 MJD Expansion de CAG<br />
avec anticipation<br />
SCA3 Machado-<br />
Joseph<br />
Atrophie<br />
cérébelleuse<br />
et pontique<br />
Syndrome cérébelleux<br />
Syndrome pyramidal<br />
Ataxine-7 Précoce Ophtalmoplégie supranucléaire<br />
Dégénérescence rétinienne<br />
maculaire ou périphérique<br />
ADAC II SCA 7 3p21.1-p12 SCA-7 Expansion de CAG<br />
avec anticipation<br />
Atrophie<br />
cérébelleuse<br />
Syndrome cérébelleux<br />
dynamique<br />
20 à 65 ans Nystagmus horizontal<br />
Poursuite saccadée<br />
Sous unité α des<br />
canaux calciques<br />
voltagedépendants<br />
ADAC III SCA 6 19p13 CACNA1A Expansion de CAG<br />
avec anticipation<br />
SCA 5 11p11-q11 ? Anticipation ? 10 à 68 ans Néant Syndrome cérébelleux<br />
dynamique<br />
Atrophie<br />
cérébelleuse<br />
Nystagmus horizontal Syndrome cérébelleux<br />
dynamique<br />
? Tardif (55 ans<br />
en moyenne)<br />
SCA 4 16q22.1 ? Anticipation peu<br />
importante<br />
Atrophie<br />
cérébelleuse et<br />
cérébrale diffuse<br />
? 14 à 44 ans Dyskinésie oculomotrice Syndrome cérébelleux<br />
cinétique<br />
Crises comitiales<br />
SCA 10 22q13 ? Expansion d’un<br />
groupe de<br />
5 nucléotides avec<br />
anticipation<br />
Atrophie<br />
cérébelleuse et<br />
corticale diffuse<br />
Syndrome cérébelleux<br />
cinétique<br />
Démence<br />
8 à 55 ans Nystagmus<br />
Dyskinésie oculaire<br />
SCA 12 5q31-q33 PPP2R2B Expansion de CAG Protéine<br />
phosphatase 2A<br />
ADAC : ataxies spinocérébelleuses dominantes ; SCA : ataxie spinocérébelleuses.
Livre.book Page 431 Jeudi, 26. février 2009 3:40 15<br />
TABLEAU 27-VI<br />
Ataxies cérébelleuses congénitales.<br />
Nom Localisation<br />
Mode<br />
de<br />
transmission<br />
ATAXIES ET DÉGÉNÉRESCENCES<br />
SPINOCÉRÉBELLEUSES<br />
Les caractéristiques cliniques et les données génétiques<br />
concernant les principales formes d’ataxies cérébelleuses<br />
congénitales, d’ataxies et de dégénérescences spinocérébelleuses<br />
ainsi que de paraparésies spastiques, ont été regroupées<br />
dans les tableaux 27-IV à 27-VI.<br />
BIBLIOGRAPHIE<br />
Âge<br />
de début<br />
[1] Abadi RV, Bjerre A. Motor and sensory characteristics of infantile nystagmus.<br />
Br J Ophthalmol 2002, 86 : 1152-1160.<br />
[2] Abdel-Salam GM, Czeizel AE, Vogt G et al. Microcephaly with chorioretinal<br />
dysplasia : characteristic facial features. Am J Med Genet. 2000, 95 :<br />
513-515.<br />
[3] Aberfeld DC. Hereditary ptosis. Birth Defects Orig Artic Ser 1971, 7 : 63-<br />
65.<br />
[4] Abicht A, Stucka R, Karcagi V et al. A Common mutation (ε2167delG) in<br />
congenital myasthenic patients of Gypsy ethnic origin. Neurology 1999,<br />
53 : 1564-1569.<br />
[5] Abrahamsson M, Fabian Gsjostrand J. Re<strong>fr</strong>action changes in children<br />
developing convergent or divergent strabismus. Br J Ophthalmol 1992,<br />
76 : 723-727.<br />
[6] Abrahamsson M, Magnusson G, Sjostrand J. Inheritance of strabismus<br />
and the gain of using heredity to determine populations at risk of developing<br />
strabismus. Acta Ophthalmol Scand 1999, 77 : 653-657.<br />
[7] Agius MA, Richman DP, Fairclough RH et al. Three forms of immune<br />
myasthenia. Ann N Y Acad Sci 2003, 998 : 453-456.<br />
[8] Aguirre-Aquino BI, Rogers D Gtraboulsi EI. A patient with de Morsier<br />
and Duane syndromes. J Aapos 2000, 4 : 243-245.<br />
[9] Al-Baradie R, Yamada K, St Hilaire C et al. Duane radial ray syndrome<br />
(Okihiro syndrome) maps to 20q13 and results <strong>fr</strong>om mutations in<br />
SALL4, a new member of the SAL family. Am J Hum Genet 2002, 71 :<br />
1195-1199.<br />
[10] Alon M, Korczyn AD. Pupillary responses and blink reflex in myotonic<br />
dystrophy. Clin Auton Res 1992, 2 : 17-19.<br />
[11] Alzial C, Dufier J, Brasnu C et al. "True" microcephaly with dominantinheritance<br />
chorioretinal dysplasia. Ann Genet 1980, 23 : 91-94.<br />
[12] Amiel J, Audollent S, Joly D, Dureau P, Salomon R, Tellier A-L, Auge J,<br />
Bouissou F, Antignac C, Gubler M-C, Eccles M-R, Munnich A, Vekemans<br />
M, Lyonnet S, Attie-Bitach T. PAX2 mutations in renal-coloboma<br />
syndrome: mutational hotspot and germline mosaicism. Eur J Hum Genet<br />
2000, 8 : 820-6.<br />
[13] Andegeko Y, Moyal L, Mittelman L et al. Nuclear retention of ATM at<br />
sites of DNA double strand breaks. J Biol Chem 2001, 276 : 38224-38230.<br />
[14] Appukuttan B, Gillanders E, Juo SH et al. Localization of a gene for<br />
Duane retraction syndrome to chromosome 2q31. Am J Hum Genet 1999,<br />
65 : 1639-1646.<br />
Mode<br />
évolutif<br />
Manifestation<br />
ophtalmologique<br />
Manifestation<br />
neurologique<br />
CLA 1 9q34-qter AR Congénital Nystagmus Syndrome<br />
cérébelleux<br />
dynamique<br />
CLA 2 Xp11.21q21.3<br />
RLX Congénital Lentement<br />
progressif<br />
Nystagmus<br />
Ralentissement des<br />
mouvements<br />
oculaires<br />
Syndrome<br />
cérébelleux<br />
dynamique<br />
CLA 3 20q11-q13 AR Congénital Non évolutif Nystagmus Syndrome<br />
cérébelleux<br />
dynamique<br />
AR : Autosomique récessif; RLX : récessif lié au chromosome X.<br />
Anomalies<br />
neuroradiologiques<br />
Atrophie vermienne<br />
importante<br />
Atrophie<br />
cérébelleuse diffuse<br />
Atrophie vermienne<br />
[15] Azuma N, Yamaguchi Y, Handa H et al. Mutations of the PAX6 gene<br />
detected in patients with a variety of optic-nerve malformations. Am J<br />
Hum Genet 2003, 72 : 1565-1570.<br />
[16] Baker M, Litvan I, Houlden H et al. Association of an extended haplotype<br />
In the tau gene with progressive supranuclear palsy. Hum Mol Genet<br />
1999, 8 : 711-715.<br />
[17] Baldwin HC, Mammers RM. Congenital blepharoptosis. Ophthalmic<br />
Plastic and Reconstructive Surgery 2002, 18 : 301-307.<br />
[18] Baraitser M, Reardon W. A new case of the Carey-Fineman-Ziter syndrome.<br />
Am J Med Genet 1994, 53 : 163-164.<br />
[19] Barcellos LF, Oksenberg JR, Green A J et al. Genetic basis for clinical<br />
expression in multiple sclerosis. Brain 2002, 125 : 150-158.<br />
[20] Battini R, Bianchi MC, Boespflug-Tanguy O et al. Unusual clinical and<br />
magnetic resonance imaging findings in a family with proteolipid protein<br />
gene mutation. Arch Neurol 2003, 60 : 268-272.<br />
[21] Beeson D, Jeremiah S, West LF et al. Assignment of the human nicotinic<br />
acetylcholine receptor genes : the alpha and delta subunit genes to chromosome<br />
2 and the beta subunit gene to chromosome 17. Ann Hum Genet<br />
1990, 54 : 199-208.<br />
[22] Benit P, Steffann J, Lebon S et al. Genotyping microsatellite DNA markers<br />
at putative disease loci in inbred/multiplex families with respiratory<br />
chain complex I deficiency allows rapid identification of a novel nonsense<br />
mutation (IVS1nt -1) in the NDUFS4 gene in Leigh syndrome. Hum<br />
Genet 2003, 112 : 563-566.<br />
[23] Betz R, Rensing C, Otto E et al. Children with ocular motor apraxia type<br />
Cogan carry deletions in the gene (NPHP1) for juvenile nephronophthisis.<br />
J Pediatr 2000, 136 : 828-831.<br />
[24] Black GCM, Perveen R, Hatchwell E et al. Locus heterogeneity in autosomal<br />
dominant congenital external ophthalmoplegia (CFEOM). J Med<br />
Genet 1998, 35 : 985-988.<br />
[25] Blair IP, Gibson RR, Bennett CL et al. Search for genes involved in Joubert<br />
syndrome : evidence that one or more major loci are yet to be identified<br />
and exclusion of candidate genes EN1, EN2, FGF8, and BARHL1.<br />
Am J Med Genet 2002, 107 : 190-196.<br />
[26] Blumenfeld A, Slaugenhaupt SA, Liebert CB et al. Precise genetic mapping<br />
and haplotype analysis of the familial dysautonomia gene on<br />
human chromosome 9q31. Am J Hum Genet 1999, 64 : 1110-1118.<br />
[27] Bobba A, Marra E, Fathallah DM et al. Non-radioactive detection of five<br />
common microsatellite markers for ATP7B gene in Wilson disease<br />
patients. Mol Cell Probes 2003, 17 : 271-274.<br />
[28] Borck G, Wirth J, Hardt T et al. Molecular cytogenetic characterisation of<br />
a complex 46,XY,t(7;8;11;13) chromosome rearrangement in a patient<br />
with Mœbius syndrome. J Med Genet 2001, 38 : 117-121.<br />
[29] Botelho PJ, Giangiacomo JG. Autosomal-dominant inheritance of congenital<br />
superior oblique palsy. Ophthalmology 1996, 103 : 1508-1511.<br />
[30] Brackett LE, Demers LM, Mamourian AC et al. Mœbius syndrome in<br />
association with hypogonadotropic hypogonadism. J Endocrinol Invest<br />
1991, 14 : 599-607.<br />
[31] Brickman JM, Clements M, Tyrell R et al. Molecular effects of novel<br />
mutations in Hesx1/HESX1 associated with human pituitary disorders.<br />
Development 2001, 128 : 5189-5199.<br />
[32] Brown CA, Neote K, Leung A et al. Introduction of the alpha subunit<br />
mutation associated with the B1 variant of Tay-Sachs disease into the<br />
beta subunit produces a beta-hexosaminidase B without catalytic activity.<br />
J Biol Chem 1989, 264 : 21705-21710.<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 431
Livre.book Page 432 Jeudi, 26. février 2009 3:40 15<br />
[33] Brownlow S, Webster R, Croxen R et al. Acetylcholine receptor delta<br />
subunit mutations underlie a fast-channel myasthenic syndrome and<br />
arthrogryposis multiplex congenita. J Clin Invest 2001, 108 : 125-130.<br />
[34] Bruck I, Antoniuk SA, Carvalho Neto AD et al. Cerebellar vermis hypoplasia<br />
- non progressive congenital ataxia : clinical and radiological findings<br />
in a pair of siblings. Arq Neuropsiquiatr 2000, 58 : 897-900.<br />
[35] Burke G, Cossins J, Maxwell S et al. Rapsyn mutations in hereditary<br />
myasthenia : Distinct early- and late-onset phenotypes. Neurology 2003,<br />
61 : 826-828.<br />
[36] Cabot A, Rozet J-M, Gerber S et al. A gene for X-linked idiopathic<br />
congenital nystagmus (NYS1) maps to chromosome Xp11.4-p11.3. Am J<br />
Hum Genet 1999, 64 : 1141-1146.<br />
[37] Calabrese G, Stuppia L, Morizio E et al. Detection of an insertion deletion<br />
of region 8q13-q21.2 in a patient with Duane syndrome : implications<br />
for mapping and cloning a Duane gene. Eur J Hum Genet 1998, 6 :<br />
187-193.<br />
[38] Calabrese G, Telvi L, Capodiferro F et al. Narrowing the Duane syndrome<br />
critical region at chromosome 8q13 down to 40 kb. Eur J Hum<br />
Genet 2000, 8 : 319-324.<br />
[39] Carpenter EM, Goddard JM, Chisaka O et al. Loss of Hox-A1 (Hox-1.6)<br />
function results in the reorganization of the murine hindbrain. Development<br />
1993, 118 : 1063-1075.<br />
[40] Carsana A, Fortunato G, De Sarno C et al. Identification of new polymorphisms<br />
in the CACNA1S gene. Clin Chem Lab Med 2003, 41 : 20-22.<br />
[41] Carstea ED, Polymeropoulos MH, Parker CC et al. Linkage of Niemann-<br />
Pick disease type C to human chromosome 18. Proc Natl Acad Sci USA<br />
1993, 90 : 2002-2004.<br />
[42] Carvalho LR, Woods KS, Mendonca BB et al. A homozygous mutation in<br />
HESX1 is associated with evolving hypopituitarism due to impaired<br />
repressor-corepressor interaction. J Clin Invest 2003, 112 : 1192-1201.<br />
[43] Chapman J, Korczyn AD, Karussis DM et al. The effects of APOE genotype<br />
on age at onset and progression of neurodegenerative diseases.<br />
Neurology 2001, 57 : 1482-1485.<br />
[44] Chew CK, Foster P, Hurst J A et al. Duane’s retraction syndrome associated<br />
with chromosome 4q27-31 segment deletion. Am J Ophthalmol 1995,<br />
119 : 807-809.<br />
[45] Chol M, Lebon S, Benit P et al. The mitochondrial DNA G13513A<br />
MELAS mutation in the NADH dehydrogenase 5 gene is a <strong>fr</strong>equent<br />
cause of Leigh-like syndrome with isolated complex I deficiency. J Med<br />
Genet 2003, 40 : 188-191.<br />
[46] Chong MJ, Murray MR, Gosink EC et al. Atm and Bax cooperate in ionizing<br />
radiation-induced apoptosis in the central nervous system. Proc Natl<br />
Acad Sci USA 2000, 97 : 889-894.<br />
[47] Christodoulou K, Tsingis M, Deymeer F et al. Mapping of the familial<br />
infantile myasthenia (congenital myasthenic syndrome type Ia) gene to<br />
chromosome 17p with evidence of genetic homogeneity. Hum Mol Genet<br />
1997, 6 : 635-640.<br />
[48] Chung GW, Edwards AO, Schimment ILA et al. Renal-coloboma<br />
syndrome : report of a novel PAX2 gene mutation. Am J Ophthalmol<br />
2001, 132 : 910-914.<br />
[49] Chung M, Stout JT, Borchert MS. Clinical diversity of hereditary<br />
Duane’s retraction syndrome. Ophthalmology 2000, 107 : 500-503.<br />
[50] Claudepierre T, Dalloz C, Mornet D et al. Characterization of the intermolecular<br />
associations of the dystrophin-associated glycoprotein complex<br />
in retinal Muller glial cells. J Cell Sci 2000, 113 : 3409-3417.<br />
[51] Cohen HB. Congenital ptosis. A new pedigree and classification. Arch<br />
Ophthalmol 1972, 87 : 161-163.<br />
[52] Cohen RN, Cohen LE, Botero D et al. Enhanced repression by HESX1 as<br />
a cause of hypopituitarism and septooptic dysplasia. J Clin Endocrinol<br />
Metab 2003, 88 : 4832-4839.<br />
[53] Conrad C, Andreadis A, Trojanowski JQ et al. Genetic evidence for the<br />
involvement of tau in progressive supranuclear palsy. Ann Neurol 1997,<br />
41 : 277-281.<br />
[54] Cormand B, Avela K, Pihko H et al. Assignment of the muscle-eye-brain<br />
disease gene to 1p32-p34 by linkage analysis and homozygosity mapping.<br />
Am J Hum Genet 1999, 64 : 126-135.<br />
[55] Cox DW, Moore SD. Copper transporting P-type ATPases and human<br />
disease. J Bioenerg Biomembr 2002, 34 : 333-338.<br />
[56] Crone RA, Velzeboer CMJ. Statistics on strabismus in the American<br />
youth. Arch ophthalmol 1956, 55 : 455-470.<br />
[57] Daskalakis GJ, Papageorgiou IS, Petrogiannis ND et al. Myasthenia gravis<br />
and pregnancy. Eur J Obstet Gynecol Reprod Biol 2000, 89 : 201-204.<br />
[58] Dattani MT, Martinez-Barbera JP, Thomas PQ et al. HESX1 : a novel<br />
gene implicated in a familial form of septo-optic dysplasia. Acta Paediatr<br />
Suppl 1999, 88 : 49-54.<br />
[59] Dattani MT, Martinez-Barbera JP, Thomas PQ et al. Mutations in the<br />
homeobox gene HESX1/Hesx1 associated with septo-optic dysplasia in<br />
human and mouse. Nat Genet 1998, 19 : 125-133.<br />
[60] Dimauro S, de Vivo DC. Genetic heterogeneity in Leigh syndrome. Ann<br />
Neurol 1996, 40 : 5-7.<br />
[61] Dixon-Salazar T, Silhavy JL, Marsh SE et al. Mutations in the AHI1<br />
Gene, Encoding Joubert, Cause Joubert Syndrome with Cortical polymicrogyria.<br />
Am J Hum Gene 2004, 75 : 979-987.<br />
[62] Djousse L, Knowlton B, Hayden M et al. Interaction of normal and<br />
expanded CAG repeat sizes influences age at onset of Huntington<br />
disease. Am J Med Genet 2003, 119A : 279-282.<br />
432 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
[63] Doherty EJ, Macy ME, Wang SM et al. CFEOM3 : a new extraocular<br />
congenital fibrosis syndrome that maps to 16q24.2-q24.3. Invest Ophthalmol<br />
Vis Sci 1999, 40 : 1687-1694.<br />
[64] Donger C, Krejci E, Serradell AP et al. Mutation in the human acetylcholinesterase-associated<br />
collagen gene, COLQ, is responsible for congenital<br />
myasthenic syndrome with end-plate acetylcholinesterase deficiency<br />
(Type Ic). Am J Hum Genet 1998, 63 : 967-975.<br />
[65] Dufier J-L, Briard M-L, Bonaiti C et al. Inheritance in the etiology of<br />
convergent squint. Ophthalmologica 1979, 179 : 225-234.<br />
[66] Duke AM, Hopkins PM, Steele DS. Effects of Mg 2+ and SR luminal Ca 2+<br />
on caffeine-induced Ca 2+ release in skeletal muscle <strong>fr</strong>om humans susceptible<br />
to malignant hyperthermia. J Physiol 2002, 544 : 85-95.<br />
[67] Dunne V, Maselli RA. Identification of pathogenic mutations in the<br />
human rapsyn gene. J Hum Genet 2003, 48 : 204-207.<br />
[68] Eng CM, Slaugenhaupt SA, Blumenfeld A et al. Prenatal diagnosis of<br />
familial dysautonomia by analysis of linked CA-repeat polymorphisms<br />
on chromosome 9q31-q33. Am J Med Genet 1995, 59 : 349-355.<br />
[69] Engle EC, McIntosh N, Yamada K et al. CFEOM1, the classic familial<br />
form of congenital fibrosis of the extraocular muscles, is genetically<br />
heterogeneous but does not result <strong>fr</strong>om mutations in ARIX. BMC Genet<br />
2002, 3 : 3.<br />
[70] Engle EC. The molecular basis of the congenital fibrosis syndromes.<br />
Strabismus 2002, 10 : 125-128.<br />
[71] Ferenci P, Caca K, Loudianos G et al. Diagnosis and phenotypic classification<br />
of Wilson disease. Liver Int 2003, 23 : 139-142.<br />
[72] Flaherty MP, Grattan-Smith P, Steinberg A et al. Congenital fibrosis of<br />
the extraocular muscles associated with cortical dysplasia and maldevelopment<br />
of the basal ganglia. Ophthalmology 2001, 108 : 1313-1322.<br />
[73] Fujita I, Koyanagi T, Kukita J et al. Mœbius syndrome with central hypoventilation<br />
and brainstem calcification : a case report. Eur J Pediatr 1991,<br />
150 : 582-583.<br />
[74] Furling D, Doucet G, Langlois MA et al. Viral vector producing antisense<br />
RNA restores myotonic dystrophy myoblast functions. Gene Ther 2003,<br />
10 : 795-802.<br />
[75] Gamez J, Montane D, Martorell L et al. Bilateral optic nerve atrophy in<br />
myotonic dystrophy. Am J Ophthalmol 2001, 131 : 398-400.<br />
[76] Gian<strong>fr</strong>anceschi L, Siciliano R, Walls J et al. Visual cortex is rescued <strong>fr</strong>om<br />
the effects of dark rearing by overexpression of BDNF. Proc Natl Acad Sci<br />
USA 2003, 100 : 12486-12491.<br />
[77] Giraud M, Beaurain G, Yamamoto AM et al. Linkage of HLA to myasthenia<br />
gravis and genetic heterogeneity depending on anti-titin antibodies.<br />
Neurology 2001, 57 : 1555-1560.<br />
[78] Giugliani R, Dutra J C, Pereira ML et al. GM1 gangliosidosis : clinical and<br />
laboratory findings in eight families. Hum Genet 1985, 70 : 347-354.<br />
[79] Glaser RL, Broman KW, Schulman RL et al. The paternal-age effect in<br />
Apert syndrome is due, in part, to the increased <strong>fr</strong>equency of mutations<br />
in sperm. Am J Hum Genet 2003, 73 : 939-947.<br />
[80] Gottlob I, Jain S, Engle EC. Elevation of one eye during tooth brushing.<br />
Am J Ophthalmol 2002, 134 : 459.<br />
[81] Graf M, Droutsas K, Kaufmann H. Congenital nystagmus : indication,<br />
results and dosage of Kestenbaum surgery in 34 patients. Klin Monatsbl<br />
Augenheilkd 2000, 217 : 334-339.<br />
[82] Grafakou O, Oexle K, Van Den Heuvel L et al. Leigh syndrome due to<br />
compound heterozygosity of dihydrolipoamide dehydrogenase gene<br />
mutations. Description of the first E3 splice site mutation. Eur J Pediatr<br />
2003, 19 : 19.<br />
[83] Griffin JR, Asano GW, Somers R J et al. Heredity in congenital esotropia.<br />
J Am Optom Assoc 1979, 50 : 1237-1242.<br />
[84] Gross C, De Baere E, Lo A et al. Cloning and characterization of human<br />
WDR10, a novel gene located at 3q21 encoding a WD-repeat protein<br />
that is highly expressed in pituitary and testis. DNA Cell Biol 2001, 20 :<br />
41-52.<br />
[85] Guerini FR, Ferrante P, Losciale L et al. Myelin basic protein gene is associated<br />
with MS in DR4- and DR5-positive Italians and Russians. Neurology<br />
2003, 61 : 520-526.<br />
[86] Gurer YK, Kukner S, Kunak B et al. Congenital ocular motor apraxia in<br />
two siblings. Pediatr Neurol 1995, 13 : 261-262.<br />
[87] Gutowski NJ. Duane’s syndrome. Eur J Neurol 2000, 7 : 145-149.<br />
[88] Haegert DG, Cowan T, Murray TJ et al. Does a shift in the T-cell receptor<br />
repertoire precede the onset of MS ? Neurology 1999, 53 : 485-490.<br />
[89] Hanson M, Lupski JR, Hicks J et al. Association of dermal melanocytosis<br />
with lysosomal storage disease : clinical features and hypotheses regarding<br />
pathogenesis. Arch Dermatol 2003, 139 : 916-920.<br />
[90] Haritoglou C, Hoops J, Stefani F et al. Histopathological abnormalities in<br />
ocular blood vessels of CADASIL patients. Am J Ophthalmol 2004, 138 :<br />
302-305.<br />
[91] Harris CM, Hodgkins PR, Kriss A et al. Familial congenital saccade initiation<br />
failure and isolated cerebellar vermis hypoplasia. Dev Med Child<br />
Neurol 1998, 40 : 775-779.<br />
[92] Harris DJ, Memmen JE, Katz NN, Parks MM. Familial congenital superior<br />
oblique palsy. Ophthalmology 1986, 93 : 88-90.<br />
[93] Hayes A, Costa T, Polomeno RC. The Okihiro syndrome of Duane anomaly,<br />
radial ray abnormalities, and deafness. Am J Med Genet 1985, 22 :<br />
273-280.<br />
[94] Hoag HM, Taylor SA, Duncan AM et al. Evidence that skewed X inactivation<br />
is not needed for the phenotypic expression of Aicardi syndrome.<br />
Hum Genet 1997, 100 : 459-464.
Livre.book Page 433 Jeudi, 26. février 2009 3:40 15<br />
[95] Holmes SE, O’Hearn E, Rosenblatt A et al. A repeat expansion in the<br />
gene encoding junctophilin-3 is associated with Huntington disease-like<br />
2. Nat Genet 2001, 29 : 377-378.<br />
[96] Hsu HN, Yang ML, Lai HC. Familial congenital ocular motor apraxia.<br />
Chang Gung Med J 2002, 25 : 411-414.<br />
[97] Hund E, Grau A, Fogel W et al. Progressive cerebellar ataxia, proximal<br />
neurogenic weakness and ocular motor disturbances : hexosaminidase A<br />
deficiency with late clinical onset in four siblings. J Neurol Sci 1997, 145 :<br />
25-31.<br />
[98] Iannaccone A, McIntosh N, Ciccarelli ML et al. Familial unilateral Brown<br />
Syndrome. Ophthalmic Genetic 2002, 23 : 175-184.<br />
[99] Inoue K, Osaka H, Thurston VC et al. Genomic rearrangements resulting<br />
in PLP1 deletion occur by nonhomologous end joining and cause different<br />
dysmyelinating phenotypes In males and females. Am J Hum Genet<br />
2002, 71 : 838-853.<br />
[100] Jiang Y, Matsuo T, Fujiwara H et al. ARIX gene polymorphisms in<br />
patients with congenital superior oblique muscle palsy. Br J Ophthalmol<br />
2004, 88 : 263-267.<br />
[101] Johnson AB. Alexander disease : a review and the gene. Int J Dev Neurosci<br />
2002, 20 : 391-394.<br />
[102] Johnson WG, Wigger HJ, Karp HR et al. Juvenile spinal muscular atrophy<br />
: a new hexosaminidase deficiency phenotype. Ann Neurol 1982, 11 :<br />
11-16.<br />
[103] Joutel A, Corpechot C, Ducros A et al. Notch3 mutations in CADASIL, a<br />
hereditary adult-onset condition causing stroke and dementia. Nature<br />
1996, 383 : 707-710.<br />
[104] Joutel A, Favrole P, Labauge P et al. Skin biopsy immunostaining with a<br />
Notch3 monoclonal antibody for CADASIL diagnosis. Lancet 2001, 358 :<br />
2049-2051.<br />
[105] Joutel A, Monet M, Domenga V et al. Pathogenic mutations associated<br />
with cerebral autosomal dominant arteriopathy with subcortical infarcts<br />
and leukoencephalopathy differently affect Jagged1 binding and Notch3<br />
activity via the RBP/JK signaling Pathway. Am J Hum Genet 2004, 74 :<br />
338-347.<br />
[106] Kan SH, Elanko N, Johnson D et al. Genomic screening of fibroblast<br />
growth-factor receptor 2 reveals a wide spectrum of mutations in<br />
patients with syndromic craniosynostosis. Am J Hum Genet 2002, 70 :<br />
472-486.<br />
[107] Katz LC, Shatz CJ. Synaptic activity and the construction of cortical circuits.<br />
Science 1996, 274 : 1133-1138.<br />
[108] Keeler LC, Marsh SE, Leeflang EP et al. Linkage analysis in families with<br />
Joubert syndrome plus oculorenal involvement identifies the CORS2<br />
locus on chromosome 11p12-q13.3. Am J Hum Genet 2003, 73 : 656-662.<br />
[109] Kerrison JB, Giorda R, Lenart TD et al. Clinical and genetic analysis of a<br />
family with X-linked congenital nystagmus (NYS1). Ophthalmic Genet<br />
2001, 22 : 241-248.<br />
[110] Kerrison JB, Koenekoop RK, Arnould VJ et al. Clinical features of autosomal<br />
dominant congenital nystagmus linked to chromosome 6p12. Am J<br />
Ophthalmol 1998, 125 : 64-70.<br />
[111] Kim J-H, Hwang J-M, Hwang YS et al. Childhood ocular myasthenia gravis.<br />
Ophthalmology 2003, 110 : 1458-1462.<br />
[112] Kirath H, Erdener U. Poland-Mœbius syndrome : a case report. Jpn J<br />
Ophthalmol 2000, 44 : 679-682.<br />
[113] Klein C, Vieregge P, Heide W et al. Exclusion of chromosome regions<br />
6p12 and 15q11, but not chromosome region 7p11, in a German family<br />
with autosomal dominant congenital nystagmus. Genomics 1998, 54 :<br />
176-177.<br />
[114] Kooy RF, Van der Veen AY, Verlind E et al. Physical localisation of the<br />
chromosomal marker D13S31 places the Wilson disease locus at the<br />
junction of bands q14.3 and q21.1 of chromosome 13. Hum Genet 1993,<br />
91 : 504-506.<br />
[115] Kremer H, Kuyt LP, Van Den Helm B et al. Localization of a gene for<br />
Mobius syndrome to chromosome 3q by linkage analysis in a Dutch<br />
family. Hum Mol Genet 1996, 5 : 1367-1371.<br />
[116] Kristiansen OP, Larsen ZM, Pociot F. CTLA-4 in autoimmune diseases –<br />
a general susceptibility gene to autoimmunity ? Genes Immun 2000, 1 :<br />
170-184.<br />
[117] Leyne M, Mull J, Gill SP et al. Identification of the first non-Jewish mutation<br />
in familial Dysautonomia. Am J Med Genet 2003, 118A : 305-308.<br />
[118] Lipson AH, Webster WS, Brown-Woodman PD et al. Mœbius syndrome<br />
: animal model--human correlations and evidence for a brainstem<br />
vascular etiology. Teratology 1989, 40 : 339-350.<br />
[119] Lorenz B. Genetics of isolated and syndromic strabismus : facts and<br />
perspectives. Strabismus 2002, 10 : 147-156.<br />
[120] Lui F, Fonda S, Merlini L et al. Saccadic eye movements are impaired in<br />
Duchenne muscular dystrophy. Doc Ophthalmol 2001, 103 : 219-228.<br />
[121] MacDermot KD, Winter RM, Taylor D et al. Oculofacialbulbar palsy in<br />
mother and son : review of 26 reports of familial transmission within the<br />
‘Mobius spectrum of defects’. J Med Genet 1991, 28 : 18-26.<br />
[122] Mackey DA, Chan WM, Chan C et al. Congenital fibrosis of the vertically<br />
acting extraocular muscles maps to the FEOM3 locus. Hum Genet<br />
2002, 110 : 510-512.<br />
[123] Magli A, De Berardinis T, D’Esposito F et al. Clinical and surgical data of<br />
affected members of a classi CFEOM I famili. BMC Ophthalmology 2003,<br />
3 : 6.<br />
[124] Manning FJ, Bruce AM, Berson EL. Electroretinograms in microcephaly<br />
with chorioretinal degeneration. Am J Ophthalmol 1990, 109 : 457-463.<br />
[125] Marsac C, Benelli C, Desguerre I et al. Biochemical and genetic studies of<br />
four patients with pyruvate dehydrogenase E1 alpha deficiency. Hum<br />
Genet 1997, 99 : 785-792.<br />
[126] Martidis A, Yee RD, Azzarelli B et al. Neuro-ophthalmic, radiographic,<br />
and pathologic manifestations of adult-onset Alexander disease. Arch<br />
Ophthalmol 1999, 117 : 265-267.<br />
[127] Massin M, Drouard E. Contribution à l’étude des strabismes concomitants<br />
familiaux. Ann Ocul (Paris) 1965, 198 : 323.<br />
[128] Matsuo T, Yamane T, Ohtsuki H. Heredity versus abnormalities in pregnancy<br />
and delivery as risk factors for different types of comitant strabismus.<br />
J Pediatr Ophthalmol Strabismus 2001, 38 : 78-82.<br />
[129] Matthews PM, Marchington DR, Squier M et al. Molecular genetic characterization<br />
of an X-linked form of Leigh’s syndrome. Ann Neurol 1993,<br />
33 : 652-655.<br />
[130] Maumenee IH, Alston A, Mets M B et al. Inheritance of congenital esotropia.<br />
Trans Am Ophthalmol Soc 1986, 84 : 85-93.<br />
[131] McMullan TF, Tyers AG. X linked dominant congenital isolated bilateral<br />
ptosis : the definition and characterisation of a new condition. Br J<br />
Ophthalmol 2001, 85 : 70-73.<br />
[132] McMullan TW, Crolla JA, Gregory SG et al. A candidate gene for congenital<br />
bilateral isolated ptosis identified by molecular analysis of a de<br />
novo balanced translocation. Hum Genet 2002, 110 : 244-250.<br />
[133] McQuillen PS, De<strong>fr</strong>eitas MF, Zada G et al. A novel role for p75NTR in<br />
subplate growth cone complexity and visual thalamocortical innervation.<br />
J Neurosci 2002, 22 : 3580-3593.<br />
[134] Mellott ML, Brown J, Jr., Fingert JH et al. Clinical characterization and<br />
linkage analysis of a family with congenital X-linked nystagmus and<br />
deuteranomaly. Arch Ophthalmol 1999, 117 : 1630-1633.<br />
[135] Michaelides M, Moore AT. The genetics of strabismus. J Med Genet<br />
2004, 41 : 641-646.<br />
[136] Middleton LT, Ohno K, Christodoulou K et al. Chromosome 17p-linked<br />
myasthenias stem <strong>fr</strong>om defects in the acetylcholine receptor ε-subunit<br />
gene. Neurology 1999, 53 : 1076.<br />
[137] Miller NR, Kiel SM, Green W R et al. Unilateral Duane’s retraction syndrome<br />
(Type 1). Arch Ophthalmol 1982, 100 : 1468-1472.<br />
[138] Mimault C, Giraud G, Courtois V et al. Proteolipoprotein gene analysis<br />
in 82 patients with sporadic Pelizaeus-Merzbacher Disease : duplications,<br />
the major cause of the disease, originate more <strong>fr</strong>equently in male<br />
germ cells, but point mutations do not. The Clinical European Network<br />
on Brain Dysmyelinating Disease. Am J Hum Genet 1999, 65 : 360-369.<br />
[139] Miterski B, Sindern E, Haupts M et al. PTPRC (CD45) is not associated<br />
with multiple sclerosis in a large cohort of German patients. BMC Med<br />
Genet 2002, 3 : 3.<br />
[140] Mootha VK, Lepage P, Miller K et al. Identification of a gene causing<br />
human cytochrome c oxidase deficiency by integrative genomics. Proc<br />
Natl Acad Sci USA 2003, 100 : 605-610.<br />
[141] Moreira MC, Barbot C, Tachi N et al. Homozygosity mapping of Portuguese<br />
and Japanese forms of ataxia-oculomotor apraxia to 9p13, and evidence<br />
for genetic heterogeneity. Am J Hum Genet 2001, 68 : 501-508.<br />
[142] Moreira MC, Barbot C, Tachi N et al. The gene mutated in ataxia-ocular<br />
apraxia 1 encodes the new HIT/Zn-finger protein aprataxin. Nat Genet<br />
2001, 29 : 189-193.<br />
[143] Mower AF, Lioa DS, Nestler EJ et al. CAMP/Ca2 + response elementbinding<br />
protien function is essential for ocular dominance plasticity. J<br />
Neurosci 2002, 22 : 2237-2245.<br />
[144] Mugikura S, Takahashi S, Higano S et al. MR findings in Tay-Sachs<br />
disease. J Comput Assist Tomogr 1996, 20 : 551-555.<br />
[145] Mullaney P, Vajsar J, Smith R et al. The natural history and ophthalmic<br />
involvement in childhood myasthenia gravis at the hospital for sick children.<br />
Ophthalmology 2000, 107 : 504-510.<br />
[146] Nagashima T, Mori M, Katayama K et al. Adult Leigh syndrome with<br />
mitochondrial DNA mutation at 8993. Acta Neuropathol (Berl) 1999, 97 :<br />
416-422.<br />
[147] Naito E, Ito M, Yokota I et al. Biochemical and molecular analysis of an<br />
X-linked case of Leigh syndrome associated with thiamin-responsive<br />
pyruvate dehydrogenase deficiency. J Inherit Metab Dis 1997, 20 : 539-<br />
548.<br />
[148] Nakano M, Yamada K, Fain J et al. Homozygous mutations in ARIX<br />
(PHOX2A) result in congenital fibrosis of the extraocular muscles type 2.<br />
Nat Genet 2001, 29 : 315-320.<br />
[149] Nanduri VR, Stanhope R. Why is the retention of gonadotrophin secretion<br />
common in children with panhypopituitarism due to septo-optic<br />
dysplasia. Eur J Endocrinol 1999, 140 : 48-50.<br />
[150] Natacci F, Corrado L, Pierri M et al. Patient with large 17p11.2 deletion<br />
presenting with Smith-Magenis syndrome and Joubert syndrome phenotype.<br />
Am J Med Genet 2000, 95 : 467-472.<br />
[151] Neilson DE, Eiben RM, Waniewski S et al. Autosomal dominant acute<br />
necrotizing encephalopathy. Neurology 2003, 61 : 226-230.<br />
[152] Nishikawa M, Ichiyama T, Hayashi T et al. Mobius-like syndrome associated<br />
with a 1 ;2 chromosome translocation. Clin Genet 1997, 51 : 122-<br />
123.<br />
[153] O’Brien KF, Engle E Ckunkel LM. Analysis of human sarcospan as a<br />
condidate gene for CFEOM1. BMC Genet 2001, 2 : 3.<br />
[154] O’Dowd BF, Klavins MH, Willard HF et al. Molecular heterogeneity in<br />
the infantile and juvenile forms of Sandhoff disease (O-variant GM2<br />
gangliosidosis). J Biol Chem 1986, 261 : 12680-12685.<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 433
Livre.book Page 434 Jeudi, 26. février 2009 3:40 15<br />
[155] Oddoux C, Reich E, Axelrod F et al. Prenatal diagnostic testing for familial<br />
dysautonomia using linked genetic markers. Prenat Diagn 1995, 15 :<br />
817-826.<br />
[156] Oetting WS, Armstrong CM, Holleschau AM et al. Evidence for genetic<br />
heterogeneity in families with congenital motor nystagmus (CN).<br />
Ophthalmic Genet 2000, 21 : 227-233.<br />
[157] Ogawa Y, Naito E, Ito M et al. Three novel SURF-1 mutations in Japanese<br />
patients with Leigh syndrome. Pediatr Neurol 2002, 26 : 196-200.<br />
[158] Ohno K, Engel AG, Brengman JM et al. The spectrum of mutations causing<br />
end-plate acetylcholinesterase deficiency. Ann Neurol 2000, 47 : 162-<br />
170.<br />
[159] Ohno K, Tsujino A, Brengman JM et al. Choline acetyltransferase mutations<br />
cause myasthenic syndrome associated with episodic apnea in<br />
humans. Proc Natl Acad Sci USA 2001, 98 : 2017-2022.<br />
[160] Ohno K, Engel AG, Shen XM et al. Rapsyn mutations in humans cause<br />
endplate acetylcholine-receptor deficiency and myasthenic syndrome.<br />
Am J Hum Genet 2002, 70 : 875-885.<br />
[161] Orbeck H, Oftedal G. Familial dysautonomia in a non-Jewish child. Acta<br />
Paediatr Scand 1977, 66 : 777-781.<br />
[162] Osanai R, Kinoshita M, Hirose K. Saccadic slowing in myotonic dystrophy<br />
and CTG repeat expansion. J Neurol 1998, 245 : 674-680.<br />
[163] Oster SF, Sretavan DW. Connecting the eye to the brain : the molecular<br />
basis of ganglion cell axon guidance. Br J Ophthalmol 2003 ; 87 : 639-645.<br />
[164] Ozkara Hsandhoff K. A new point mutation (G412 to A) at the last<br />
nucleotide of exon 3 of hexosaminidase alpha-subunit gene affects splicing.<br />
Brain Dev 2003, 25 : 203-206.<br />
[165] Ozkurt H, Basak M, Oral Y et al. Magnetic resonance imaging in<br />
Duane’s retraction syndrome. J Pediatr Ophthalmol Strabismus 2003, 40 :<br />
19-22.<br />
[166] Parfait B, Chretien D, Rotig A et al. Compound heterozygous mutations<br />
in the flavoprotein gene of the respiratory chain complex II in a patient<br />
with Leigh syndrome. Hum Genet 2000, 106 : 236-243.<br />
[167] Parikh V, Shugart YY, Doheny KF et al. A strabismus susceptibility locus<br />
on chromosome 7p. Proc Natl Acad Sci USA 2003 ; 100 : 12283-12288.<br />
[168] Pattyn A, Morin X, Cremer H et al. Expression and interactions of the<br />
two closely related homoebox genes Phox2a and phox2b during neurogenesis.<br />
Development 1997, 124 : 4065-4075.<br />
[169] Paul T, Ohardage LK. The heritability of strabismus. Ophthalmic Genet<br />
1994, 15 : 1-18.<br />
[170] Pennybacker M, Liessem B, Moczall H et al. Identification of domains in<br />
human beta-hexosaminidase that determine substrate specificity. J Biol<br />
Chem 1996, 271 : 17377-17382.<br />
[171] Pequignot MO, Desguerre I, Dey R et al. New splicing-site mutations in<br />
the SURF1 gene in Leigh syndrome patients. J Biol Chem 2001, 276 :<br />
15326-15329.<br />
[172] Petruzzella V, Vergari R, Puzziferri I et al. A nonsense mutation in the<br />
NDUFS4 gene encoding the 18 kDa (AQDQ) subunit of complex I abolishes<br />
assembly and activity of the complex in a patient with Leigh-like<br />
syndrome. Hum Mol Genet 2001, 10 : 529-535.<br />
[173] Pham YC, Man N, Lam LT et al. Localization of myotonic dystrophy<br />
protein kinase in human and rabbit tissues using a new panel of monoclonal<br />
antibodies. Hum Mol Genet 1998, 7 : 1957-1965.<br />
[174] Phillips HE, Carter AP, Kennedy JL, JR. et al. Aicardi’s syndrome ; radiologic<br />
manifestations. Radiology 1978, 127 : 453-455.<br />
[175] Phillips PH, Brodsky M, Chenry PM. Congenital ocular motor apraxia<br />
with autosomal dominant inheritance. Am J Ophthalmol 2000, 129 : 820-<br />
822.<br />
[176] Pizzuti A, Calabrese G, Bozzali M et al. Peptidase gene in chromosome<br />
8q is disrupted by a balanced translocation in a duane syndrome patient.<br />
Invest Ophthalmol and Vis Sci 2002, 43 : 3609-3612.<br />
[177] Poorkaj P, Muma NA, Zhukareva V et al. An R5L tau mutation in a subject<br />
with a progressive supranuclear palsy phenotype. Ann Neurol 2002,<br />
52 : 511-516.<br />
[178] Quiram PA, Ohno K, Milone M et al. Mutation causing congenital myasthenia<br />
reveals acetylcholine receptor beta/delta subunit interaction<br />
essential for assembly. J Clin Invest 1999, 104 : 1403-1410.<br />
[179] Ragge NK, Hartley C, Dearlove AM et al. Familial vestibulocerebellar<br />
disorder maps to chromosome 13q31-q33 : a new nystagmus locus. J<br />
Med Genet 2003, 40 : 37-41.<br />
[180] Rahman S, Blok RB, Dahl HH et al. Leigh syndrome : clinical features<br />
and biochemical and DNA abnormalities. Ann Neurol 1996, 39 : 343-351.<br />
[181] Ranum LP, Day JW. Myotonic dystrophy : clinical and molecular parallels<br />
between myotonic dystrophy type 1 and type 2. Curr Neurol Neurosci<br />
Rep 2002, 2 : 465-470.<br />
[182] Reck AC, Manners Rhatchwell E. Phenotypic heterogeneity may occur<br />
in congenital fibrosis of the extraocular muscles. Brit J Ophthal 1998, 82 :<br />
676-679.<br />
[183] Remy C. Strabisme et hérédité. Bull Soc Ophtalmol Fr 1987, 87 : 981.<br />
[184] Renier WO, Gabreels FJ, Hustinx TW et al. Connatal Pelizaeus-Merzbacher<br />
disease with congenital stridor in two maternal cousins. Acta Neuropathol<br />
(Berl) 1981, 54 : 11-17.<br />
[185] Reuter DA, Anetseder M, Muller R et al. The ryanodine contracture test<br />
may help diagnose susceptibility to malignant hyperthermia. Can J<br />
Anaesth 2003, 50 : 643-648.<br />
[186] Rickard S, Parker M, Van’t Hoff W et al. Oto-facio-cervical (OFC) syndrome<br />
is a contiguous gene deletion syndrome involving EYA1 : molecular<br />
analysis confirms allelism with BOR syndrome and further narrows<br />
434 NEUROPATHIES OPTIQUES ET NEURO-OPHTALMOLOGIE<br />
the Duane syndrome critical region to 1 cM. Hum Genet 2001, 108 : 398-<br />
403.<br />
[187] Robinson R, Hopkins P, Carsana A et al. Several interacting genes<br />
influence the malignant hyperthermia phenotype. Hum Genet 2003, 112 :<br />
217-218.<br />
[188] Robles J. Congenital ocular motor apraxia in identical twins. Arch<br />
ophthalmol 1966, 75 : 746-749.<br />
[189] Rubinsztein DC, Leggo J, Coles R et al. Phenotypic characterization of<br />
individuals with 30-40 CAG repeats in the Huntington disease (HD)<br />
gene reveals HD cases with 36 repeats and apparently normal elderly<br />
individuals with 36-39 repeats. Am J Hum Genet 1996, 59 : 16-22.<br />
[190] Sadler LS, Robinson LK. Chorioretinal dysplasia-microcephaly-mental<br />
retardation syndrome : report of an American family. Am J Med Genet.<br />
1993, 47 : 65-68.<br />
[191] Schaffner C, Idler I, Stilgenbauer S et al. Mantle cell lymphoma is characterized<br />
by inactivation of the ATM gene. Proc Natl Acad Sci USA 2000,<br />
97 : 2773-2778.<br />
[192] Scott SP, Bendix R, Chen P et al. Missense mutations but not allelic<br />
variants alter the function of ATM by dominant interference in patients<br />
with breast cancer. Proc Natl Acad Sci USA 2002, 99 : 925-930.<br />
[193] Seemungal BM, Faldon M, Revesz T et al. Influence of target size on vertical<br />
gaze palsy in a pathologically proven case of progressive supranuclear<br />
palsy. Mov Disord 2003, 18 : 818-822.<br />
[194] Sener EC, Lee BA, Turgut B et al. A clinically variant fibrosis syndrome<br />
in a Turkish family maps to the CFEOM1 locus on chromosome 12. Arch<br />
Ophthalmol 2000, 118 : 1090-1097.<br />
[195] Sener RN. Septo-optic dysplasia (de Morsier’s syndrome) associated<br />
with total callosal absence. A new type of the anomaly. J Neuroradiol<br />
1996, 23 : 79-81.<br />
[196] Shen XM, Ohno K, Fukudome T et al. Congenital myasthenic syndrome<br />
caused by low-expressor fast-channel AChR δ subunit mutation. Neurology<br />
2002, 59 : 1881-1888.<br />
[197] Shen XM, Ohno K, Tsujino A et al. Mutation causing severe myasthenia<br />
reveals functional asymmetry of AChR signature cystine loops in agonist<br />
binding and gating. J Clin Invest 2003, 111 : 497-505.<br />
[198] Slaugenhaupt SA, Blumenfeld A, Gill SP et al. Tissue-specific expression<br />
of a splicing mutation in the IKBKAP gene causes familial dysautonomia.<br />
Am J Hum Genet 2001, 68 : 598-605.<br />
[199] Slee JJ, Smart R Dviljoen DL. Deletion of chromosome 13 in Mœbius<br />
syndrome. J Med Genet 1991, 28 : 413-414.<br />
[200] Solomon D, Shepard N, Mishra A. Congenital periodic alternating nystagmus<br />
: response to baclofen. Ann N Y Acad Sci 2002, 956 : 611-615.<br />
[201] Sperl W, Bart G, Vanier MT et al. A family with visceral course of Niemann-Pick<br />
disease, macular halo syndrome and low sphingomyelin<br />
degradation rate. J Inherit Metab Dis 1994, 17 : 93-103.<br />
[202] Tajima T, Hattorri T, Nakajima T et al. Sporadic heterozygous <strong>fr</strong>ameshift<br />
mutation of HESX1 causing pituitary and optic nerve hypoplasia<br />
and combined pituitary hormone deficiency in a Japanese patient. J Clin<br />
Endocrinol Metab 2003, 88 : 45-50.<br />
[203] Takano K, Nakamoto T, Okajima M et al. Cerebellar and brainstem<br />
involvement in familial juvenile nephronophthisis type I. Pediatr Neurol<br />
2003, 28 : 142-144.<br />
[204] Taylor RW, Morris AA, Hutchinson M et al. Leigh disease associated<br />
with a novel mitochondrial DNA ND5 mutation. Eur J Hum Genet 2002,<br />
10 : 141-144.<br />
[205] Temtamy SA, Shoukry AS, Ghaly I et al. The Duane radial dysplasia<br />
syndrome : an autosomal dominant disorder. Birth Defects Orig. Art Ser<br />
1975 ;XI :344-345.<br />
[206] Thomas PQ, Dattani MT, Brickman JM et al. Heterozygous HESX1<br />
mutations associated with isolated congenital pituitary hypoplasia and<br />
septo-optic dysplasia. Hum Mol Genet 2001, 10 : 39-45.<br />
[207] Thorn F. Development of re<strong>fr</strong>action and strabismus. Curr Opin Ophthalmol<br />
2000, 11 : 301-305.<br />
[208] Tiranti V, Munaro M, Sandona D et al. Nuclear DNA origin of cytochrome<br />
c oxidase deficiency in Leigh’s syndrome : genetic evidence<br />
based on patient’s-derived rho(0) transformants. Hum Molec Genet 1995,<br />
4 : 2017-2023.<br />
[209] Tiranti V, Jaksch M, Hofmann S et al. Loss-of-function mutations of<br />
SURF-1 are specifically associated with Leigh syndrome with cytochrome<br />
c oxidase deficiency. Ann Neurol 1999, 46 : 161-166.<br />
[210] Tokita N, Sekhar HK, Sachs M et al. Familial dysautonomia (Riley-Day<br />
syndrome). Temporal bone findings and otolaryngological manifestations.<br />
Ann Otol Rhinol Laryngol Suppl 1978, 87 : 1-12.<br />
[211] Traboulsi EI, Lee BA, Mousawi A et al. Evidence of genetic heterogeneity<br />
in autosomal recessive congenital fibrosis of the extraocular muscles. Am<br />
J Ophthalmol 2000, 129 : 658-662.<br />
[212] Trifiletti RR, Incorpora G, Polizzi A et al. Aicardi syndrome with multiple<br />
tumors : a case report with literature review. Brain Dev 1995, 17 :<br />
283-285.<br />
[213] Trottier Y, Biancalana V, Mandel JL. Instability of CAG repeats in Huntington’s<br />
disease : relation to parental transmission and age of onset. J<br />
Med Genet 1994, 31 : 377-382.<br />
[214] Tsai FJ, Peng CT, Tsai CH et al. Niemann-Pick disease type B with ocular<br />
involvement : report of a case. Zhonghua Min Guo Xiao Er Ke Yi Xue Hui<br />
Za Zhi 1991, 32 : 177-182.<br />
[215] Tsao CY, Mendell JR, Lo WD et al. Myasthenia gravis and associated<br />
autoimmune diseases in children. J Child Neurol 2000, 15 : 767-769.
Livre.book Page 435 Jeudi, 26. février 2009 3:40 15<br />
[216] Uhlenberg B, Schuelke M, Ruschendorf F, et al. Mutations in the gene<br />
encoding gap junction protein alpha-12 (connexin 46.6) cause Pelizaeus-<br />
Merzbacher-like disease. Am J Hum Genet 2004, 75 : 251-260.<br />
[217] Vahedi K, Chabriat H, Levy C et al. Migraine with aura and brain<br />
magnetic resonance imaging abnormalities in patients with CADASIL.<br />
Arch Neurol 2004, 61 : 1237-1240.<br />
[218] Valente EM, Salpietro DC, Brancati F et al. Description, nomenclature,<br />
and mapping of a novel cerebello-renal syndrome with the molar tooth<br />
malformation. Am J Hum Genet 2003, 73 : 663-670.<br />
[219] Van Coster R, Seneca S, Smet J et al. Homozygous Gly555Glu mutation<br />
in the nuclear-encoded 70 kDa flavoprotein gene causes instability of the<br />
respiratory chain complex II. Am J Med Genet 2003, 120A :13-18.<br />
[220] Vanier MT, Millat G. Niemann-Pick disease type C. Clin Genet 2003, 64 :<br />
269-281.<br />
[221] Varani L, Hasegawa M, Spillantini MG et al. Structure of tau exon 10<br />
splicing regulatory element RNA and destabilization by mutations of<br />
<strong>fr</strong>ontotemporal dementia and parkinsonism linked to chromosome 17.<br />
Proc Natl Acad Sci USA 1999, 96 : 8229-8234.<br />
[222] Versino M, Rossi B, Beltrami G et al. Ocular motor myotonic phenomenon<br />
in myotonic dystrophy. J Neurol Neurosurg Psychiatry 2002, 72 : 236-<br />
240.<br />
[223] Verzijl HT, Van Den Helm B, Veldman B et al. A second gene for autosomal<br />
dominant Mobius syndrome is localized to chromosome 10q, in a<br />
Dutch family. Am J Hum Genet 1999, 65 : 752-756.<br />
[224] Vincent C, Kalatzis V, Abdelhak S et al. BOR and BO syndromes are allelic<br />
defects of EYA1. Eur J Hum Genet 1997, 5 : 242-246.<br />
[225] Walton DS, Robb R Mcrocker AC. Ocular manifestations of group A<br />
Niemann-Pick disease. Am J Ophthalmol 1978, 85 : 174-180.<br />
[226] Wang HL, Milone M, Ohno K et al. Acetylcholine receptor M3 domain :<br />
stereochemical and volume contributions to channel gating. Nat Neurosci<br />
1999, 2 : 226-233.<br />
[227] Wang SM, Zwaan J, Mullaney PB et al. Congenital fibrosis of the extraocular<br />
muscles type 2, an inherited exotropic strabismus fixus, maps to<br />
distal 11q13. Am J Hum Genet 1998, 63 : 517-525.<br />
[228] Wilmore HP, Smith MJ, Wilcox S A et al. SOX14 is a candidate gene for<br />
limb defects associated with BPES and Mobius syndrome. Hum Genet<br />
2000, 106 : 269-276.<br />
[229] Winograd-Gurvich CT, Georgiou-Karistianis N, Evans A et al. Hypometric<br />
primary saccades and increased variability in visually-guided saccades<br />
in Huntington’s disease. Neuropsychologia 2003, 41 : 1683-1692.<br />
[230] Wu ZY, Lin MT, Murong SX et al. Molecular diagnosis and prophylactic<br />
therapy for presymptomatic Chinese patients with Wilson disease. Arch<br />
Neurol 2003, 60 : 737-741.<br />
[231] Yamanaka S, Johnson M, Grinberg A et al. Targeted disruption of the<br />
Hexa gene results in mice with biochemical and pathologic features of<br />
Tay-Sachs disease. Proc Natl Acad Sci USA 1994, 91 : 9975-9979.<br />
[232] Yamaya Y, Yoshioka A, Shirakawa T et al. Apraxia of eyelid closure in a<br />
patient with progressive supranuclear palsy. Rinsho Shinkeigaku 1999,<br />
39 : 940-943.<br />
[233] Zhu Z, Yao J, Johns T et al. SURF1, encoding a factor involved in the biogenesis<br />
of cytochrome c oxidase, is mutated in Leigh syndrome. Nat<br />
Genet 1998, 20 : 337-343.<br />
[234] Ziakas NG, Woodruff G, Smith LK et al. A study of heredity as a risk<br />
factor in strabismus. Eye 2002, 16 : 519-521.<br />
[235] Ziter FA, Wiser W, Crobinson A. Three-generation pedigree of a Mobius<br />
syndrome variant with chromosome translocation. Arch Neurol 1977, 34 :<br />
437-442.<br />
[236] Zuccato C, Ciammola A, Rigamonti D et al. Loss of huntingtin-mediated<br />
BDNF gene transcription in Huntington’s disease. Science 2001, 293 :<br />
493-498.<br />
STRABISME, MYOPATHIES, NEURO-OPHTALMOLOGIE 435
Livre.book Page 436 Jeudi, 26. février 2009 3:40 15