Energia libera - Università degli Studi di Salerno
Energia libera - Università degli Studi di Salerno
Energia libera - Università degli Studi di Salerno
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
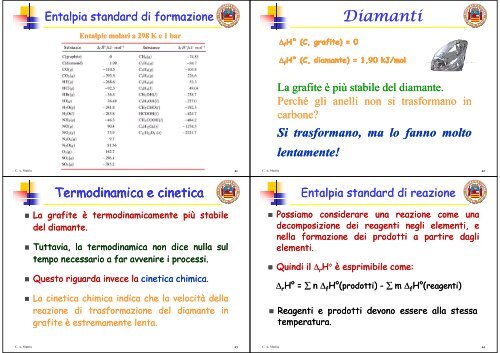
Entalpia p standard <strong>di</strong> formazione<br />
Entalpie molari a 298 K e 1 bar<br />
C. A. Mattia 41<br />
Termo<strong>di</strong>namica e cinetica<br />
La grafite è termo<strong>di</strong>namicamente più stabile<br />
del <strong>di</strong>amante <strong>di</strong>amante.<br />
Tuttavia, la termo<strong>di</strong>namica non <strong>di</strong>ce nulla sul<br />
tempo necessario afar far avvenire i processi processi.<br />
Questo riguarda invece la cinetica chimica chimica.<br />
La cinetica chimica in<strong>di</strong>ca che la velocità della<br />
reazione <strong>di</strong> trasformazione del <strong>di</strong>amante in<br />
grafite è estremamente lenta. lenta<br />
C. A. Mattia 43<br />
fH fH H° (C (C, (C, grafite) grafite) = = 0<br />
Diamanti<br />
fH fH H° (C (C, (C, <strong>di</strong>amante) <strong>di</strong>amante) = 1 1,90 90 kJ/mol<br />
La grafite è più stabile del <strong>di</strong>amante.<br />
Perché P PPerché hé gli li anelli lli non si i trasformano f i in<br />
carbone?<br />
Si trasformano, ma lo fanno molto<br />
lentamente!<br />
C. A. Mattia 42<br />
Entalpia p standard <strong>di</strong> reazione<br />
Possiamo considerare una reazione come una<br />
decomposizione dei reagenti negli elementi, e<br />
nella formazione dei prodotti a partire dagli<br />
elementi elementi.<br />
Quin<strong>di</strong> il rH è esprimibile come:<br />
rH° = n n fH°(prodotti prodotti) ) - m m fH°(reagenti reagenti)<br />
Reagenti e prodotti devono essere alla stessa<br />
temperatura<br />
temperatura.<br />
C. A. Mattia 44