Energia libera - Università degli Studi di Salerno
Energia libera - Università degli Studi di Salerno
Energia libera - Università degli Studi di Salerno
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Cambiamenti <strong>di</strong> fase<br />
bl blH ° subl sublH =<br />
= f H ° = + H °<br />
fus fusH + vap vapH<br />
C. A. Mattia 9<br />
Altri H H standard<br />
Combustione cHH°<br />
Ionizzazione ion<br />
ionH° ionH<br />
Idratazione hyd<br />
hydH° hyd<br />
Miscelazione mix<br />
E altri …<br />
mixH°<br />
Il H° delle transizioni <strong>di</strong> fase è comodo<br />
riportarlo i l alla ll temperatura a cui i avviene i la l<br />
transizione.<br />
C. A. Mattia 11<br />
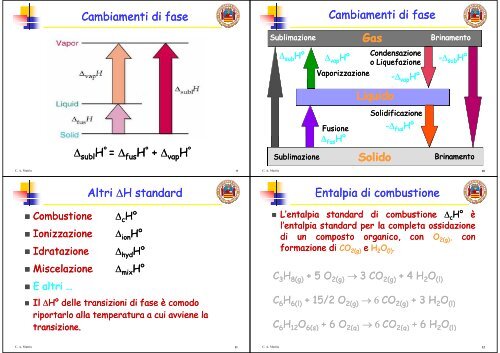
Cambiamenti <strong>di</strong> fase<br />
Gas<br />
Sublimazione Brinamento<br />
Condensazione<br />
vapH<br />
o Li Liquefazione f i<br />
Vaporizzazione<br />
sub subH° sub vap vapH° vap<br />
- sub subH° sub subH<br />
Fusione<br />
fus fusH° H°<br />
Liquido<br />
- vap vapH° vap vapH<br />
Soli<strong>di</strong>ficazione<br />
S Solido lid<br />
- fus fusH°<br />
S Sublimazione bli i<br />
Bi Brinamento t<br />
C. A. Mattia 10<br />
Entalpia p <strong>di</strong> combustione<br />
L’entalpia Lentalpia standard <strong>di</strong> combustione cH° cH è<br />
l’entalpia standard per la completa ossidazione<br />
<strong>di</strong> un composto organico organico, con O O2(g) (g), con<br />
formazione <strong>di</strong> CO<br />
CO2(g) (g) e H2O (l) (l).<br />
C C3HH 8(g) + 5 O 2(g) 3 3 CO 2(g) + 4 H H2O O (l)<br />
C6H 6(l) + 15/2 O O2(g) C6H12 12O 6(s) + 6 O O2(g) 2(g) CO CO2(g) 2(g) CO CO2(g) 2(g) + 3 H H2O (l)<br />
2(g) + 6 H H2O (l)<br />
C. A. Mattia 12