Energia libera - Università degli Studi di Salerno
Energia libera - Università degli Studi di Salerno
Energia libera - Università degli Studi di Salerno
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
H° a partire dai fH°<br />
r p f<br />
I fH H in kJ/m kJ/mol l sono s n tabulati. tabulati<br />
Al (s) (s)<br />
BaCO<br />
CO (g)<br />
CO 2(g)<br />
CS<br />
S Sostanza t fHH Sostanza fHH <br />
BaCO3(s) 3(s)<br />
CS 2(g)<br />
0<br />
-1219 1219<br />
-110 110<br />
-394 394<br />
+117<br />
Cl 2(g)<br />
H H2O O(ll)<br />
H2O (g)<br />
NaHCO<br />
Na Na2CO NaHCO NaHCO3(s) 3(s) 3(s) 3(s)<br />
CO 3(s)<br />
0<br />
-286 286<br />
-242 242<br />
-947,7 947,7<br />
-1131 1131<br />
Ricordare che i fH H per gli elementi nei loro stati<br />
standard è 0.<br />
C. A. Mattia 45<br />
Variazione rH° con la temperatura<br />
p<br />
r<br />
Le entalpie standard <strong>di</strong> molte importanti<br />
reazioni sono state misurate a varie<br />
temperature e riportate in tabelle tabelle.<br />
In mancanza <strong>di</strong> informazioni informazioni, si possono<br />
calcolare in modo approssimato rH°(T) (T).<br />
L’espressione della variazione <strong>di</strong> entalpia<br />
H ( T<br />
T<br />
2) H ( T1)<br />
<br />
2<br />
T<br />
1<br />
C pdT<br />
C. A. Mattia 47<br />
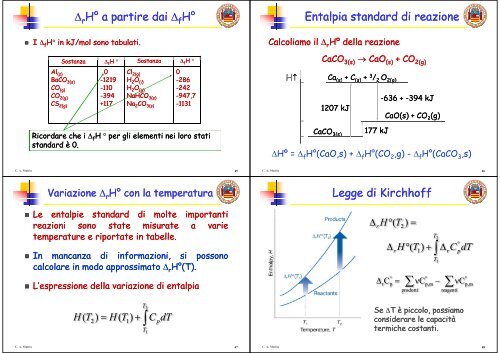
Entalpia p standard <strong>di</strong> reazione<br />
Calcoliamo il rHº Hº della reazione<br />
CaCO 3( 3(s) ) CaO () ()+ (s) + CO CO2(g) 2( 2(g) )<br />
H Ca () ()+ + C () ()+ + 3 H Ca (s) + C (s) + / 2<br />
1207 kJ<br />
CaCO 3(s)<br />
2 O O2(g) 2( 2(g) )<br />
177 kJ<br />
-636 636 + -394 394 kJ<br />
CaO(s) + CO CO2(g) 2(g) (g)<br />
Hº H = fH°(CaO fH (CaO,s) s) + fH°(CO fH (CO22,g) g) - fH°(CaCO fH (CaCO33,s) s)<br />
C. A. Mattia<br />
Legge gg <strong>di</strong> Kirchhoff<br />
<br />
r<br />
H (<br />
T2<br />
) <br />
<br />
C<br />
r<br />
<br />
p<br />
r<br />
T<br />
H (<br />
T1)<br />
<br />
rC<br />
<br />
<br />
prodotti<br />
C<br />
<br />
p,<br />
m<br />
T<br />
2<br />
1<br />
<br />
<br />
reagenti<br />
<br />
p<br />
C<br />
Se T T T T è è piccolo, piccolo possiamo<br />
considerare le capacità<br />
termiche costanti.<br />
C. A. Mattia 48<br />
dT<br />
<br />
p,<br />
m<br />
46