Einsatz von Statinen in der Primärprävention - DIMDI
Einsatz von Statinen in der Primärprävention - DIMDI
Einsatz von Statinen in der Primärprävention - DIMDI
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Der <strong>E<strong>in</strong>satz</strong> <strong>von</strong> <strong>Stat<strong>in</strong>en</strong> <strong>in</strong> <strong>der</strong> <strong>Primärprävention</strong><br />
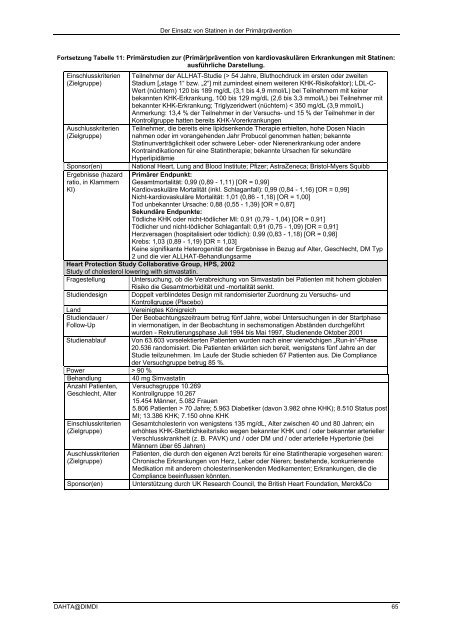
Fortsetzung Tabelle 11: Primärstudien zur (Primär)prävention <strong>von</strong> kardiovaskulären Erkrankungen mit <strong>Stat<strong>in</strong>en</strong>:<br />
ausführliche Darstellung.<br />
E<strong>in</strong>schlusskriterien<br />
(Zielgruppe)<br />
Auschlusskriterien<br />
(Zielgruppe)<br />
Teilnehmer <strong>der</strong> ALLHAT-Studie (> 54 Jahre, Bluthochdruck im ersten o<strong>der</strong> zweiten<br />
Stadium [„stage 1“ bzw. „2“] mit zum<strong>in</strong>dest e<strong>in</strong>em weiteren KHK-Risikofaktor); LDL-C-<br />
Wert (nüchtern) 120 bis 189 mg/dL (3,1 bis 4,9 mmol/L) bei Teilnehmern mit ke<strong>in</strong>er<br />
bekannten KHK-Erkrankung, 100 bis 129 mg/dL (2,6 bis 3,3 mmol/L) bei Teilnehmer mit<br />
bekannter KHK-Erkrankung; Triglyzeridwert (nüchtern) < 350 mg/dL (3,9 mmol/L)<br />
Anmerkung: 13,4 % <strong>der</strong> Teilnehmer <strong>in</strong> <strong>der</strong> Versuchs- und 15 % <strong>der</strong> Teilnehmer <strong>in</strong> <strong>der</strong><br />
Kontrollgruppe hatten bereits KHK-Vorerkrankungen<br />
Teilnehmer, die bereits e<strong>in</strong>e lipidsenkende Therapie erhielten, hohe Dosen Niac<strong>in</strong><br />
nahmen o<strong>der</strong> im vorangehenden Jahr Probucol genommen hatten; bekannte<br />
Stat<strong>in</strong>unverträglichkeit o<strong>der</strong> schwere Leber- o<strong>der</strong> Nierenerkrankung o<strong>der</strong> an<strong>der</strong>e<br />
Kontra<strong>in</strong>dikationen für e<strong>in</strong>e Stat<strong>in</strong>therapie; bekannte Ursachen für sekundäre<br />
Hyperlipidämie<br />
Sponsor(en) National Heart, Lung and Blood Institute; Pfizer; AstraZeneca; Bristol-Myers Squibb<br />
Ergebnisse (hazard<br />
ratio, <strong>in</strong> Klammern<br />
KI)<br />
Primärer Endpunkt:<br />
Gesamtmortalität: 0,99 (0,89 - 1,11) [OR = 0,99]<br />
Kardiovaskuläre Mortalität (<strong>in</strong>kl. Schlaganfall): 0,99 (0,84 - 1,16) [OR = 0,99]<br />
Nicht-kardiovaskuläre Mortalität: 1,01 (0,86 - 1,18) [OR = 1,00]<br />
Tod unbekannter Ursache: 0,88 (0,55 - 1,39) [OR = 0,87]<br />
Sekundäre Endpunkte:<br />
Tödliche KHK o<strong>der</strong> nicht-tödlicher MI: 0,91 (0,79 - 1,04) [OR = 0,91]<br />
Tödlicher und nicht-tödlicher Schlaganfall: 0,91 (0,75 - 1,09) [OR = 0,91]<br />
Herzversagen (hospitalisiert o<strong>der</strong> tödlich): 0,99 (0,83 - 1,18) [OR = 0,98]<br />
Krebs: 1,03 (0,89 - 1,19) [OR = 1,03]<br />
Ke<strong>in</strong>e signifikante Heterogenität <strong>der</strong> Ergebnisse <strong>in</strong> Bezug auf Alter, Geschlecht, DM Typ<br />
2 und die vier ALLHAT-Behandlungsarme<br />
Heart Protection Study Collaborative Group, HPS, 2002<br />
Study of cholesterol lower<strong>in</strong>g with simvastat<strong>in</strong>.<br />
Fragestellung Untersuchung, ob die Verabreichung <strong>von</strong> Simvastat<strong>in</strong> bei Patienten mit hohem globalen<br />
Risiko die Gesamtmorbidität und -mortalität senkt.<br />
Studiendesign Doppelt verbl<strong>in</strong>detes Design mit randomisierter Zuordnung zu Versuchs- und<br />
Kontrollgruppe (Placebo)<br />
Land Vere<strong>in</strong>igtes Königreich<br />
Studiendauer /<br />
Follow-Up<br />
Der Beobachtungszeitraum betrug fünf Jahre, wobei Untersuchungen <strong>in</strong> <strong>der</strong> Startphase<br />
<strong>in</strong> viermonatigen, <strong>in</strong> <strong>der</strong> Beobachtung <strong>in</strong> sechsmonatigen Abständen durchgeführt<br />
wurden - Rekrutierungsphase Juli 1994 bis Mai 1997, Studienende Oktober 2001<br />
Studienablauf Von 63.603 vorselektierten Patienten wurden nach e<strong>in</strong>er vierwöchigen „Run-<strong>in</strong>“-Phase<br />
20.536 randomisiert. Die Patienten erklärten sich bereit, wenigstens fünf Jahre an <strong>der</strong><br />
Studie teilzunehmen. Im Laufe <strong>der</strong> Studie schieden 67 Patienten aus. Die Compliance<br />
<strong>der</strong> Versuchgruppe betrug 85 %.<br />
Power > 90 %<br />
Behandlung 40 mg Simvastat<strong>in</strong><br />
Anzahl Patienten,<br />
Geschlecht, Alter<br />
E<strong>in</strong>schlusskriterien<br />
(Zielgruppe)<br />
Auschlusskriterien<br />
(Zielgruppe)<br />
Versuchsgruppe 10.269<br />
Kontrollgruppe 10.267<br />
15.454 Männer, 5.082 Frauen<br />
5.806 Patienten > 70 Jahre; 5.963 Diabetiker (da<strong>von</strong> 3.982 ohne KHK); 8.510 Status post<br />
MI; 13.386 KHK; 7.150 ohne KHK<br />
Gesamtcholester<strong>in</strong> <strong>von</strong> wenigstens 135 mg/dL, Alter zwischen 40 und 80 Jahren; e<strong>in</strong><br />
erhöhtes KHK-Sterblichkeitsrisiko wegen bekannter KHK und / o<strong>der</strong> bekannter arterieller<br />
Verschlusskrankheit (z. B. PAVK) und / o<strong>der</strong> DM und / o<strong>der</strong> arterielle Hypertonie (bei<br />
Männern über 65 Jahren)<br />
Patienten, die durch den eigenen Arzt bereits für e<strong>in</strong>e Stat<strong>in</strong>therapie vorgesehen waren:<br />
Chronische Erkrankungen <strong>von</strong> Herz, Leber o<strong>der</strong> Nieren; bestehende, konkurrierende<br />
Medikation mit an<strong>der</strong>ern cholester<strong>in</strong>senkenden Medikamenten; Erkrankungen, die die<br />
Compliance bee<strong>in</strong>flussen könnten.<br />
Sponsor(en) Unterstützung durch UK Research Council, the British Heart Foundation, Merck&Co<br />
DAHTA@<strong>DIMDI</strong> 65