في كل مكان
1TsOjdS
1TsOjdS
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
أبحاث<br />
أنباء وآراء<br />
مخ <strong>في</strong><br />
مرحلة النمو<br />
+<br />
خلايا عصبية جذعية<br />
وسل<strong>في</strong>ة مستنبتة<br />
كسر مزدوج<br />
(الفريسة)<br />
كروموسوم<br />
كسر مزدوج<br />
جين كبير منسوخ بش<strong>كل</strong><br />
نشط، وتضاعَ ف مؤخرً ا<br />
كسر<br />
مزدوج<br />
(الط ُّ عم)<br />
ربط<br />
النهايات<br />
عمليات إزفاء<br />
عمليات إعادة ترتيب أخرى<br />
جنين فأر<br />
هل هو اكتساب لوظيفة ما، أم فَ قْ د؟<br />
تداعيات وظي<strong>في</strong>ة<br />
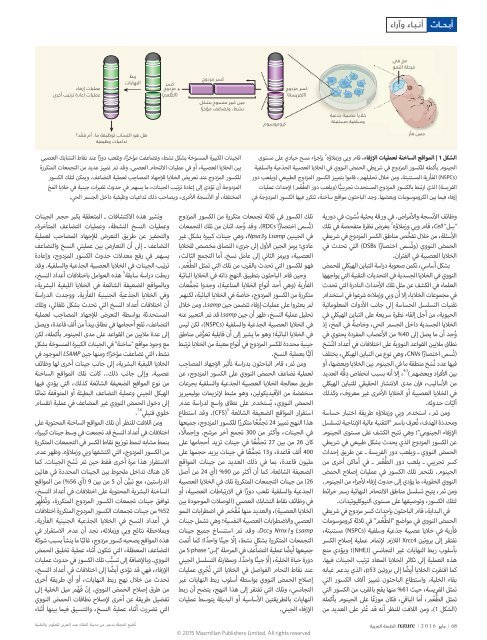
الش<strong>كل</strong> | 1 المواقع الساخنة لعمليات ال زفاء. قام ويي وزمالؤه 2 بإجراء مسح حيادي على مستوى<br />
الجينوم بأكمله للكسور المزدوج <strong>في</strong> شريطي الحمض النووي <strong>في</strong> الخاليا العصبية الجذعية والسل<strong>في</strong>ة<br />
)NSPCs( الفأرية المستنبتة. ومن خالل تحليلهم، قاموا بتمييز الكسور المزدوج الطبيعي )ويلعب دور<br />
الفريسة( الذي ارتبط بالكسور المزدوج المستحدث تجريبيًّا )ويلعب دور الطُّعْ م( لإحداث عمليات<br />
إزفاء <strong>في</strong>ما بين الكروموسومات وبعضها. وجد الباحثون مواقع ساخنة، تتكرر <strong>في</strong>ها الكسور المزدوجة <strong>في</strong><br />
الجينات الكبيرة المنسوخة بش<strong>كل</strong> نشط، وتضاعفت مؤخرًا، وتلعب دورًا عند نقاط التشابك العصبي<br />
بين الخاليا العصبية، أو <strong>في</strong> عمليات اللتحام العصبي. وقد تم تمييز عديد من التجمعات المتكررة<br />
للكسور المزدوج عند تعريض الخاليا لالإجهاد المصاحِ ب لعملية التضاعف. ويمكن لتلك الكسور<br />
المزدوجة أن تؤدي إلى إعادة ترتيب الجينات، ما يسهم <strong>في</strong> حدوث تغيرات جينية <strong>في</strong> خاليا المخ<br />
المختلفة، أو ال أ نسجة ال أ خرى، ويصاحب ذلك تداعيات وظي<strong>في</strong>ة داخل الجسم الحي.<br />
وظائف ال أ نسجة وال أ مراض. <strong>في</strong> ورقة بحثية نُشرت <strong>في</strong> دورية<br />
"سِ ل" ،Cell قام ويي وزمالؤه 2 بعرض نظرة متفحصة <strong>في</strong> تلك<br />
ال أ سئلة، من خالل تفحُّ ص مناطق الكسر المزدوج <strong>في</strong> شريطي<br />
الحمض النووي )وتُسمى اختصارًا )DSBs التي تحدث <strong>في</strong><br />
الخاليا العصبية <strong>في</strong> الفئران.<br />
بش<strong>كل</strong> أساسي، تكمن صعوبة دراسة التباين الهي<strong>كل</strong>ي للحمض<br />
النووي <strong>في</strong> الخاليا الجسدية <strong>في</strong> التحديات التقنية التي يواجهها<br />
العلماء <strong>في</strong> الكشف عن مثل تلك ال أ حداث النادرة التي تحدث<br />
<strong>في</strong> مجموعات الخاليا، إل أن ويي وزمالءە شرعوا <strong>في</strong> استخدام<br />
تقنيات التسلسل الحساسة إلى جانب ال أ دوات المعلوماتية<br />
الحيوية، من أجل إلقاء نظرة سريعة على التباين الهي<strong>كل</strong>ي <strong>في</strong><br />
الخاليا الجسدية داخل الجسم الحي، وخاصةً <strong>في</strong> المخ، إذ<br />
وُجد أن ما يصل إلى %40 من ال أ عصاب المفردة يحتوي <strong>في</strong><br />
نطاق ماليين القواعد النووية على اختالفات <strong>في</strong> أعداد النُسَ خ<br />
)تُسمى اختصارًا ،CNVs وهي نوع من التباين الهي<strong>كل</strong>ي، يختلف<br />
<strong>في</strong>ها عدد نُسَ خ منطقة ما <strong>في</strong> الجينوم بين الخاليا وبعضها، أو<br />
بين ال أ فراد وبعضهم( ، 4,3 إل أنه بسبب انخفاض دِ قَّة العديد<br />
من ال أ ساليب، فإن مدى النتشار الحقيقي للتباين الهي<strong>كل</strong>ي<br />
<strong>في</strong> الخاليا العصبية أو الخاليا ال أ خرى غير معروف، وكذلك<br />
آليّات حدوثه.<br />
ومن ثم، استخدم ويي وزمالؤه طريقة اختبار حساسة<br />
ومحددة الهدف، تُعرف باسم "التقنية عالية الإنتاجية لتسلسل<br />
الإ زفاء الجينومي"؛ وهي تتيح الكشف على مستوى الجينوم<br />
عن الكسور المزدوج الذي يحدث بش<strong>كل</strong> طبيعي <strong>في</strong> شريطي<br />
الحمض النووي ويلعب دور الفريسة عن طريق إحداث<br />
كسر تجريبي يلعب دور الطُّعْ م <strong>في</strong> أماكن أخرى من<br />
الجينوم. تلتحم تلك الكسور <strong>في</strong> عمليات إصالح الحمض<br />
النووي الخلوية، ما يؤدي إلى حدوث إزفاء ل أ جزاء من الجينوم.<br />
ومن ثم، يتيح تسلسل مناطق اللتحام النهائية رسم خرائط<br />
لتلك الكسور، وتوصيفها على مستوى النيو<strong>كل</strong>يوتيدات.<br />
<strong>في</strong> البداية، قام الباحثون بإحداث كسر مزدوج <strong>في</strong> شريطي<br />
الحمض النووي <strong>في</strong> مواضع "الطُّعْ م" <strong>في</strong> ثالثة كروموسومات<br />
فأرية <strong>في</strong> خاليا عصبية جذعية وسل<strong>في</strong>ة )NSPCs( مستنبتة،<br />
تفتقر إلى بروتين Xrcc4 الالزم لإتمام عملية إصالح الكسر<br />
بأسلوب ربط النهايات غير التجانسي )NHEJ(؛ ويؤدي منع<br />
هذه العملية إلى تكاثر الخاليا المعاد ترتيب الجينات <strong>في</strong>ها.<br />
كما افتقرت الخاليا أيضً ا إلى بروتين p53، الذي يدعم غيابه<br />
بقاء الخلية. واستطاع الباحثون تمييز آلف الكسور التي<br />
تمثل الفريسة، حيث %61 منها يقع بالقرب من الكسور التي<br />
تمثل الطُّعْ م، أما الباقي، فكان موزعًا على الجينوم بأكمله<br />
)الش<strong>كل</strong> 1(. ومن الالفت للنظر أنه قد عُثر على العديد من<br />
تلك الكسور <strong>في</strong> ثالثة تجمعات متكررة من الكسور المزدوج<br />
)تُسمى اختصارًا .)RDCs وقد وُجد اثنان من تلك التجمعات<br />
<strong>في</strong> الجينين Lsamp وNpsa3، وهي جينات كبيرة بش<strong>كل</strong> غير<br />
عادي؛ يرمز الجين ال أ ول إلى جزيء التصاق مخصص للخاليا<br />
العصبية، ويرمز الثاني إلى عامل نسخ. أما التجمع الثالث،<br />
فهو للكسور التي تحدث بالقرب من تلك التي تمثل الطُّعْ م.<br />
وحين قام الباحثون بتطبيق النهج ذاته <strong>في</strong> الخاليا البائية<br />
الفأرية )وهي أحد أنواع الخاليا المناعية(، وجدوا تجمُّ عات<br />
متكررة من الكسور المزدوج، خاصة <strong>في</strong> الخاليا البائية، لكنهم<br />
لم يعثروا على عمليات إزفاء تتضمن جين .Lsamp ومن خالل<br />
تحليل عملية النسخ، ظهر أن جين Lsamp قد تم التعبير عنه<br />
<strong>في</strong> الخاليا العصبية الجذعية والسل<strong>في</strong>ة ،)NSPCs( لكن ليس<br />
<strong>في</strong> الخاليا البائية؛ وهو ما يشير إلى أن قابلية تعرُّض مناطق<br />
جينية محددة للكسر المزدوج <strong>في</strong> أنواع معينة من الخاليا ترتبط<br />
آليًّا بعملية النسخ.<br />
ومن ثم، قام الباحثون بدراسة تأثير الإجهاد المصاحِ ب<br />
لعملية تضاعف الحمض النووي على الكسور المزدوج، عن<br />
طريق معالجة الخاليا العصبية الجذعية والسل<strong>في</strong>ة بجرعات<br />
منخفضة من ال أ <strong>في</strong>ديكولين، وهو مثبط لإنزيمات بوليميريز<br />
الحمض النووي، يُستخدم على نطاق واسع لدراسة عدم<br />
استقرار المواقع الضعيفة الشائعة .)CFS( 5 وقد استطاع<br />
هذا النهج تمييز 24 تجمُّ عً ا متكررًا للكسور المزدوج، جميعها<br />
<strong>في</strong> الجينات، وأكثر من 300 تجمع آخر مرشح. وإجمالً ،<br />
كان 26 من بين 27 تجمُّ عً ا <strong>في</strong> جينات تزيد أحجامها على<br />
400 ألف قاعدة، و13 تجمُّ عً ا <strong>في</strong> جينات يزيد حجمها على<br />
مليون قاعدة، بما <strong>في</strong> ذلك العديد من جينات المواقع<br />
الضعيفة الشائعة. كما أن أكثر من %90 )أي 24 من أصل<br />
26( من جينات التجمعات المتكررة تلك <strong>في</strong> الخاليا العصبية<br />
الجذعية والسل<strong>في</strong>ة تلعب دورًا <strong>في</strong> الرتباطات العصبية، أو<br />
<strong>في</strong> وظائف نقاط التشابك العصبي )الوصالت الموجودة بين<br />
الخاليا العصبية(، والعديد منها مُ قْحَ م <strong>في</strong> اضطرابات النمو<br />
العصبي والضطرابات العصبية النفسية؛ وهي تشمل جينات<br />
Lsamp وNrnx1 وDcc. وقد تم استنساخ جميع جينات<br />
التجمعات المتكررة بش<strong>كل</strong>ٍ نشط، إلّ جينًا واحدً ا؛ كما أتمت<br />
جميعها أيضً ا عملية التضاعف <strong>في</strong> المرحلة "إس" S phase من<br />
دورة حياة الخلية، إلّ جينًا واحدً ا. وبمقارنة التسلسل الجيني<br />
عند نقاط التحام الفواصل <strong>في</strong> الخاليا التي تُجْ رِي عمليات<br />
إصالح الحمض النووي بواسطة أسلوب ربط النهايات غير<br />
التجانسي، وتلك التي تفتقر إلى هذا النهج، يتضح أن ربط<br />
النهايات بالطريقتين ال أ ساسية أو البديلة يتوسط عمليات<br />
الإ زفاء الجيني.<br />
وتشير هذه الكتشافات المتعلقة بكبر حجم الجينات<br />
وعمليات النسخ النشطة، وعمليات التضاعف المتأخرة،<br />
والتح<strong>في</strong>ز عن طريق التعرض لالإجهاد المصاحب لعملية<br />
التضاعف إلى أن التعارض بين عمليتي النسخ والتضاعف<br />
يسهم <strong>في</strong> رفع معدلت حدوث الكسور المزدوج، وإعادة<br />
ترتيب الجينات <strong>في</strong> الخاليا العصبية الجذعية والسل<strong>في</strong>ة. وقد<br />
ربطت دراسة سابقة 5 هذه العوامل باختالفات أعداد النسخ،<br />
وبالمواقع الضعيفة الشائعة <strong>في</strong> الخاليا اللي<strong>في</strong>ة البشرية،<br />
و<strong>في</strong> الخاليا الجذعية الجنينية الفأرية. ووجدت الدراسة<br />
أن اختالفات أعداد النسخ التي تحدث بش<strong>كل</strong> تلقائي، وتلك<br />
المستحدثة بواسطة التعرض لالإجهاد المصاحِ ب لعملية<br />
التضاعف، تقع أحجامها <strong>في</strong> نطاق يبدأ من ألف قاعدة، ويصل<br />
إلى عدة ماليين من القواعد على مدى الجينوم بأكمله، لكن<br />
مع وجود مواقع "ساخنة" <strong>في</strong> الجينات الكبيرة المنسوخة بش<strong>كل</strong><br />
نشط، التي تضاعفت مؤخرًا؛ ومنها جين LSAMP الموجود <strong>في</strong><br />
الخاليا اللي<strong>في</strong>ة البشرية، إلى جانب جينات أخرى لها وظائف<br />
عصبية. وإلى جانب ذلك.. كانت تلك المواقع الساخنة<br />
من نوع المواقع الضعيفة الشائعة كذلك، التي يؤدي <strong>في</strong>ها<br />
الهي<strong>كل</strong> الجيني وعملية التضاعف البطيئة أو المتوقفة تمامً ا<br />
إلى دخول الحمض النووي غير المضاعف <strong>في</strong> عملية انقسام<br />
خلوي فتيلي . 7,6<br />
ومن الالفت للنظر أن تلك المواقع الساخنة المحتوية على<br />
اختالفات <strong>في</strong> أعداد النسخ قد تجمعت <strong>في</strong> وسط جينات كبيرة،<br />
بنمط مشابه لنمط توزيع نقاط الكسر <strong>في</strong> التجمعات المتكررة<br />
من الكسور المزدوج، التي اكتشفها ويي وزمالؤه. وظهر عدم<br />
الستقرار هذا مرة أخرى فقط حين تم نَسْ خ الجينات. كما<br />
كان هناك تداخل ملحوظ بين الجينات المحددة <strong>في</strong> هاتين<br />
الدراستين، مع تبيُّن أن 5 من بين 9 )أي %56( من المواقع<br />
الساخنة البشرية المحتوية على اختالفات <strong>في</strong> أعداد النسخ،<br />
توافق جينات تجمعات الكسور المزدوج المتكررة، وتُظْهِ ر<br />
%52 من جينات تجمعات الكسور المزدوج المتكررة اختالفات<br />
<strong>في</strong> أعداد النسخ <strong>في</strong> الخاليا الجذعية الجنينية الفأرية.<br />
وبمالحظة نتائج ويي وزمالئه، نجد أن عدم الستقرار <strong>في</strong><br />
هذه المواقع يصحبه كسور مزدوج، غالبًا ما ينشأ بسبب شوكة<br />
التضاعف المعطلة، التي تتكون أثناء عملية تخليق الحمض<br />
النووي. وبالإضافة إلى تسبُّب تلك الكسور <strong>في</strong> حدوث عمليات<br />
الإ زفاء، فهي قد تؤدي أيضً ا إلى اختالفات <strong>في</strong> أعداد النسخ،<br />
تحدث من خالل نهج ربط النهايات، أو أي طريقة أخرى<br />
من طرق إصالح الحمض النووي. إنّ فَهْم ميل الخلية إلى<br />
تفضيل طريقة عن أخرى لإصالح نطاقات الحمض النووي<br />
التي تضررت أثناء عملية النسخ، والتنسيق <strong>في</strong>ما بينها أثناء<br />
| 68 مايو | 2016 الطبعة العربية تُطبع المجلة بدعم من مدينة الملك عبد العزيز للعلوم والتقنية<br />
© 2015 Macmillan Publishers Limited. All rights reserved